食品中锌的测定方法
出处:按学科分类—工业技术 中国轻工业出版社《食品添加剂分析检验手册》第204页(12176字)
一、葡萄糖酸锌
化学名:葡萄糖酸锌(Zinc gluconate)
结构式
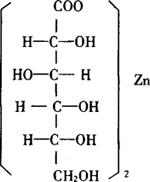
分子式:C12H22O14Zn
相对分子质量:455.69(无水物),509.73(三水物)
(一)葡萄糖酸锌的鉴别
1.试剂和溶液
1.1 亚铁氰化钾1→10水溶液,本液应临用新配。
1.2 稀盐酸 取234mL盐酸加水稀释至1000mL,摇匀。
1.3 冰乙酸。
1.4 苯肼。
2.操作步骤
2.1 取本品的水溶液(1→20)数滴,加亚铁氰化钾溶液,即发生白色沉淀,分离,沉淀在稀盐酸中不溶解。
2.2 取本品1.0g加水10mL,溶解(必要时加热),取5mL,加0.7mL冰乙酸和1mL新蒸镏的苯肼,在水浴上加热30min,冷却后,用玻璃棒磨擦试管内壁,则析出结晶。
(二)葡萄糖酸锌含量的测定
1.试剂和溶液
1.1 氨水。
1.2 氯化铵。
1.3 氨-氯化铵缓冲液(pH10) 称取5.4g氯化铵,加20mL水溶解后,加氨水35mL,再加水稀释到100mL,摇匀。
1.4 乙二胺四乙酸二钠 0.05mol/L标准溶液,按GB601《标准溶液配制方法》配制与标定。
1.5 铬黑T。
1.6 氯化钠。
1.7 铬黑T指示剂 称取铬黑T0.1g加氯化钠10g,研磨均匀,即得。
2.测定方法
取本品约0.5g,精密称定,加水100mL,使溶解(必要时加热),加氨-氯化铵缓冲液5mL,铬黑T指示剂少许,用乙二胺四乙酸二钠液滴定,至溶液呈现蓝色即得,每毫升0.05mol/L乙二胺四乙酸二钠液相当于22.78mg葡萄糖酸锌。
3.分析结果的表述

式中 w——葡萄糖酸锌(以C12H22O14Zn计)含量,%
M——乙二胺四乙酸二钠液浓度,mol/L
V——乙二胺四乙酸二钠液用量,mL
m1——样品质量,g
w1——样品水分,%
二、甘氨酸锌
化学名:甘氨酸锌(Zinc Glycinate)
结构式
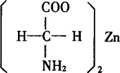
分子式:C4H8O4N2Zn
相对分子质量:205.49
1.试剂和溶液
1.1 甘氨酸锌。
1.2 亚铁氰化钾。
1.3 盐酸。
1.4 亚硝酸钠。
1.5 三氯化铁。
1.6 酚。
1.7 次氯酸钠。
2.操作步骤
2.1 锌离子反应 取本品溶液(1+10),加亚铁氰化钾试剂产生白色沉淀。沉淀不溶于稀盐酸。
2.2 取5mL本品溶液(1+10),加入5滴稀盐酸、5滴亚硝酸钠试剂(1+2),即产生无色气体。
2.3 取2mL本品溶液(1+10),加1mL三氯化铁溶液试液呈红色,加过量稀盐酸,红色消失,加过量强碱液,红色复现。
2.4 取2mL本品溶液(1+10),加1滴液体酚及5mL次氯酸钠试剂,呈蓝色。
三、乳酸锌
化学名:乳酸锌(Zinc Lactate)
结构式
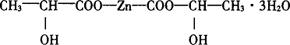
分子式:Zn(C3H5O3)2·3H2O
相对分子质量:297.97
乳酸锌的鉴别
1.试剂和溶液
1.1 乳酸锌。
1.2 溴水。
1.3 硫酸。
1.4 硫酸铵。
1.5 10%亚硝酸铁氰化钠硫酸溶液。
1.6 氨。
1.7 亚铁氰化钾。
1.8 0.1%硫酸铜。
1.9 5%硫氰酸汞铵溶液。
2.操作步骤
2.1 取本品溶液(1+10)5mL,置于试管中,加溴试液(20%)1mL与稀硫酸0.5mL,置于水浴上加热,并用玻璃棒搅拌至黄色褪去,加硫酸铵4g。混匀,沿管壁逐滴加入10%亚硝酸铁氰化钠的硫酸溶液0.2mL和浓氨液1mL,使形成两液层。放置30min,在两液层的界面处出现一暗绿色的环。
2.2 取本品溶液(1+10)5mL,加10%新配制的亚铁氰化钾溶液,即发生白色沉淀,分离,沉淀不溶解于稀盐酸。
2.3 取本品溶液(1+10)5mL,以10%稀硫酸酸化,加0.1%硫酸铜溶液1滴及5%硫氰酸汞铵溶液数滴,即产生紫色沉淀。
四、硫酸锌
化学名:硫酸锌(Zinc Sulfate)
分子式:ZnSO4·XH2O
相对分子质量:161.45(无水物),287.56(七水物)
(一)硫酸锌的鉴别
1.试剂和溶液
1.1 硫酸锌。
1.2 盐酸。
1.3 亚铁氰化钾。
2.鉴别方法
2.1 本品水溶液,加入稀盐酸使成酸性,加入亚铁氰化钾溶液(5%),生成白色沉淀。
2.2 硫酸盐试验应呈阳性。
(二)硫酸锌的含量测定
1.试剂和溶液
1.1 氨-氯化铵缓冲液(pH10.0)。
1.2 铬黑T。
1.3 0.05mol/L乙二胺四醋酸二钠溶液。
2.测定方法
取本品约0.3g,精密称定,加水30mL溶解后,加氨-氯化铵缓冲液(pH10.0)10mL与铬黑T指示剂少许,用乙二胺四醋酸二钠滴定液(0.05mol/L)滴定,至溶液自紫红色转变为纯蓝色,每毫升乙二胺四醋酸二钠滴定液(0.05mol/L)相当于14.38mgZnSO4·7H2O。
五、食品中锌的测定
(一)原子吸收光谱法
1.原理
样品经处理后,导入原子吸收分光光度计中,原子化以后,吸收波长213.8nm共振线,其吸收值与锌量成正比,与标准系列比较定量。
2.试剂和溶液
2.1 磷酸(1+10)。
2.2 盐酸(1+11) 量取10mL盐酸,加到适量水中,再稀释至120mL。
2.3 锌标准溶液 准确称取0.500g金属锌(99.99%),溶于10mL盐酸中,然后在水浴上蒸发至近干,用少量水溶解后移入1000mL容量瓶中,以水稀释至刻度,贮于聚乙烯瓶中,此溶液每毫升相当于0.50mg锌。
2.4 锌标准使用液 吸取10.0mL锌标准溶液,置于50mL容量瓶中,以0.1mol/LHCl溶液稀释至刻度,此溶液每毫升相当于100.0μg锌。
3.仪器
原子吸收分光光度计。
4.测定方法
4.1 样品处理。
4.1.1 谷类:去除其中杂物及尘土,必要时除去外壳,磨碎,过40目筛,混匀。称取约5.00~10.00g置于50mL瓷坩埚中,小心炭化至无烟后移入马弗炉中,(500±25)℃灰化约8h后,取出坩埚,放冷后再加入少量混合酸,小火加热,不使干涸,必要时加少许混合酸,如此反复处理,直至残渣中无炭粒,待坩埚稍冷,加10mL盐酸(1+11),溶解残渣并移入50mL容量瓶中,再用盐酸(1+11)反复洗涤坩埚,洗液并入容量瓶中,并稀释至刻度,混匀备用。
取与样品处理相同量的混合酸和盐酸(1+11),按同一操作方法做试剂空白试验。
4.1.2 蔬菜、瓜果及豆类:取可食部分洗净晾干,充分切碎或打碎混匀。称取10.00~20.00g,置于瓷坩埚中,加1mL磷酸(1+10),小火炭化,以下按4.1.1自“至无烟后移入马弗炉中……”起依法操作。
4.1.3 禽、蛋、水产及乳制品:取可食部分充分混匀。称取5.00~10.00g,置于瓷坩埚中,小心炭化,以下按4.1.1自“至无烟后移入马弗炉中”起依法操作。
乳类经混匀后,量取50mL,置于瓷坩埚中,加1mL磷酸(1+10),在水浴上蒸干,再小火炭化,以下按4.1.1自“至无烟后移入马弗炉中……”起依法操作。
4.2 测定 吸取0.0,0.10mL,0.20mL,0.40mL,0.80mL锌标准使用液,分别置于50mL容量瓶中,以1mol/LHCl溶液稀释至刻度,混匀(各容量瓶中每毫升分别相当于0.0,0.2μg,0.4μg,0.8μg,1.6μg锌)。
将处理后的样液、试剂空白液和各容量瓶中锌标准溶液分别导入调至最佳条件的火焰原子化器进行测定。参考测定条件:灯电流6mA,波长213.8nm,狭缝0.38nm,空气流量10L/min,乙炔流量2.3L/min,灯头高度3mm,氘灯背景校正,以锌含量对应吸光值,绘制标准曲线或计算直线回归方程,样品吸光值与曲线比较或代入方程求出含量。
5.分析结果的表述

式中 x1——样品中锌的含量,mg/kg或mg/L
ρ1——测定用样品液中锌的含量,μg/m
ρ2——试剂空白液中锌的含量,μg/mL
m1——样品质量(体积),g(mL)
V1——样品处理液的总体积,mL
结果的表述:报告平行测定的算术平均值的2位有效数字。
6.允许差
相对相差≤10%。
(二)二硫腙比色法
1.原理
样品经消化后,在pH4.0~5.5时,锌离子与二硫腙形成紫红色络合物,溶于四氯化碳,加入硫代硫酸钠,防止铜、汞、铅、铋、银和镉等离子干扰,与标准系列比较定量。
2.试剂和溶液
2.1 2mol/L乙酸钠溶液 称取68g乙酸钠(CH3COONa·3H2O),加水溶解后稀释至250mL。
2.2 2mol/L乙酸 量取10.0mL冰乙酸,加水稀释至85mL。
2.3 乙酸-乙酸盐缓冲液 2mol/L乙酸钠溶液与2mol/L乙酸等量混合,此溶液pH4.7左右。用0.1g/L二硫腙-四氯化碳溶液提取数次,每次10mL,除去其中的锌,至四氯化碳层绿色不变为止,弃去四氯化碳层,再用四氯化碳提取乙酸-乙酸盐缓冲液中过剩的二硫腙,至四氯化碳无色,弃去四氯化碳层。
2.4 氨水(1+1)。
2.5 2mol/LHCl 量取10mL盐酸,加水稀释至60mL。
2.6 0.02mol/LHCl 吸取1mL盐酸(2mol/L),加水稀释至100mL。
2.7 200g/L盐酸羟胺溶液 称取20g盐酸羟胺,加60mL水,滴加氨水(1+1),调节pH至4.0~5.5,以下按2.9用二硫腙-四氯化碳溶液(0.1g/L)处理。
2.8 硫代硫酸钠溶液(250g/L):用乙酸(2mol/L)调节pH至4.0~5.5。以下按2.9用二硫腙-四氯化碳溶液(0.1g/L)处理。
2.9 二硫腙-四氯化碳溶液(0.1g/L)。
2.10 二硫腙使用液 吸取1.0mL二硫腙-四氯化碳溶液(0.1g/L),加四氯化碳至10.0mL,混匀。用1cm比色杯,以四氯化碳调节零点,于波长530nm处测吸光度(A)。用式(9-20)计算出配制100mL二硫腙使用液(57%透光率)所需的二硫腙-四氯化碳溶液(0.10g/L)毫升数(V)。

2.11 锌标准溶液 准确称取0.1000g锌,加10mL2mol/LHCl溶液,溶解后移入1000mL容量瓶中,加水稀释至刻度。此溶液每毫升相当于100.0μg锌。
2.12 锌标准使用液 吸取1.0mL锌标准溶液,置于100mL容量瓶中,加1mL2mol/LHC]溶液,以水稀释至刻度,此溶液每毫升相当于1.0μg锌。
2.13 1g/L酚红指示液 称取0.1g酚红,用乙醇溶解至100mL。
3.仪器
分光光度计。
4.测定方法
4.1 样品消化。
4.L1 硝酸~高氯酸-硫酸法。
4.1.L1 粮食、粉丝、粉条、豆干制品、糕点、茶叶等及其他含水分少的固体食品:称取5.00g或10.00g的粉碎样品,置于250~500mL定氮瓶中,先加水少许使湿润,加数粒玻璃珠、10~15mL硝酸-高氯酸混合液,放置片刻,小火缓缓加热,待作用缓和,放冷。沿瓶壁加入5mL或10mL硫酸,再加热,至瓶中液体开始变成棕色时,不断沿瓶壁滴加硝酸-高氯酸混合液至有机质分解完全。加大火力,至产生白烟,待瓶口白烟冒净后,瓶内液体再产生白烟为消化完全,该溶液应澄明无色或微带黄色,放冷。在操作过程中应注意防止爆沸或爆炸。
加20mL水煮沸,除去残余的硝酸至产生白烟为止,如此处理2次,放冷。将冷后的溶液移入50mL或100mL容量瓶中,用水洗涤定氮瓶,洗液并入容量瓶中,放冷,加水至刻度,混匀。定容后的溶液每10mL相当于1g样品,相当加入硫酸量1mL。
取与消化样品相同量的硝酸-高氯酸混合液和硫酸,按同一方法做试剂空白试验。
4.1.1.2 蔬菜、水果:称取25.00g或50.00g,洗净打成匀浆的样品,置于250~500mL定氮瓶中,加数粒玻璃珠、10~15mL硝酸-高氯酸混合液,以下按4.1.1.1自“放置片刻……”起依法操作,但定容后的溶液每10mL相当于5g样品,相当加入硫酸1mL。
4.1.1.3 酱、酱油、醋、冷饮、豆腐、腐乳、酱腌菜等:称取10.00g或20.00g样品(或吸取10.0mL或20.0mL液体样品),置于250~500mL定氮瓶中,加数粒玻璃珠、5~15mL硝酸-高氯酸混合液。以下按4.1.1.1自“放置片刻……”起依法操作,但定容后的溶液每10mL相当于2g或2mL样品。
4.1.1.4 含乙醇饮料或含二氧化碳饮料:吸取10.00mL或20.00mL样品,置于250~500mL定氮瓶中。加数粒玻璃珠,先用小火加热除去乙醇或二氧化碳,再加5~10mL硝酸-高氯酸混合液,混匀后,以下按4.1.1.1自“放置片刻……”起依法操作,但定容后的溶液每10mL相当于2mL样品。吸取5~10mL水代替样品,加与消化样品相同量的硝酸-高氯酸混合液和硫酸,按相同操作方法做试剂空白试验。
4.1.1.5 含糖量高的食品:称取5.00g或10.0g样品,置于250~500mL定氮瓶中,先加少许水使湿润,加数粒玻璃珠、5~10mL硝酸-高氯酸混合后,摇匀。缓缓加入5mL或10mL硫酸,待作用缓和停止起泡后,先用小火缓缓加热(糖分易炭化),不断沿瓶壁补加硝酸-高氯酸混合液,待泡沫全部消失后,再加大火力,至有机质分解完全,发生白烟,溶液应澄明无色或微带黄色,放冷。以下按4.1.1.1自“加20mL水煮沸……”起依法操作。
4.1.1.6 水产品:取可食部分样品捣成匀浆,称取5.00g或10.0g(海产藻类、贝类可适当减少取样量),置于250~500mL定氮瓶中,加数粒玻璃珠,5~10mL硝酸-高氯酸混合液,混匀后,以下按4.1.1.1自“沿壁加入5mL或10mL硫酸……”起依法操作。
4.1.2 硝酸-硫酸法:以硝酸代替硝酸-高氯酸混合液进行操作。
4.1.3 灰化法:
4.1.3.1 粮食、茶叶及其他含水分少的食品:称取5.00g磨碎样品,置于坩埚中,加1g氧化镁及10mL硝酸镁溶液,混匀,浸泡4h。于低温或置水浴埚上蒸干,用小火炭化至无烟后移入马弗炉中加热至550℃,灼烧3~4h,冷却后取出。加5mL水湿润后,用细玻璃棒搅拌,再用少量水洗下玻璃棒上附着的灰分至坩埚内。放水浴上蒸干后移入马弗炉550℃灰化2h,冷却后取出。
加5mL水湿润灰分,再慢慢加入10mL盐酸(1+1),然后将溶液移入50mL容量瓶中,坩埚用盐酸(1+1)洗涤3次,每次5mL,再用水洗涤3次,每次5mL,洗液均并入容量瓶中,再加水至刻度,混匀。定容后的溶液每10mL相当于1g样品,其加入盐酸量不少于(中和需要量除外)1.5mL。全量供测定时,不必再加盐酸。
按同一操作方法做试剂空白试验。
4.1.3.2 植物油:称取5.00g样品,置于50mL瓷坩埚中,加10g硝酸镁,再在上面覆盖2g氧化镁,将坩埚置小火上加热,至刚冒烟,立即将坩埚取下,以防内容物溢出,待烟小后,再加热至炭化完全。将坩埚移至马弗炉中,550℃以下灼烧至灰化完全,冷后取出。
加5mL水湿润灰分,再缓缓加入15mL盐酸(1+1),然后将溶液移入50mL容量瓶中,坩埚用盐酸(1+1)洗涤5次,每次5mL,洗液均并入容量瓶中,加盐酸(1+1)至刻度,混匀。定容后的溶液每10mL相当于1g样品,相当于加入盐酸量(中和需要量除外)1.5mL。
按同一操作方法做试剂空白试验。
4.1.3.3 水产品:取可食部分样品捣成匀浆,称取5.00g置于坩埚中,加1g氧化镁及10mL硝酸镁溶液,混匀,浸泡4h。以下按4.1.3.1自“于低温或置水浴锅上蒸干……”起依法操作。
4.2 测定 准确吸取5.0~10.0mL定容的消化液和相同量的试剂空白液,分别置于125mL分液漏斗中,加5mL水、0.5mL200g/L盐酸羟胺溶液,摇匀,再加2滴酚红指示液,用氨水(1+1)调节至红色,再多加2滴。再加5mL二硫腙-四氯化碳溶液(0.1g/L),剧烈振摇2min,静置分层。将四氯化碳层移入另-分液漏斗中,水层再用少量二硫腙-四氯化碳溶液振摇提取,每次2~3mL,直至二硫腙-四氯化碳溶液绿色不变为止。合并提取液,用5mL水洗涤,四氯化碳层用0.02mol/LHCl溶液提取2次,每次10mL,提取时剧烈振摇2min,合并0.02mol/LHCL提取液,并用少量四氯化碳洗去残留的二硫腙。
吸取0.0,1.0mL,2.0mL,3.0mL,4.0mL,5.0mL锌标准使用液(相当0.0,1.0μg,2.0μg,3.0μg,4.0μg,5.0μg锌),分别置于125mL分液漏斗中,各加0.02mol/LHCl溶液至20mL。于样品提取液、试剂空白提取液及锌标准溶液各分液漏斗中加10mL乙酸-乙酸盐缓冲液、1mL250g/L硫代硫酸钠溶液,摇匀,再各加入10.0mL二硫腙使用液,剧烈振摇2min。静置分层后,经脱脂棉将四氯化碳层滤入1cm比色杯中,以四氯化碳调节零点,于波长530nm处测吸光度,标准各点吸收值减去零管吸收值后绘制标准曲线,或计算直线回归方程,样液吸收值与曲线比较或代入方程求得含量。
5.分析结果的表述

式中 x2——样品中锌的含量,mg/kg或mg/L
m2——测定用样品消化液中锌的质量,μg
m3——试剂空白液中锌的质量,μg
m1——样品质量,g(mL)
V2——样品消化液的总体积,mL
V3——测定用消化液的体积,mL
结果的表述:报告平行测定的算术平均值的二位有效数字。
6.允许差
相对相差≤10%。
(三)双硫腙比色法(一次提取)
1.原理
同本节(二)。
2.试剂和溶液
2.1 乙酸-乙酸盐缓冲液 同本节(二)2.3。
2.2 250g/L硫代硫酸钠溶液 同本节(二)2.8。
2.3 二硫腙-四氯化碳溶液(0.01g/L)。
2.4 氨水(1+1)。
2.5 锌标准使用液 同本节(二)2.12。
2.6 2g/L甲基橙指示液 称取0.2g甲基橙,用乙醇(20%)溶解,并稀释至100mL。
3.仪器
分光光度计。
4.测定方法
4.1 样品消化 同本节(二)4.1。
4.2 测定 准确吸取5.0~10.0mL定容的消化液和相同量的试剂空白液,分别置于125mL分液漏斗中,加水至10mL。
吸取0.0,1.0mL,2.0mL,3.0mL,4.0mL,5.0mL锌标准使用液(相当0.0,1.0μg,2.0μg,3.0μg,4.0μg,5.0μg锌),分别置于125mL分液漏斗中,各加水至10mL。
于样品消化液、试剂空白及锌标准液中各加1滴甲基橙指示液,用氨水调至由红变兰,再各加5mL乙酸-乙酸盐缓冲液及1mL硫代硫酸钠溶液(250g/L)混匀后,各加10.0mL双硫腙-四氯化碳溶液(0.01g/L),剧烈振摇4min,以下按本节(二)4.2自“静置分层……”起依法操作。
5.分析结果的表述
同本节(二)5。