离子不能大量共存的判断方法
书籍:高中数理化公式定理大全
出处:按学科分类—文体、科学、教育 商务印书馆国际有限公司《高中数理化公式定理大全》第349页(904字)
1.结合生成难溶物质的离子不能大量共存,如Fe2+与S2—、Ca2+与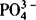 ,Ag+与I—等.
,Ag+与I—等.
2.结合生成气体物质的离子不能大量共存,如S2—与H+,H+与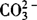 ,
,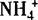 与OH等
与OH等
3.结合生成难电离物质的离子不能大量共存,如:H+与OH—,H+与CH3COO—,H+与F—等.
4.发生氧化还原反应的离子不能大量共存,如:Fe3+与S2—,Fe3+与I—,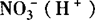 与Fe2+等.
与Fe2+等.
5.发生水解反应相互促进的离子不能大量共存,如Al3+,Fe3+分别与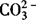 、HCO3—、
、HCO3—、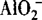 ;Al3+与S2—等.
;Al3+与S2—等.
6.弱酸酸式酸根离子不能与H+、OH共存,如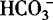 与H+,HCO3—与OH—,
与H+,HCO3—与OH—,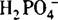 与H+,
与H+,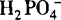 与OH—等.
与OH—等.
7.在题目中提示酸性溶液(pH<7)或碱性溶液(pH>7)应在各待选答案中均加入H+或OH—考虑.
8.在题目中告知是无色溶液,应在各待选答案中排除具有颜色的Fe3+、Cu2+、Fe2+、MnO4—等离子.
例 下列各组离子,在强碱性溶液中可以大量共存的是( ).
A.K+、Na+、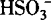 、Cl
、Cl
B.Na+、Ba2+、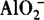 、NO3—
、NO3—
C.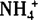 、K+、Cl—、NO3—
、K+、Cl—、NO3—
D.K+、Na+、ClO—、S2—
解析 A中的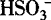 、C中的
、C中的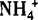 均不能与OH—大量共存;而D项中ClO—具有强氧化性,能与具有还原性的S2—发生氧化还原反应而不能共存.
均不能与OH—大量共存;而D项中ClO—具有强氧化性,能与具有还原性的S2—发生氧化还原反应而不能共存.
答 B.
上一篇:离子方程式的正误判断
下一篇:高中数理化公式定理大全目录