达到化学平衡状态的标志
出处:按学科分类—文体、科学、教育 商务印书馆国际有限公司《高中数理化公式定理大全》第393页(1170字)
1.v正=v逆·2.各组分的物质的量、质量、含量保持不变.
注意 化学平衡还可以从以下几方面进行判断:
①全是气体参加前后系数改变的可逆反应,压强保持不变.
②全是气体参加的前后系数改变的可逆反应,平均相对的分子质量保持不变.
③对于有颜色物质参加或生成的可逆反应,颜色不随时间变化而变化.
④对同一物质而言,断裂化学键的物质的量与形成化学键的物质的量相等.
⑤对于绝热体中进行的可逆反应,体系温度不随时间变化而变化.
例1 (1999.广东·6)在一定温度下,可逆反应 达到平衡的标志是( ).
达到平衡的标志是( ).
A.Z生成的速率与Z分解的速率相等
B.单位时间生成amolX,同时生成3amolY
C.X、Y、Z的浓度不再变化
D.X、Y、Z的分子数比为1∶3∶2
解析 选项A和选项C符合上述对平衡状态的描述,因而可作为达到平衡状态的标志.选项B的叙述,只要是可逆反应都是正确的,因而不能作为达到平衡状态的标志,选项D描述的是反应中X、Y、Z三种物质的化学计量数之比,与平衡状态无关.
答 A、C.
例2 可逆反应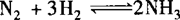 的正、逆反应速率可用各反应物或生成物浓度的变化来表示,下列各关系中能说明反应已达到平衡状态的是( ).
的正、逆反应速率可用各反应物或生成物浓度的变化来表示,下列各关系中能说明反应已达到平衡状态的是( ).
A.v正(N2)=v正(H2)
B.v正(N2)=v逆(NH3)
C.2v正(H2)=3v逆(NH3)
D.v正(N2)=3v正(H2)
解析 化学平衡是可逆反应在一定条件下正逆速率反应达到相等的状态.用不同物质表示化学反应速率的数据是不相同的,但速率之比即为化学方程式中的计量数之比.对照各选项,只有C符合题意.
答 C.