用惰性电极电解电解质溶液的规律
出处:按学科分类—文体、科学、教育 商务印书馆国际有限公司《高中数理化公式定理大全》第456页(1162字)
1.电解水型:含氧酸、强碱、活泼金属的含氧酸盐(如NaOH、H2SO4、K2SO4等)的电解.
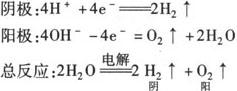
2.分解电解质型:无氧酸(除HF外)、不活泼的无氧酸盐(氟化物除外)(如HCl CuCl2等)溶液的电解
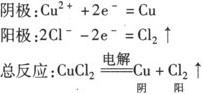
3.放氢生碱型:活泼金属的无氧酸盐(氟化物除外)(如NaCl、MgBr2)溶液的电解
阴极:2H++2e—=H2↑
阳极:2Cl——2e—=Cl2↑
总反应:
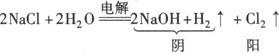
4.放氧生酸型:不活泼金属的含氧酸盐(如CuSO4、AgNO3等)溶液的电解.
阴极:2Cu2++4e—=2Cu
阳极:4OH——4e—=O2↑+2H2O
总反应:
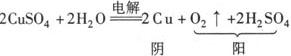
注 (1)活性电极是指除Au、Pt以外的金属电极,它与活泼金属作电极不能划等号.
(2)各种电解质的电解实质,可通过以H+与OH—为分界线进行分析判断,同时还可判断电解质溶液电解前后溶液的pH变化情况.一般规律为:
①pH变大:电解活泼金属的无氧酸盐(氟化物除外)、强碱溶液、不活泼金属的无氧酸盐溶液、无氧酸酸(HF除外).如:NaCl溶液、NaOH溶液、CuCl2溶液(若考虑Cl2的溶解则pH减小)、盐酸的电解.
②pH不变:电解活泼金属的含氧酸盐溶液.如NaNO3、K2SO4等盐溶液的电解.
③pH减小:电解不活泼金属的含氧酸盐溶液、含氧酸溶液.如:AgNO3溶液、硫酸溶液的电解.
(3)电解质溶液电解后溶液浓度恢复的原则:什么离开溶液体系就加什么(相当的物质也行);多少离开就加多少.如用惰性电极电解CuSO4溶液一段时间后,由子电解时析出Cu和放出O2,所以可以加入适量的CuO或CuCO3可使溶液恢复原浓度.