图象题的常见题型
出处:按学科分类—文体、科学、教育 商务印书馆国际有限公司《初中数理化公式定理大全》第366页(3719字)
1.溶解度曲线的图象2.金属活动性顺序的图象题3.pH变化的图象题4.溶质质量分数的图象题5.化学反应的图象题6.根据化学方程式计算的图象题等.
例1 如图是a、b两种固体物质的溶解度曲线,下列说法正确的是( ).
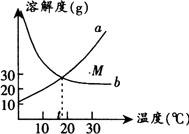
A.a的溶解度大于b的溶解度
B.在t℃时,a、b的溶解度相同
C.a、b都属易溶物质
D.M点时a、b溶液都是饱和溶液
E.当a中有少量b时,可以用结晶法提纯a
【分析】 溶解度曲线是固体物质的溶解度与温度间的一种函数关系,它具有三个意义:(1)同种物质在不同温度时的溶解度.曲线及以上的任一点都表示物质达到了饱和状态,而曲线下的点都未达到饱和,故M点时b达到饱和,a未达到饱和,D错.(2)不同物质在同一温度时的溶解度比较.A中没有指明温度,a、b曲线相交,无法比较大小,相交的交点是指在该温度时溶解度相同,所以A错B对.由图得到:20℃时a、b的溶解度都大于10克,属于易溶物质,故C对.(3)物质的溶解度受温度变化影响的大小趋势,从图中曲线可知a的溶解度随温度升高而增大,b却减少,所以a适于用结晶法提纯而b不适宜,E对.
答案 B、C、E.
例2 等质量的三种金属a、b、c分别和足量的溶质质量分数相同的稀硫酸反应,都生成相同价态的硫酸盐,其反应情况如图所示,问:
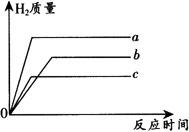
(1)三种金属活动顺序由强到弱的是_____.
(2)三种金属相对原子质量由大到小的是____.
解析 由图象可知,斜线表示金属和酸的反应速率,越陡,速率越快,金属活动性越强,因此(1)的答案是a>c>b.横线表示完全反应后生成H2质量,越高,生成H2越多,产生H2质量为a>b>c.结合题意,通过计算可知,等质量的金属产生氢气的质量由金属相对原子质量确定,越大,产生H2质量越少,则金属相对原子质量顺序是c>b>a.
答案 (1)a>c>b;(2)c>b>a.
例3 向一定量的Ba(OH)2溶液中逐滴滴入稀H2SO4,与反应有关的变化关系如图所示,其中正确的是( ).
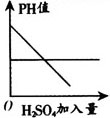
A
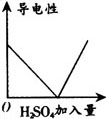
B
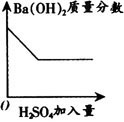
C
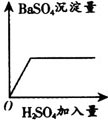
D
解析 由于Ba(OH)2+H2SO4=BaSO42H↓(2O是典型的酸碱中和反应,图中横坐标都是硫酸加入量,随着硫酸加入,反应逐渐完全至硫酸过量,因此Ba(OH)2的质量分数应减少至0,故C错,自由移动的离子越来越少,故溶液导电性减弱至0,再因过量的H2SO4电离,溶液的导电性又增强,PH值减小至7后继续减小,而生成BaSO4沉淀量达到最大值后再不发生改变了,因此正确为A、B、C,
答案 D.
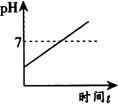
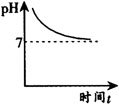
例4 某种药片的有效成分中的氢氧化镁,能减缓因胃酸过多引起的疼痛,在氢氧化镁与胃酸作用的过程中,胃液pH变化的情况是( ).
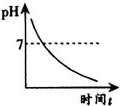
A
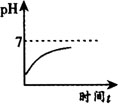
B
C
D
【分析】 因胃酸过多,故开始胃液一定显酸性,排除A和D.氢氧化镁与胃酸作用,而使酸性变弱,但不能变成碱性,故排除C.选B.
答案 B.
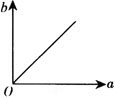
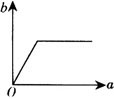
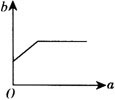
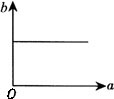
例5 在一定温度下,向一定量的水中不断加入氯化钠固体,并搅拌.在此过程中,溶质的质量分数(b)与加入氯化钠质量(a)的变化关系如下图所示,其中正确的是( ).
【分析】 由于加氯化钠固体前水中不存在氯化钠,溶液中氯化钠的质量分数应该是从零开始的,故排除C、D.随着加入的氯化钠固体不断溶解,溶液由不饱和逐渐变为饱和,氯化钠的质量分数也不断地增大,当氯化钠
A
B
C
D
达到饱和状态后,继续加入氯化钠固体将不再溶解,其质量分数也不再变化,反映在图象上将出现与横坐标平行的一条射线.
答案 B.
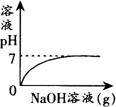
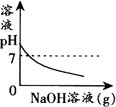
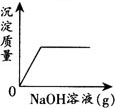
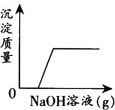
例6 向HCl和FeCl3的混合溶液中不断加入NaOH溶液,下图曲线正确的是( ).
A
B
C
D
解析 HCl和FeCl3的混合溶液显酸性,其溶液pH<7,向混合溶液中不断加入NaOH溶液,发生如下反应:HCl+NaOH=NaCl+H2O,FeCl3+3NaOH=Fe(OH)33NaCl.溶液的酸性逐渐减弱,其pH将增大;当恰好反应完全时,pH=7,若继续加入NaOH溶液,其pH将大于7,由此可排除A、B.由于NaOH先和HCl发生中和反应,反应完后再与FeCl↓(3反应生成Fe(OH)3沉淀,故产生的沉淀不能从零点开始,且当FeCl3反应完毕,再加NaOH溶液沉淀的量不再发生变化,综上所述,应选D.
答案 D.
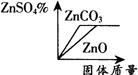
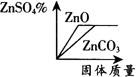
例7 将某H2SO4溶液分成两等份,分别向其中加入足量的ZnO、ZnCO3固体,充分反应,所得ZnSO4溶液质量分数与所加固体质量关系图正确的是( ).
A
B
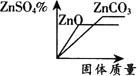
C
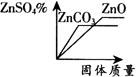
D
【分析】 由于是等质量的H2SO4与足量的ZnO、ZnCO3固体充分反应,所以生成ZnSO4的质量相等,即溶质的质量相同,故欲判断反应后所得溶液的溶质质量分数大小,只要看“反应生成的水的多少”,无需计算,观察化学方程式:ZnO+H2SO4=ZnSO4+H2O,ZnCO3+H2SO4=ZnSO4+H2O+CO2难看出,生成水的量也相同,故反应后所得溶液的溶质质量分数大小相同,排除C、D.由于ZnCO↓(3的相对分子质量比ZnO的大,故与等质量的H2SO4反应所需的ZnCO3固体的质量大于ZnO的质量.
答案 B.
例8 用相同质量的铁和锌跟一定量的稀硫酸反应,其反应过程如图所示(图中横、纵坐标分别表示反应的时间t和产生H2的质量).试回答:
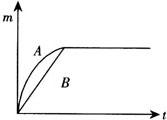
(1)曲线A表示的是__跟稀硫酸反应的情况;
(2)图象除说明(1)的结论外,还可以得出另外两个结论,它们是__.
解析 (1)根据金属活动性顺序知,锌排在铁的前面,所以锌跟稀H2SO4反应要比铁快,可见曲线A表示锌与稀H2SO4反应.
(2)由图象知,产生H2的质量相等,而题设Zn、Fe质量相同,故知稀H2SO4均不足量,或Zn、Fe均过量(足量).