开放性试题
出处:按学科分类—文体、科学、教育 商务印书馆国际有限公司《初中数理化公式定理大全》第373页(4358字)
此类题目一般答案不惟一,为学生提供了广阔的思维空间和充分展示自己才智的机会.解题中只要按照常规思路分析、解出符合题意的答案即可.
例1 科学家正研究在太空建一座把太阳光变成激光的装置,然后用激光照射添加了催化剂二氧化钛(TiO2)的水,水就能有效地分解产生氢气和氧气,即
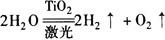
某同学看到此化学方程式,即想到以下两点:(1)水在激光和催化剂TiO2的作用下,能产生氢气和氧气;(2)每36g水可分解生成4g氢气和32g氧气.
你还能想到更多吗?请将你的想法填写到下面的空白中(再任写两点):__;____.
【分析】 这是一道根据化学方程式信息去联想的开放性试题,化学方程式从质变和量变两方面表示的意义已给出,答题可从化学反应的类型、质量守恒的原因、由化学式去联想物质的组成等方面回答.可从以下答案中任选两条:(1)化学反应前后氢原子的个数不变;(2)化学反应前后元素的种类不变;(3)此反应为分解反应;(4)水由氢元素和氧元素组成;(5)每2个水分子分解生成2个氢分子和1个氧分子.
例2 有一包固体粉末,可能由CaCO3、Na2SO4、Na2CO3、CuSO4和BaCl2中的一种或几种组成,做实验得以下结果:
(1)此固体粉末加到水中,得到白色沉淀,上层清液为无色;
(2)滴入足量稀硝酸后白色沉淀部分溶解.
从实验可判断出,该粉末可能的三组组成:<1>__;<2>__;<3>____.
【分析】 由实验结论逆推物质的组成,需要具有良好的分析、判断和逻辑思维能力.由(1)可知,上层清液无色,说明不含CuSO4,白色沉淀不溶于水,可能是CaCO3、BaCO3、BaSO4中的一种或多种;由(2)可知,沉淀部分溶解,说明沉淀一定含有BaSO4,可能含有CaCO3、BaCO3中的一种或两种.所以三组答案为:
<1>CaCO3、Na2SO4、BaCl2;
<2>Na2CO3、Na2SO4、BaCl2;
<3>CaCO3、Na2SO4、Na2CO3、BaCl2.
例3 向盛有一种无色溶液的试管中加入另一种无色溶液,生成了一种白色沉淀.试根据你学过的酸、碱、盐的性质,推断生成的白色沉淀可能是哪几种物质,参加反应的两种相应无色溶液各是什么?(写出三种推测)

【分析】 要求根据酸、碱、盐的性质推断,范围较大.反应物为两种无色溶液,生成物有一种白色沉淀的复分解反应有以下四种类型:
(1)碱+酸=盐+水,例如:
Ba(OH)2+H2SO4=BaSO42H↓(2O
(2)碱+盐=另一种碱+另一种盐,例如:
Ca(OH)2+Na2CO3=2NaOH+CaCO3/p> 2NaOH+MgSO↓(4
(3)酸+盐=另一种酸+另一种盐,例如:
H2SO4+BaCl2=2HCl+BaSO4/p> HCl+AgNO↓(3 (4)盐+盐=另外两种盐,例如: BaCl↓(2
AgNO↓(3+NaCl=AgClNaNO↓(3
CaCl2+Na2SO3=CaCO32NaCl
答案 可从以上任选三种白色沉淀及它们各自对应的两种无色溶液.
例4 X、Y、Z是初中化学常见的单质,A、B是与它们相关的两种化合物,它们的相互关系如下图所示.请写出两组符合条件的单质及化合物的化学式.

(1)X____,Y____,Z____,A____,B____.
(2)X____,Y____,Z____,A____,B____.
【分析】 这道开放性推断题,在初中化学知识范围内回答,综合判断能力要求高.X、Y、Z是单质,A、B是化合物,反应类型可有:
X+A→Y+B,属于置换反应;X+Z→B,Y+Z→A,属于化合反应.
可以判断,置换反应又是氧化还原反应,可能有氧的得失,Z选氧气较合适,X可是H↓(2、C,A可是CuO、Fe3O4等.答案可从下面选两组:
(1)X是H2,Y是Cu,Z是O2,A是CuO,B是H2O.
(2)X是H2,Y是Fe,Z是O2,A是Fe3O4,B是H2O.
(3)X是C,Y是Cu,Z是O2,A是CuO,B是CO2.
(4)X是C,Y是Fe,Z是O2,A是Fe3O4,B是CO2.
例5 在“氧气的制取和性质”实验课中,某同学取一段纱窗网上的细铁丝,在自己收集到的氧气中做“铁丝在氧气中燃烧”的实验.结果没有观察到“火星四射”的现象,请分析此实验失败的一种可能原因:____.____.
【分析】 此题以实验中出现的异常现象进行命题,考查纠错能力和探究能力.解题时,应从铁丝在氧气中燃烧具备的条件与实验技能等方面进行分析,探究实验失败的各种原因.
(1)从学生收集氧气的情况分析,如收集的氧气纯度太低等;
(2)从铁丝情况分析,如铁丝生锈或含油漆等;
(3)从燃烧条件分析,如未达到着火点等.
例6 已知几种离子或原子的结构、带电情况及其化合价如下表所示.

通过此表总结出:“带电荷的原子属于离子”.还能总结出:
①____;
②____;
③____;
④____;
⑤____.
【分析】 运用归纳总结的方法,从题给信息中发现规律,答案不惟一,可归纳为:
①核电荷数大于核外电子总数为阳离子;
核电荷数小于核外电子总数为阴离子;
②核外电子数相同而核电荷数不同,可分属不同元素;
③原子失去的电子数等于某元素正价数;
④核外电子排布相同,可分别是阳离子、原子、阴离子;
⑤阴离子电荷数=化合价数=8-原子最外层电子数.
例7 有三瓶失去标签的试剂,只知道它们分别是NaOH溶液,NaCl溶液,Na2SO4溶液.现有石蕊试液,酚酞试液,KNO3溶液,BaCl2溶液可供选用.要通过实验将它们区别开来,请将有关物质或实验现象填入下图所示的方框中,每个方框中只填写一种物质或实验现象.

解法一
①酚酞试液②变成红色③NaOH④NaCl⑤Na2SO4溶液⑥BaCl2溶液⑦白色沉淀⑧Na2SO4溶液⑨NaCl溶液
解法二
①石蕊试液②变成蓝色③NaOH溶液④NaCl溶液⑤Na2SO4溶液⑥BaCl2溶液⑦白色沉淀⑧Na2SO4溶液⑨NaCl溶液
解法三
①BaCl2溶液②白色沉淀③Na2SO4溶液④NaOH溶液⑤NaCl溶液⑥酚酞试液⑦变成红色⑧NaOH溶液⑨NaCl溶液
解法四
①BaCl2溶液②白色沉淀③Na2SO4溶液④NaOH溶液⑤NaCl溶液⑥石蕊试液⑦变成蓝色⑧NaOH溶液⑨NaCl溶液