苯的性质
出处:按学科分类—文体、科学、教育 商务印书馆国际有限公司《高中数理化公式定理大全》第422页(1310字)
1.苯的物理性质:苯是没有颜色,带有特殊气味的液体,有毒,不溶于水,密度比水小,熔点5.5℃,沸点80.1℃
2.苯的化学性质
苯分子中特殊的键决定了其化学性质的独特性:兼有饱和烃、不饱和烃的性质,能发生取代反应和加成反应.
(1)取代反应

HBr
注 a.苯只与液溴发生反应,不与溴水反应.溴水中的溴可被苯萃取.
b.该反应中加入的催化剂是铁粉,实际起催化作用的是FeBr3.
c.有关实验中的几个问题:
(ⅰ)试剂加入顺序:先加苯,再加溴,最后加铁粉.
(ⅱ)长导管的作用:因该反应是放热反应且苯和Br2易挥发,长导管除了导气外,兼起冷凝作用.
(ⅲ)现象:导管口有白雾(生成的HBr溶于水)、水底有油状液体(溴苯不溶于水、密度比水大);锥形瓶中加AgNO3溶液有浅黄色沉淀生成.
(2)硝化反应
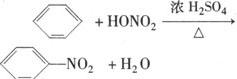
注意 a.浓HNO3和浓H2SO4混合放出大量的热,所以加入试剂时应将浓H2SO4慢慢加入到浓HNO3中,并冷却到50℃~60℃后再加入苯.
b.浓H2SO4的作用是催化剂和吸水剂
c.加热方式:水浴加热,这样便于控制温度且能使反应混合物受热均匀.温度计水银球应放入水浴中.
d.硝基苯是无色、有苦杏仁味的油状液体,密度比水大,有毒.
(3)磺化反应
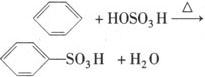
浓H2SO4在此反应中是反应物.生成的苯磺酸水溶液呈酸性.
(4)加成反应

3.苯的燃烧反应
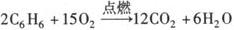
注意 a.因苯的含碳量高(与C2H2相同),苯在空气里燃烧时火焰明亮并带有浓烟.
b.苯不能被酸性KMnO4溶液氧化,也不与溴水反应(溴水中的溴可被苯萃取).