血栓性微血管病
出处:按学科分类—医药、卫生 科学技术文献出版社《肾脏内科疾病诊断标准》第151页(6052字)
一、概述
溶血性尿毒症综合征(HUS)由Gasser于1955年首先报道,它与1925年Moschcowitz报道的血栓性血小板减少性紫癜(TTP)临床表现极为相似,均以微血管病性溶血性贫血、血小板减少、急性肾衰竭(ARF)、发热、中枢神经系统病变为主要临床表现。过去认为,这是两种不同的疾病,许多基础和临床研究证实此两种疾病在发病机理、病因和病理改变大致相同,故目前统称为TTP与HUS综合征或血栓性微血管病(TMA)。
二、流行病学
TTP与HUS并非少见疾病,国内外报道其占ARF发生率2.7%~12.0%,且呈不断上升趋势。因其发病机理和病因未完全明确,病程凶险,无特殊有效预防手段,预后相对较差。随着包括血浆置换和免疫吸附等治疗手段不断进步,TTP与HUS预后大为改观。未治疗的TTP与HUS病死率90%~100%,治疗后存活率达90%~93%,肾脏治愈率可达50%~60%。国外HUS为常见病,特别是在小儿ARF中占首位,与过去呈爆发性不同,现多散发性发作。
三、病因
病因未明,目前认为与下列因素有关。
1.感染 感染是诱发儿童TMA的首位因素。
(1)细菌感染:如大肠杆菌、志贺痢疾杆菌、伤寒杆菌、肺炎球菌。
(2)病毒感染:包括柯萨奇病毒、埃可病毒、流感病毒、巨细胞病毒、人类免疫缺陷病毒(HIV)等均可诱发TMA。
2.药物 多种药物包括化疗药物如丝裂霉素、长春新碱、柔红霉素等;环孢霉素A、避孕药物或其他含雌激素的药物、青霉素、保泰松、奎宁等均可诱发TMA。
3.遗传缺陷 不少报道显示HUS者伴G6PD缺陷,国内亦有病例报道。
4.妊娠 妊娠期特别是伴有先兆子痫、胎盘早剥等并发症的孕妇可并发TMA,而病死率很高。
5.其他 目前TMA的家族性发病已有很多报道,一般认为HUS为常染色体隐性遗传。另外,自身免疫功能紊乱性疾病如SLE、类风湿性关节炎、硬皮病、抗磷脂抗体综合征均可引起TMA,骨髓、肾等移植后也可引发TMA;某些癌症如胃肠道淋巴癌也常是并发本病的病因。
四、发病机理
(一)HUS的发病机理
HUS发病机理迄今未明确,可能是多种机理联合作用。血管内皮细胞损伤、凝血纤溶障碍、血小板活化、自身免疫反应以及遗传因素近来报道增多。
1.肾脏局部的微血管性溶血及血管内凝血 这是HUS的主要发病机理。某些有害因素(如细菌及其内毒素或药物成分)损伤了肾小球毛细血管内皮细胞,致使血小板在肾小球毛细血管内皮细胞损伤处聚积、并使纤维蛋白在损伤部位沉积,而形成了纤维蛋白丝网。血流中的红细胞和血小板在流经肾脏毛细血管时即可受到纤维蛋白丝网的机械冲撞而破裂,从而引起了微血管性溶血性贫血和血小板减少。另一方面由于这种微血管病和内皮细胞的肿胀,引起了肾内血循环障碍及广泛的肾内微血管的血栓栓塞,致使肾小球滤过率急剧下降,重症可发生肾皮质坏死,最终导致急性肾衰竭。
(1)妊娠:正常妊娠妇女血循环中的纤维蛋白原、第Ⅶ、Ⅷ、Ⅴ凝血因子升高,而纤溶能力降低,处于高凝状态。当出现流产、胎盘早剥及子痫等并发症时,胎盘释放出促凝血酶原激酶可导致血栓形成而致病。
(2)血小板活化作用增强:血小板活化因子(PAF)由血小板、肾小球系膜细胞、内皮细胞产生,可促进血小板聚集和活化。有研究发现,儿童HUS急性期尿中PAF浓度明显升高,恢复期则下降,提示PAF参与了HUS的病理过程。
(3)前列环素(PGI2)和血栓素A2(TXA2)失衡:正常情况下PGI2通过兴奋血小板膜上腺苷酸环化酶受体和抑制血小板上纤维蛋白原受体发挥抗血小板聚集、黏附和血栓形成作用,并与促进血小板聚集的TXA2保持动态平衡。当内皮细胞受损伤后,产生PGI2明显减少,另外有学者指出HUS患者血浆中缺乏PGI2合成的刺激因子,因此导致血栓形成。
(4)神经氨酸酶:神经氨酸酶为一种有害因子,可损伤肾小球毛细血管内皮细胞而致病。HUS常与肺炎双球菌感染有关,因肺炎双球菌能产生此酶,而该酶能使肾小球毛细血管内皮细胞、红细胞和血小板膜上的Thomsen—Friedenerich抗原(T—抗原)暴露,致使血浆中出现抗T—抗原的IgM抗体,抗原与抗体相互作用后使红细胞和血小板聚集于毛细血管损伤处而致病。
(5)活性代谢产物:HUS时,红细胞的自身抗氧化能力降低,红细胞的超氧化物歧化酶(SOD)减少而红细胞膜的脂质过氧化产物丙二醛(MDA)增加,致使异常的脂质过氧化物出现,有助于血小板的聚积。又由于红细胞的抗氧化能力减退,致使红细胞寿命缩短、易发生溶血,促使HUS的贫血更加严重。
(6)细胞内毒素:①使细胞因子释放介导内皮细胞损伤而发病;②激活巨噬细胞使活性氧代谢产物增加;③激活中性粒细胞,增加细胞表面受体表达,促进白细胞聚集,致使中性粒细胞介导的细胞毒损伤;④激活补体与血小板活化因子,参与发病。
2.免疫机理 HUS的发病可能与免疫有关。其原因为:①HUS发病前2/3以上病例有呼吸道或胃肠道的细菌感染,符合抗原—抗体反应的发病过程;②部分患者于病初期可见IgG减少而IgA、IgM升高,C3下降。或可测得C3b、C3c碎片、C3NeF和B因子。肾组织免疫荧光检查可见IgM、C3、C1q、备解素及纤维蛋白原的沉积。
(二)TTP的发病机理
TTP与HUS的发病机理相同,均为肾脏局部的血管内凝血、肾内微血栓及微血管性溶血。还包括以下几种:
1.血浆中异常大分子VWF肽的作用 TTP患者血循环中出现异常的大分子肽(von Willebrand factor,VWF肽),它是由内皮细胞合成的VWF肽聚集而成。在TTP急性期,患者血浆中此种大分子VWF肽浓度急剧升高。而在病恢复期浓度下降,在慢性反复发作期亦升高。大分子VWF肽能使血小板在毛细血管内皮细胞损伤处黏附、聚集,从而引起微血管血栓。
2.PGI2的代谢异常 有作者提出TTP患者缺乏由内皮细胞产生的PGI2合成因子。另有作者报道TTP患者PGI2破坏速度极快,此乃由于患者血浆中缺乏PGI2稳定因子。另外,血小板聚集时释放出的β—血小板球蛋白,也具有破坏PGI2合成的作用。
3.组织—纤溶酶原活化剂(tissue—plasminogen activator,t—PA)活性降低 TTP时,毛细血管内皮细胞的另一异常是缺乏活性的t—PA,从而纤溶活性降低,使已形成血栓的微血管难以再疏通。
4.血小板聚集蛋白参与发病 血小板聚集蛋白是作用于血小板膜上具有抗原性的糖蛋白GPⅡb和GPⅢa而使血小板聚集。另有报道某些TTP者的血小板聚集活性与钙依赖性半胱氨酸蛋白酶有关。
5.免疫机理 ①该病常见于药物过敏反应后;②TTP患者血清补体水平降低;③血管病变处可见免疫球蛋白和补体成分;④血液循环中可找到循环免疫复合物。
五、分类
血栓性微血管病可分为两类:溶血性尿毒症综合征(HUS)和血栓性血小板减少性紫癜(TTP)。溶血性尿毒症综合征(HUS)由Gasser于1955年首先报道。其临床特点是微血管性溶血性贫血、急性肾功能不全和血小板减少,构成三联综合征。如同时伴有神经系统症状和发热成五联综合征时,则称之为血栓性血小板减少性紫癜。
六、临床表现
典型的HUS一般发病前2~14日常有先兆性腹泻,且多为出血性腹泻。成人及小儿均可见,但主要发生于婴幼儿和儿童,其流行期约在每年的6~9月。在发病前常有腹泻、腹痛、呕吐等胃肠炎症状,易误诊为急腹症。非典型HUS部分可有呼吸道症状,或有家族史,另外与肿瘤、恶性高血压、先兆子痫等有关。TTP为一种散发性病例,任何年龄均可发病,以30~40岁为发病高峰,90%呈急性经过。其与HUS在以下几方面存在类似与不同点。
1.微血管病性溶血性贫血 HUS及TTP均表现明显,在数日内患者血红蛋白下降显着,网织红细胞升高,游离胆红素水平升高,血浆乳酸脱氢酶及其同工酶—丙酮酸脱氢酶活性升高,外周血涂片可见红细胞碎片及变形红细胞、幼红细胞;有时可出现血红蛋白尿。
2.血小板减少致出血 TTP全身各处均有可能出血,以皮肤和黏膜为主,严重者可有颅内出血,一般血小板减少呈重度;而HUS最易出血部位在胃肠道,血小板减少程度较轻。
3.神经系统症状 见于84%~92%的TTP患者和40%的HUS患者,如头痛、头晕、精神错乱、惊厥、视力障碍、失语、肢体麻木、昏迷等。
4.肾功能损害 76%~88%的TTP患者和几乎100%的HUS患者可累及肾脏,TTP患者肾脏受累多为轻度,可有血尿、蛋白尿,40%~80%有轻度氮质血症;而急性肾衰竭是HUS的重要临床表现,绝大多数病例有少尿或无尿,此外由于血容量增多,高血压、心衰的发生率也高于TTP。
5.发热 TTP患者59%~98%可出现不同程度的发热,而HUS则相对较少。
七、检查
1.溶血性贫血 短期内血红蛋白下降,严重者可降30g/L,但与急性肾衰竭的严重程度并不一致;末梢血网织红细胞升高可达6%~19%;血涂片可见破碎红细胞,比例10%以上;血清间接胆红素升高,抗人体球蛋白实验(Coombs’test)阳性;血浆乳酸脱氢酶及其同工酶升高。
2.血小板减少 最低可达10×109/L,1~2周后恢复,下降程度和持续时间与肾衰竭的严重程度无关,骨髓象可见巨核细胞形态正常,仅数目减少。
3.白细胞升高 可达(20~30)×109/L,与急性肾衰竭的严重程度及预后有关。
4.凝血和纤溶指标异常 凝血酶原时间、部分凝血活酶时间及Ⅴ和Ⅷ因子多正常,早期纤维蛋白原减少,其降解产物增高。
5.肾功能异常 尿蛋白多为1~2g/L,尿常规镜检可见红细胞、白细胞及管型,血尿酸和尿素氮、血肌酐升高更显着。
八、诊断
1.HUS同时或先后出现出血、溶血、肾功能不全及神经系统症状的患者应考虑HUS的存在。临床上具备微血管性溶血性贫血、血小板减少及急性肾功能不全三联症者,HUS诊断可成立。肾活检可帮助确诊及估计预后。
2.74%病例有血小板减少、微血管性溶血性贫血及神经系统受累的三联症表现,40%病例除上述三联症表现外,还伴有发热及急性肾衰竭,呈五联征表现。如伴有血小板减少、异常破碎的红细胞增多及网织红细胞增高时,则TTP诊断即可成立。
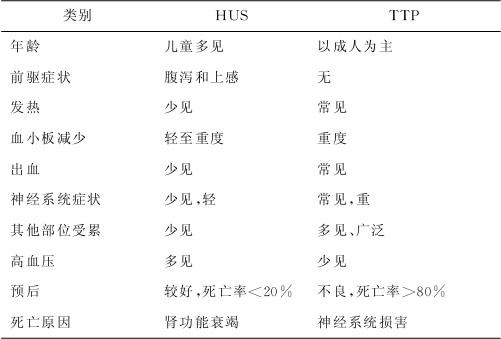
HUS及TTP的区别见表3—6。
表3—6 HUS及TTP的区别
九、鉴别诊断
1.弥漫性血管内凝血(DIC) TMA有时出现严重的出血倾向及血小板减少,纤维蛋白降解产物增多,易误诊为DIC,但应注意TMA时凝血酶原时间、部分凝血活酶时间、凝血因子水平正常,可与DIC鉴别。
2.Evan’s综合征 是一种自身免疫性疾病,体内产生抗红细胞和血小板抗体,表现为溶血、血小板减少,可与其他自身免疫性疾病同时并存,如干燥综合征、SLE、自身免疫性溶血性贫血、肝炎、甲状腺功能减退等,但其周围血涂片多见球形红细胞,一般无变形及破碎红细胞,人体球蛋白实验(Coombs’test)阳性。
3.系统性红斑狼疮(SLE) SLE时可有肾脏损害,精神症状,血小板减少和溶血性贫血,但多发于青年女性,外周血中无变形和破碎红细胞,免疫学检查多阳性。
4.流行性出血热(EHF) 常有发热,出血倾向,但一般无溶血表现,EHF抗体阳性。
5.溶血、肝酶升高及血小板减少综合征(HELLP综合征) 是严重先兆子痫的一种表现,在重症妊高征基本病理变化、全身小血管痉挛基础上并发血小板减少和微血管病性溶血,大部分发生在产前,随妊娠结束可缓解。