食品中铜的测定方法
出处:按学科分类—工业技术 中国轻工业出版社《食品添加剂分析检验手册》第221页(7056字)
一、葡萄糖酸铜
化学名:葡萄糖酸铜(Copper Gluconate)
结构式
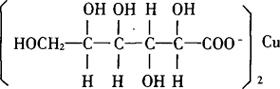
分子式:C12H22CuO4
相对分子质量:453.84
葡萄糖酸铜的鉴别
1.试剂和溶液
1.1 氢氧化铵。
1.2 10%亚铁氰化钾。
1.3 盐酸。
1.4 冰乙酸。
1.5 苯肼。
2.操作步骤
2.1 取本品水溶液,加入过量氢氧化铵试液,即产生蓝色沉淀后变为深蓝色溶液。
2.2 取本品水溶液,加10%亚铁氰化钾试液(新配),即产生棕红色沉淀,不溶于稀盐酸。
2.3 取5mL温热本品水溶液,加入0.7mL冰乙酸、1mL新蒸馏苯肼,在水浴中加热30min,冷却,用玻璃棒摩擦玻璃管内壁,即生成葡萄糖酸苯肼结晶。
二、硫酸铜
化学名:硫酸铜(Cupric Sulfate;Copper Sulfate)
结构式:CuSO4·5H2O
相对分子质量:249.69
(一)鉴别方法
本品5%溶液呈铜盐反应和硫酸盐反应。
1.试剂和溶液
1.1 亚铁氰化钾。
1.2 乙酸。
1.3 氨。
1.4 氯化钡。
1.5 盐酸。
1.6 硝酸。
1.7 醋酸铅。
1.8 醋酸铵。
1.9 氢氧化钠。
2.操作步骤
2.1 硫酸盐反应。
2.1.1 取供试品溶液,加氯化钡试液,即生成白色沉淀;分离,沉淀在盐酸或硝酸中均不溶解。
2.1.2 取供试品溶液,加醋酸铅试液,即生成白色沉淀;分离,沉淀在醋酸铵试液或氢氧化钠试液中溶解。
2.1.3 取供试品溶液,加盐酸,不生成白色沉淀(与硫代硫酸盐区别)。
2.2 铜盐反应 向本品溶液中添加新配亚铁氰化钾溶液(1+10)产生红棕色沉淀。向一部分沉淀中加稀乙酸(1+20),沉淀不溶。向另一部分沉淀中添加氨试液(40mL氯水制成100mL溶液),沉淀溶解,溶液的颜色变深蓝。
(二)食品中铜的测定方法
1.原子吸收分光光度法原理
样品处理后,导入原子吸收分光光度计中,原子化以后,吸收324.8nm共振线,其吸收量与铜量成正比,与标准系列比较定量。
2.试剂和溶液
要求使用去离子水,优级纯或高级纯试剂。
2.1 铜标准溶液 精密称取1.0000g金属铜(99.99%),分次加入6mol/LHNO3溶液溶解,总量不超过37mL,移入1000mL容量瓶中,用水稀释至刻度。此溶液每毫升相当于1mg铜。
2.2 铜标准使用液 吸取10.0mL铜标准溶液,置于100mL容量瓶中,加0.5%硝酸稀释至刻度。
2.3 硝酸。
2.4 6mol/L HNO3 量取38mL硝酸,加水稀释至100mL。
2.5 0.5%硝酸 量取lmL硝酸,加水稀释至200mL。
2.6 10%硝酸 量取l0.5mL硝酸,加水稀释至100mL。
2.7 过硫酸铵。
2.8 0.5%硫酸钠溶液。
2.9 石油醚。
3.仪器
原子吸收分光光度计。
4.操作方法
4.1 样品处理。
4.1.1 谷类:除去外壳,磨碎,过20目筛,混匀。称取1.0~5.0g样品,置于石英或瓷坩埚中,加5mL硝酸,放置0.5h,小火蒸干,继续加热炭化,移入高温炉中,500℃灰化1h,取出放冷,再加1mL硝酸浸湿灰分,小火蒸干。称取2g过硫酸铵,覆盖灰分,再移入高温炉中,800℃灰化20min,冷却后取出,以0.5%硫酸钠溶液少量多次洗入l0mL容量瓶中,并稀释至刻度,备用。
取与样品相同量的硝酸、过硫酸铵,按同法作试剂空白试验。
4.1.2 水产类:取可食部分捣成匀浆。称取1.0~5.0g,以下按4.1.1自“置于石英或瓷坩埚中……”起依法操作。
4.1.3 乳、炼乳、乳粉、茶、咖啡:称取2g混匀或磨碎样品,置于瓷坩埚中,加热炭化后,置高温炉中,420℃灰化3h,放冷后加水少许,稍加热,然后加1mLl∶1硝酸,加热溶解后,移入100mL容量瓶中,加水稀释至刻度,备用。
4.1.4 油脂类:称取2.0g混匀样品,固体油脂先加热融成液体,置于l00mL锥形瓶中,加10mL石油醚,用10%硝酸提取2次,每次5mL,振摇lmin,合并硝酸液于50mL容量瓶中,加水稀释至刻度,混匀,备用。
4.1.5 饮料、酒、醋等:吸取2.0mL样品,置于100mL容量瓶中,加0.5%硝酸至刻度,混匀,备用。
4.2 测定 吸取0,lmL,2mL,4mL,6mL,8mL铜标准使用液,分别置于100mL容量瓶中,加0.5%硝酸稀释至刻度,混匀。容量瓶中每毫升分别相当于0,10ng,20ng,40ng,60ng,80ng铜。
将处理后的样液、试剂空白和各容量瓶中铜标准液分别导入火焰进行测定。测定条件:灯电流6mA,波长324.8nm,狭缝0.19nm,空气流量9L/min,乙炔流量2L/min,灯头高度3mm,氘灯背景校正(也可根据仪器型号,调至最佳条件),以铜含量对应浓度吸光度,绘制标准曲线比较。
5.分析方法的表述

式中 x——样品中铜的含量,mg/kg
ρ1——测定用样品中铜的含量,ng/mL
ρ2——试剂空白液中铜的含量,ng/mL
V——样品处理后的总体积,mL
m——样品质量(体积),g(mL)
(三)二乙胺基二硫代甲酸钠法
1.原理
样品经消化后,在碱性溶液中铜离子与二乙胺基二硫代甲酸钠生成棕黄色络合物,溶于四氯化碳与标准系列比较定量。
2.试剂和溶液
2.1 柠檬酸铵、乙二胺四乙酸二钠溶液称取20g柠檬酸铵及5g乙二胺四乙酸二钠溶于水中,加水稀释至100mL。
2.2 2mol/L硫酸量取20mL硫酸,倒入300mL水中,冷后再加水稀释至360mL。
2.3 1∶1氨水。
2.4 酚红指示液 0.1%乙醇溶液。
2.5 铜试剂溶液 0.1%二乙氨基二硫代甲酸钠〔(C2H5)2NCS2Na·3H2O〕溶液,必要时可过滤,贮存于冰箱中。
2.6 四氯化碳。
2.7 铜标准溶液 同原子吸收分光光度法中的2.1。
2.8 铜标准使用液 吸取铜标准溶液10.0mL,置于100mL容量瓶中,加2mol/L(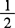 H2SO4)稀释至刻度。如再稀释一次,至每毫升相当于10μg铜。
H2SO4)稀释至刻度。如再稀释一次,至每毫升相当于10μg铜。
2.9 6mol/LHNO3 量取60mL硝酸,加水稀释至160mL。
3.仪器
分光光度计。
4.操作方法
4.1 样品消化。
4.1.1 硝酸-硫酸法。
4.1.1.1 粮食、粉丝、粉条、豆干制品、糕点、茶叶等及其他含水分少的固体食品:称取5.0g或10.0g的粉碎样品,置于250~500mL定氮瓶中,先加水少许使湿润,加数粒玻璃珠,10~15mL硝酸,放置片刻,小火缓缓加热,待作用缓和,放冷。沿瓶壁加入5mL或10mL硫酸,再加热,至瓶中液体开始变成棕色时,不断沿瓶壁滴加硝酸至有机质分解完全。加大火力,至产生白烟,溶液应澄明无色或微带黄色,放冷。在操作过程中应注意防止爆炸。
加20mL水煮沸,除去残余的硝酸至产生白烟为止,如此处理2次,放冷。将冷后的溶液移入50mL或100mL容量瓶中,用水洗涤定氮瓶,洗液并入容量瓶中,放冷,加水至刻度,混匀。定容后的溶液每10mL相当于1g样品,相当加入硫酸量1mL。
取与消化样品相同量的硝酸和硫酸,按同一方法作试剂空白试验。
4.1.1.2 蔬菜、水果:称取25.0g或50.0g洗净打成匀浆的样品。置于250~500mL定氮瓶中,加数粒玻璃珠,10~15mL硝酸,以下按4.1.1.1自“放置片刻……”起依法操作,但定容后的溶液每10mL相当于5g样品,相当加入硫酸量1mL。
4.1.1.3 酱、酱油、醋、冷饮、豆腐、腐乳、酱腌菜等:称取10.0g或20.0g样品(或吸取10.0mL或20.0mL液体样品),置于250~500mL定氮瓶中,加数粒玻璃珠,5~15mL硝酸。以下按4.1.1.1自“放置片刻……”起依法操作,但定容后的溶液每10mL相当于2g或2mL样品。
4.1.1.4 含酒精性饮料或含二氧化碳饮料:吸取10.0mL或20.0mL样品,置于250~500mL定氮瓶中,加数粒玻璃珠,先用小火加热除去乙醇或二氧化碳,再加5~10mL硝酸,混匀后,以下按4.1.1.1自“放置片刻……”起依法操作,但定容后的溶液每10mL相当于2mL样品。
吸取5~10mL水代替样品,加与消化样品相同量的硝酸和硫酸,按相同操作方法做试剂空白试验。
4.1.1.5 含糖量高的食品:称取5.0g或10.0g样品,置于250~500mL定氮瓶中,先加少许水使湿润,加数粒玻璃珠、5~10mL硝酸混合后,摇匀。缓缓加入5mL或10mL硫酸,待作用缓和停止起泡沫后,先用小火缓缓加热(糖分易炭化),不断沿瓶壁补加硝酸,待泡沫全部消失后,再加大火力,至有机质分解完全,发生白烟,溶液应澄明无色或微带黄色,放冷。以下按4.1.1.1自“加20mL水煮沸……”起依法操作。
4.1.1.6 水产品:取可食部分样品捣成匀浆,称取5.0g或10.0g(海产藻类、贝类可适当减少取样量),置于250~500mL定氮瓶中,加数粒玻璃珠、5~10mL硝酸,混匀后,以下按4.1.1.1自“沿瓶壁加入5或10mL硫酸……”起依法操作。
4.1.2 灰化法。
4.1.2.1 粮食及其他含水分少的食品:称取5.0g样品,置于坩埚中,加热至炭化,然后移入高温炉中,500℃灰化3h,放冷,取出坩埚,加1mL硝酸,润湿灰分,用小火蒸干,在500℃灼烧1h,放冷,取出坩埚。加1mL1∶1硝酸,加热,使灰分溶解,移入50mL容量瓶中,用水洗涤坩埚,洗液并入容量瓶中,加水至刻度,混匀备用。
4.1.2.2 含水分多的食品或液体样品:称取5.0g或吸取5.0mL样品,置于蒸发皿中,先在水浴上蒸干,以下再按4.1.2.1自“加热至炭化……”起依法操作。
4.2 测定 吸取10.0mL消化后的定容溶液和同量的试剂空白液,分别置于125mL分液漏斗中,加水稀释至20mL。
吸取0.00,0.50mL,1.00mL,1.50mL,2.00mL,2.50mL铜标准使用液(相当0、5μg、10μg、15μg、20μg、25μg铜),分别置于125mL分液漏斗中,各加2mol/L(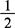 H2SO4)至20mL。
H2SO4)至20mL。
于样品消化液、试剂空白液和铜标准液中,各加5mL柠檬酸铵、乙二胺四乙酸二钠溶液和3滴酚红指示液,混匀,用1∶1氨水调至红色。各加2mL铜试剂溶液和10.0mL四氯化碳,剧烈振摇2min,静置分层后,四氯化碳层经脱脂棉滤入2cm比色杯中,以零管调节零点,于波长440nm处测吸光度,绘制标准曲线比较。
5.分析方法的表述

式中 x——样品中铜的含量,mg/kg或mg/L
m1——测定用样品消化液中铜的含量,μg
m2——试剂空白液中铜的含量,μg
m——样品质量(体积),g(mL)
V1——样品消化液的总体积,mL
V2——测定用样品消化液体积,mL