糖精钠
出处:按学科分类—工业技术 中国轻工业出版社《食品添加剂分析检验手册》第339页(9991字)
结构式:

分子式:C7H4O3NSNa·2H2O
相对分子质量:241.19
一、糖精钠的鉴别
1.试剂
1.1 间苯二酚。
1.2 硫酸。
1.3 氢氧化钠 40g/L溶液。
1.4 盐酸 100g/L溶液。
2.仪器
一般实验室仪器。
3.操作步骤
3.1 取试样约20mg,加间苯二酚约40mg,混合后加硫酸10滴,用微火加热,至显深绿色,放冷,加水10mL与过量的氢氧化钠溶液即成绿色有荧光的溶液。
3.2 取铂丝,用盐酸湿润后,蘸取试样,在无色火焰中燃烧,火焰即显鲜黄色。
3.3 熔点测定 按《中华人民共和国药典》1977年版熔点测定法规定。取试样约0.3g,加水5mL溶解后,加稀盐酸1mL,即析出结晶,过滤,滤渣用水洗净,经105℃干燥后,测定其熔点应为226~230℃。
二、糖精钠的含量测定
1.试剂和溶液
1.1 冰乙酸。
1.2 乙酸酐。
1.3 结晶紫指示液 0.5%乙酸溶液。
1.4 无水乙酸 取冰乙酸适量,按含水量计算1g水加乙酸酐5.22mL即得。
1.5 高氯酸 0.1mol/LHClO4标准溶液,按GB601配制。
2.仪器
一般实验室仪器和自动滴定管(25mL)。
3.测定方法
取干燥失重测定后试样0.3g,称准至0.0002g,加入乙酸酐5mL,溶解后,加2滴结晶紫指示液,用0.1mol/LHClO4溶液滴定至蓝绿色。
4.分析结果的表述
糖精钠质量分数(w),按式(11-1)计算:

式中 c——HClO4标准溶液浓度,mol/L
V——消耗高氯酸标准溶液的体积,mL
m——试样质量,g
0.2052——每毫摩糖精钠的质量,g/mmol
三、食品中糖精钠的测定方法
(一)高效液相色谱法
1.原理
样品加温除去二氧化碳和乙醇,调节pH至近中性,过滤后进高效液相色谱仪。经反相色谱分离后,根据保留时间和峰面积进行定性定量。取样量为2.5g时,进样量为10μL时,最低检出量为1.5ng。
2.试剂和溶液
2.1 甲醇 经滤膜(0.5μm)过滤。
2.2 氨水(1+1) 氨水加等体积水混合。
2.3 0.02mol/L乙酸铵溶液 称取1.54g乙酸铵,加水至1000mL溶解,经滤膜(0.45μm)过滤。
2.4 糖精钠标准贮备溶液 准确称取0.0851g经120℃烘干4h后的糖精钠(C7H4O3NSNa·2H20),加水溶解定容至100.0mL。糖精钠含量1.0mg/mL,作为储备溶液。
2.5 糖精钠标准使用溶液 吸取糖精钠标准贮备液10.0mL,放入100mL容量瓶中,加水至刻度。经滤膜(0.45μm)过滤。该溶液每毫升相当于0.10mg的糖精钠。
3.仪器
高效液相色谱仪,紫外检测器。
4.测定方法
4.1 样品处理。
4.1.1 汽水、饮料、果汁类:汽水需微温搅拌除去二氧化碳,然后吸取2.0mL样品加入已装有中性氧化铝(3cm×1.5cm)的小柱中,过滤,弃去初滤液。然后用移动相洗脱糖精钠,接收于25mL带塞量筒中,洗脱至刻度,摇匀。此液通过微孔滤膜后进样。
4.1.2 配制酒类:称取10.0g样品,放入小烧杯中,水浴加热除去乙醇,用氨水(1+1)调至pH7,加水定容至适当体积,经滤膜(0.45μm)过滤。
4.2 高效液相色谱参考条件:
4.2.1 色谱柱:YWG-C18 4.6mm×150mm,5μm,或其他型号C18柱。
4.2.2 流动相: 甲醇+乙酸铵溶液(0.02mol/L)(5+95)。
4.2.3 流速:1.0mL/min。
4.2.4进样量:10μL。
4.2.5 检测器:紫外检测器,波长230μm,灵敏度0.2AUFS。根据保留时间定性,外标峰面积法定量。
5.分析结果的表述
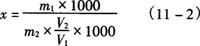
式中 x——样品中糖精钠的含量,g/kg(L)
m1——进样体积中糖精钠的质量,mg
V2——进样体积,mL
V1——样品稀释总体积,mL
m2——样品质量,g
6.其他
本方法可同时测定山梨酸、苯甲酸、糖精钠(见图11-1)。

图11-1 高效液相苯甲酸、山梨酸、糖精钠色谱图
1-苯甲酸 2-山梨酸 3-糖精钠
(二)薄层色谱法
1.原理
在酸性条件下,食品中的糖精钠用乙醚提取、浓缩、薄层色谱分离,显色后与标准比较,进行定性和半定量测定。
2.试剂和溶液
2.1 乙醚 不含过氧化物。
2.2 无水硫酸钠。
2.3 无水乙醇及乙醇(95%)。
2.4 聚酰胺粉 100~140目。
2.5 盐酸(1+1) 取100mL盐酸,加水稀释至200mL。
2.6 展开剂。
2.6.1 正丁醇+氨水+无水乙醇(20+1+1)。
2.6.2 异丙醇+氨水+无水乙醇(20+1+1)。
2.7 显色剂 称取0.040g溴甲酚紫溶于100mL50%乙醇溶液,用1.2mL0.4%氢氧化钠溶液调至pH8。
3.仪器
3.1 吹风机。
3.2 层析缸。
3.3 玻璃板5cm×20cm。
3.4 微量注射器10μL。
3.5 玻璃喷雾器。
4.测定方法
4.1 样品提取。
4.1.1 饮料、果酱:称取2.5g(mL)已经混匀的样品(汽水需加热去除二氧化碳),置于25mL带塞量筒中,加氯化钠至饱和(约1g),加0.5mL26mol/LHCl溶液酸化,用15mL、10mL乙醚提取2次,每次振摇1min,静止分层,用滴管将上层乙醚提取液通过无水硫酸钠滤入25mL容量瓶中,用少量乙醚洗无水硫酸钠,加乙醚至刻度,混匀。吸取10.0mL乙醚提取液分2次置于10mL带塞离心管中,在约40℃水浴上挥发至干,加入0.1mL无水乙醇溶解残渣,备用。
4.1.2 糕点:称取2.5g糕点样品,研碎,置于25mL带塞量筒中,用石油醚提取3次,每次20mL,每次振摇3min,弃去石油醚,让样品挥干后(在通风橱中不断搅拌样品,以除去石油醚),加入0.5mL6mol/LHCl溶液酸化,再加约1g氯化钠,以下按4.1.1自“用15mL、10mL乙醚提取2次……”起依法操作。
4.2 测定。
4.2.1 聚酰胺粉板的制备:称取4g聚酰胺粉,加1.0g可溶性淀粉,加约14mL水研磨均匀合适为止,立即倒入涂布器内制成面积为5cm×20cm,厚度为0.3mm的薄层板6块。室温干燥后,于80℃干燥1h,取出,置于干燥器中保存、备用。
4.2.2 点样:薄层板下端2cm的基线上,用微量注射器于板中间点4μL样品溶液,两侧各点2μL、3μL糖精钠标准液。
4.2.3 展开与显色:将点样后的薄层板放入预先盛有展开剂(2.6.1或2.6.2)的展开槽中,展开槽周围贴有滤纸,待溶剂前沿上展至10cm以上时,取出在空气中挥干,喷显色剂其斑点成黄色,背景成蓝色。样品中糖精钠的量与标准斑点深浅比较定量(用2.6.2展开剂时,糖精钠的比移值为0.31,环己基氨基磺酸为0.47,苯甲酸为0.61,山梨酸为0.73)。
5.分析结果的表述

式中 x——样品中糖精钠的含量,g/kg或g/L
m1——测定用样液中糖精钠的质量,mg
m2——样品质量(体积),g(mL)
V1——样品提取液残留物加入乙醇的体积,mL
V2——点样液体积,mL
(三)离子选择电极测定方法
1.原理
糖精钠选择电极是以季铵盐所制PVC薄膜为感应膜的电极,它和作为参比电极的饱和甘汞电极配合使用,以测定食品中糖精钠的含量。当测定温度、溶液总离子强度和溶液接界电位条件一致时,测得的电位遵守能斯特方程式,电位差随溶液中糖精离子的活度(或浓度)改变而变化。
被测溶液中糖精钠含量在0.02~1mg/mL范围内。电极值与糖精离子浓度的负对数成直线关系。
2.试剂和溶液
2.1 乙醚 使用前用盐酸(6mol/L)饱和。
2.2 无水硫酸钠。
2.3 6mol/L盐酸 取100mL盐酸,加水稀释至200mL,使用前以乙醚饱和。
2.4 0.06mol/L氢氧化钠溶液 取2.4g氢氧化钠加水溶解并稀释至1000mL。
2.5 100g/L硫酸铜溶液 称取硫酸铜(CuSO4·5H2O)10g溶于100mL水中。
2.6 40g/L氢氧化钠溶液。
2.7 0.02mol/LNaOH溶液 将2.4稀释而成。
2.8 1mol/LNaH2PO4·2H20溶液 取78g磷酸二氢钠(NaH2PO4·2H2O)溶解后转入500mL容量瓶中,加水稀释至刻度,摇匀。
2.9 总离子强度调节缓冲液 87.7mL磷酸二氢钠溶液(1mol/L)与12.3mL磷酸氢二钠溶液(1moL/L)混合即得。
2.10 糖精钠标准溶液 准确称取O.0851g经120℃干燥4h后的糖精钠结晶移入100mL容量瓶中,加水稀释至刻度,摇匀备用。此溶液每毫升相当于1.0mg糖精钠(C6H4CONNaSO2·2H2O)。
3.仪器
3.1 精密级酸度计或离子活度计或其他精密级电位计 准确到±1mV。
3.2 糖精选择电极。
3.3 217型甘汞电极 具双盐桥式甘汞电极,下面的盐桥内装入含有1%琼脂的氯化钾溶液(3mol/L)。
3.4 磁力搅拌器。
3.5 透析用玻璃纸。
3.6 半对数纸。
4.测定方法
4.1 样品提取。
4.1.1 液体样品 浓缩果汁、饮料、汽水、汽酒、配制酒等。准确吸取25mL均匀试样(汽水、汽酒等需先除去二氧化碳后取样),置于250mL分液漏斗中,加2mL6mol/LHCl溶液,用20mL,20mL,10mL乙醚提取3次。合并乙醚提取液,用5mL经盐酸酸化的水洗涤1次,弃去水层,乙醚层转移至50ml容量瓶,用少量乙醚洗涤原分液漏斗合并入容量瓶,并用乙醚定容至刻度,必要时加入少许无水硫酸钠,摇匀,脱水备用。
4.1.2 含蛋白质、脂肪、淀粉量高的食品:糕点、饼干、酱菜、豆制品、油炸食品,称取20.00g切碎样品,置透析用玻璃纸中,加50mL0.02mol/LNaOH溶液,调匀后将玻璃纸口扎紧,放入盛有200mL0.02mol/LNaOH溶液的烧杯中,盖上表面皿,透析24h,并不时搅动浸泡液。量取125mL透析液,加约0.4mL6mol/LHCl溶液使成中性,加20mL硫酸铜溶液混匀,再加4.4mL氢氧化钠溶液(40g/L),混匀。静置30min,过滤。取100mL滤液于250mL分液漏斗中,以下按4.1.1自“加2mL6mol/LHCl……”起依法操作。
4.1.3 蜜饯类:称取10.0g切碎均匀样品,置透析用玻璃纸中,加50mL0.06mol/LNaOH溶液,调匀后将玻璃纸扎紧,放入盛有200mL0.06mol/LNaOH溶液的烧杯中,透析,沉淀,提取按4.1.2操作。
4.1.4 糯米制食品:称取25.00g切成米粒状小块均匀样品,按4.1.2操作。
4.2 测定。
4.2.1 标准曲线的绘制:准确吸取0.0,0.5mL,1.0mL,2.5mL,5.0mL,10.0mL糖精钠标准溶液(相当于0.0,0.5mg,1.0mg,2.5mg,5.0mg,10.0mg糖精钠),分别置于50mL容量瓶中,各加5mL总离子强度调节缓冲液,加水至刻度,摇匀。
将糖精选择电极和甘汞电极分别与测量仪器的负端和正端相连接,将电极插入盛有水的烧杯中,按其仪器的使用说明书调节至使用状态,在搅拌下用水洗至起始电位(例如某些电极起始电位达-320mV)。取出电极用滤纸吸干。将上述标准系列溶液按低浓度到高浓度逐个测定,得其在搅拌时的平衡电位值(-mV)。
在半对数纸上以毫升(毫克)为纵坐标,电位值(-mV)为横坐标绘制标准曲线。
4.2.2 样品的测定:准确吸取20mL4.1下的乙醚提取液置于50mL烧杯中,挥发至干残渣,加5mL总离子强度调节缓冲液。小心转动,振摇烧杯使残渣溶解,将烧杯内容物定量转移入50mL容量瓶中,原烧杯用少量水多次漂洗后,并入容量瓶中,最后加水至刻度摇匀。依法测定其电位值(-mV),查标准曲线求得测定液中糖精钠毫克数。
5.分析结果的表述

式中 x——样品中糖精钠含量,g/kg或g/L
m1——测定液中糖精钠的质量,mg
m2——样品的质量或体积,g或mL
V1——乙醚提取液的体积,mL
V2——分取乙醚提取液的体积,mL
6.干扰
本法对苯甲酸钠的浓度在200~1000mg/kg时无干扰;山梨酸的浓度在50~500mg/kg,糖精钠的含量在100~150mg/kg范围内,约有3%~10%的正误差,水杨酸及对羟基苯甲酸酯对本法的测定有严重干扰。
(四)导数光谱分析法(参考方法)
1.原理
利用糖精钠的4阶导数,在波长232.2nm和224.8nm出现糖精钠的特征吸收峰而进行定量。
2.试剂和溶液
2.1 乙醚。
2.2 6moL/LHCl溶液 取100mL盐酸,加100mL水即得。
2.3 100g/L硫酸铜溶液 称取硫酸铜(CuSO4·5H2O)10g溶于100mL水中。
2.4 200g/L氢氧化钠溶液 称取氢氧化钠20g溶于100mL水中。
2.5 20g/L碳酸氢钠溶液 称取2g碳酸氢钠溶于100mL水中。
2.6 1.0g/L糖精标准溶液 称取0.1g糖精,加2%碳酸氢钠溶解至100mL。
2.7 无水硫酸钠 分析纯。
3.仪器
紫外分光光度计(附导数光谱)。
4.测定方法
4.1 样品处理。
4.1.1 液体样品:饮料、樱桃罐头汁、酱油、葡萄酒等,参照国家标准分析方法的提取方法取2.00mL(样品含CO2,加热除去;含乙醇,用NaOH调至碱性,在沸水浴上加热除去),置25mL比色管中,加0.40mL6mol/LHCl溶液,用6.0mL、4.0mL、4.0mL乙醚提取3次,合并乙醚,用1.0mL盐酸酸化的水洗涤1~3次,弃去水层,乙醚通过无水硫酸钠置100mL三角烧杯中,水浴挥干,加2%NaHCO310~50mL溶解残渣待用。
4.1.2 半固体、固体样品:半固体(如果茶)称取10.0g,固体样品经粉碎,称取5.0g,置50.0mL比色管中,加水至30.0mL,加10mL10%CuSO4·5H2O,用NaOH调至碱性,加水至50.0mL,混匀,静止30min,用滤纸过滤,取滤液5.0mL置25.0mL比色管中,加0.40mL6mol/LHCl溶液,加乙醚10.0mL,10.0mL,5.0mL提取3次,合并乙醚提取液,用2.0mL盐酸酸化的水洗涤1~3次,弃去水层,乙醚通过无水Na2SO4脱去杂质,置100mL三角瓶中水浴挥干,用2%NaHCO3定容至10~50mL,待用。
4.1.3 标准曲线的制备及样品测定:用2%NaHCO3溶液配制0.000,0.005g/L,0.010g/L,0.020g/L,0.030g/L,0.040g/L糖精钠标准液。按仪器测定条件记录标液和样品的4阶导数光谱,以波长232.2nm附近的吸收强度定量。
5.分析结果的表述

式中 x——样品中糖精钠含量,g/kg或g/L
m1——样品测定液中糖精钠的含量,g/L
V1——样品定容体积
m2——样品体积(mL)或质量,g