亚硫酸盐溶液的成分和性质
出处:按学科分类—工业技术 中国轻工业出版社《制浆造纸工业计算手册上册》第102页(4650字)
1.SO2的溶解度
(1)SO2在水中的溶解度
①计算法
【说明】SO2属于中等不溶解性气体,在水中的溶解度可用下式计算。
【公式】
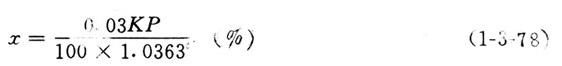
式中 x——SO2在水中的含量(%)
K——SO2在气体中的含量(体积%)
P——总压力(mmHg)
t——温度(℃)
1.0363′——系数,见表1-3-21
表1-3-21 系数1.0363t值
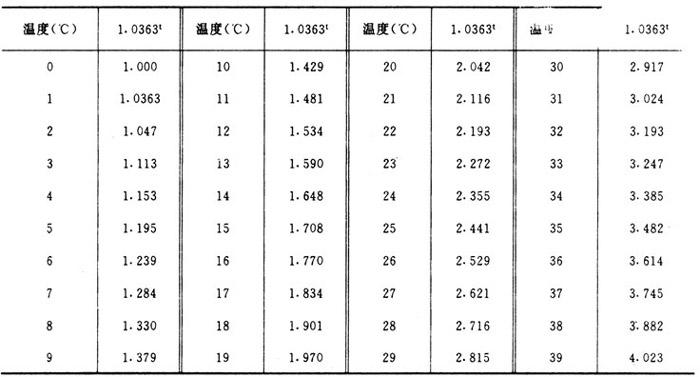
②查图法
【说明】见图1-3-11。
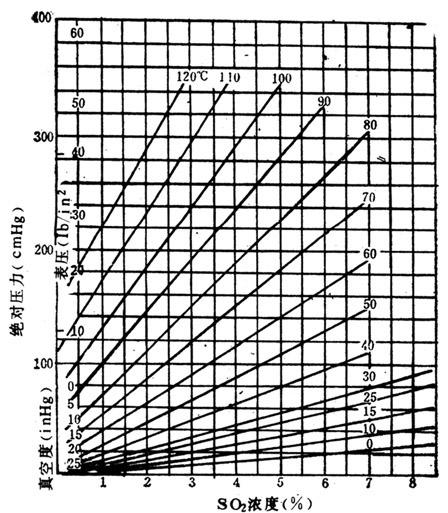
图1-3-11 SO2在水中的溶解度
③列线图法
【说明】见图1-3-12;图中SO2分压见图1-3-13和表1-3-22。
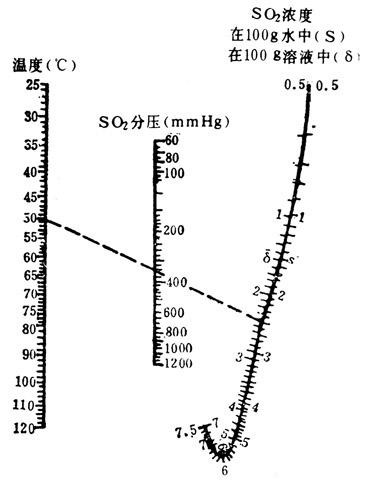
图1-3-12 SO2在水中的浓度列线图
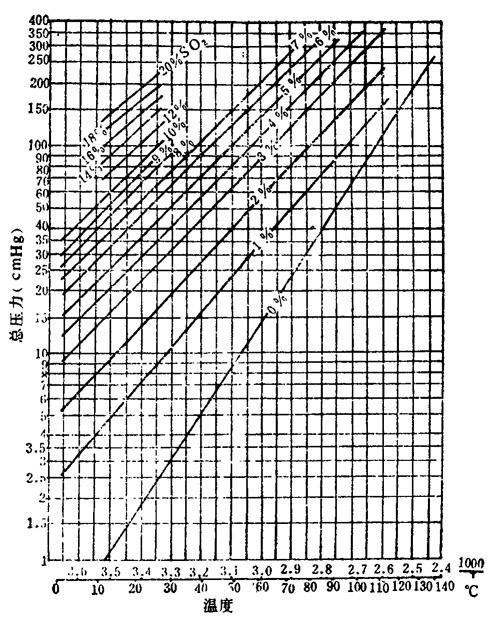
图1-3-13 SO2水溶液的蒸汽压
表1-3-22 在不同温度下SO2和水的蒸汽压
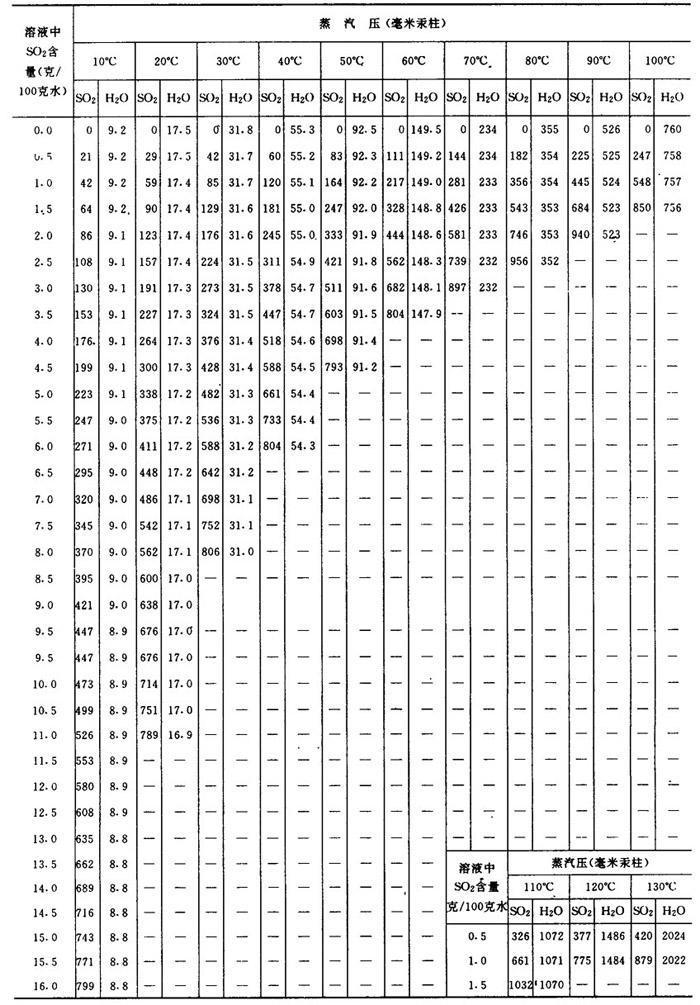
④查表法
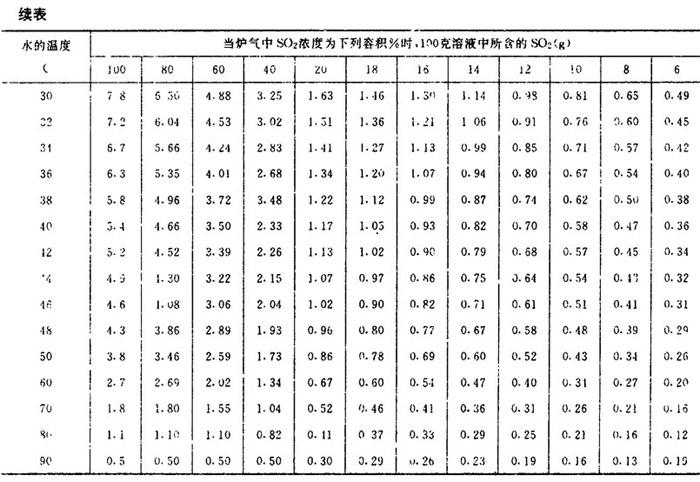
【说明】在大气压力下SO2在水中的溶解度见表1-3-23。
表1-3-23 大气压力下SO2在水中的溶解度
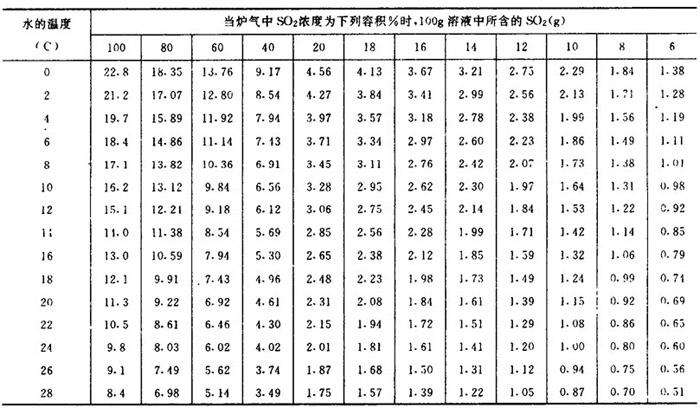
(2)SO2在Ca(HSO3)2溶液中的溶解度
【说明】当溶液中存在亚硫酸氢盐时,[HSO3]浓度增加,SO2的溶解度降低。
【公式】
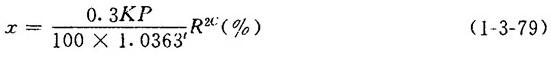
式中 x——SO2在Ca(HSO3)2溶液中的溶解度(%)
K——在气体中SO2的体积(%)
P——总压力(mmHg)
R——常数,取0.89
C——化合酸含量(C·A)(%)
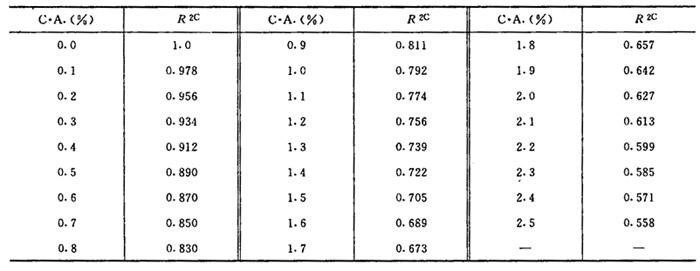
R2C——其值见表1-3-24
表1-3-24 系数R值
2.H2SO3+Ca(HSO3)2溶液的性质计算
(1)H2SO3的离解常数
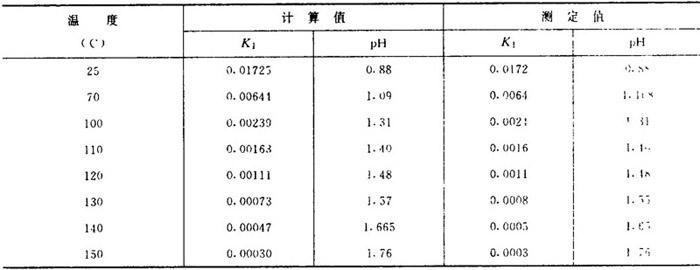
【说明】亚硫酸盐的离解平衡常数随温度的提高而降低。H2SO3第一级解离平衡常数见表1-3-25。
表1-3-25 亚硫酸溶液的K1、pH值和温度的关系
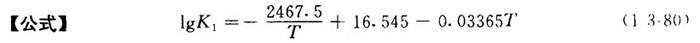
式中 K1——H2SO3第一级解离平衡常数
T——绝对温度(°K)
(2)溶液的酸度
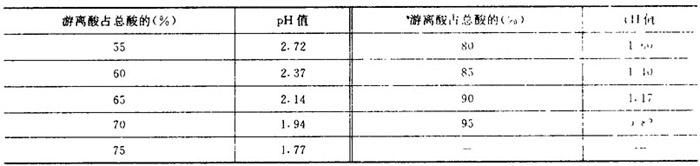
【说明】原酸的pH值取决于游离酸在总酸中所占的百分数。蒸煮酸中由于含有一部分有机酸,因此其pH值较组成相同的原酸为低。0C时原酸的pH值见表1-3-25。
表1-3-26 0℃时原酸的pH值
(3)溶液的相对密度
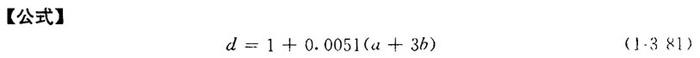
式中 d——15℃时酸液的相对密度
a——酸液中总酸浓度(%)
b——酸液中CaO含量(%)
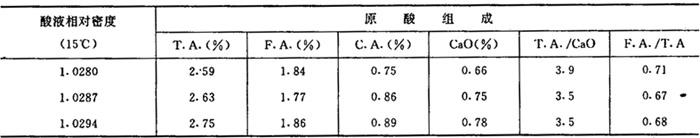
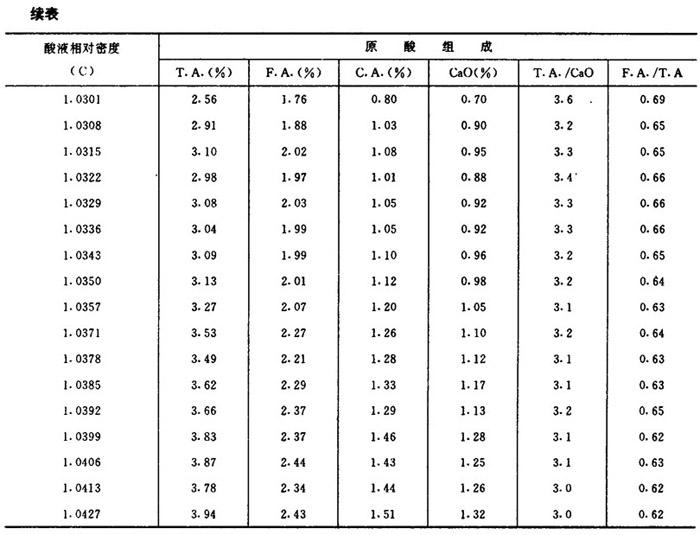
【附表】原酸的相对密度与酸液组成的关系见表1-3-27。
表1-3-27 原酸的相对密度与酸液组成的关系
3.Mg(HSO3)2+MgSO3溶液的性质
(1)溶液的相对密度d
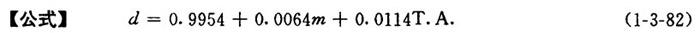
式中 d——15.5℃时酸液的相对密度
T.A.——总酸含量(%)
m——亚硫酸盐含量(过剩亚硫酸)以SO2计(%)
【注意】上式适用范围:T.A.=1.8~8.0%;m=0~1.2%。
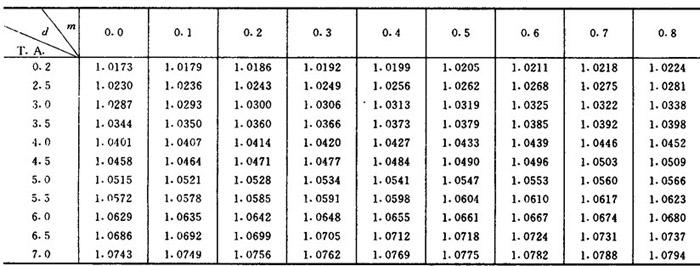
【附表】亚硫酸氢镁溶液的相对密度见表1-3-28。
表1-3-28 亚硫酸氢镁溶液的相对密度
(2)溶液的粘度μ
【公式】
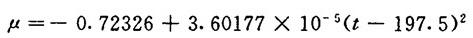
+9.73065×10-4×(T.A.t×33.122)2-3.13162
×10-4(T.A.t)+0.03006m+0.0018S(cP)(1-3-83)
式中 S——硫酸盐中的硫对总酸的重量(%)
t——华氏温度
【附图】 亚硫酸氢镁溶液的粘度见图1-3-14。
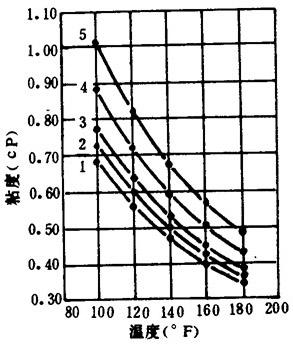
图1-3-14 亚硫酸氢镁溶液的粘度
1-水 2-T.A.1.37% 3-T.A.2.65% 4-T.A.5.22% 5-T.A.7.74%
(3)溶液的酸度
【说明】亚硫酸氢镁溶液的组成和pH(25℃)值的关系如图1-3-15;不同组成的酸液pH值随温度的变化见图1-3-16。
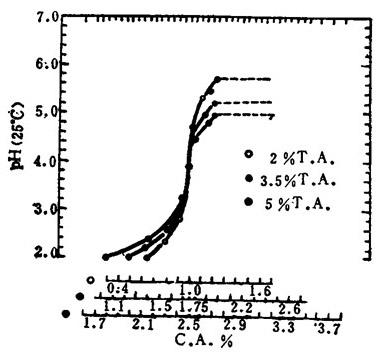
图1-3-15 亚硫酸氢镁溶液的pH值
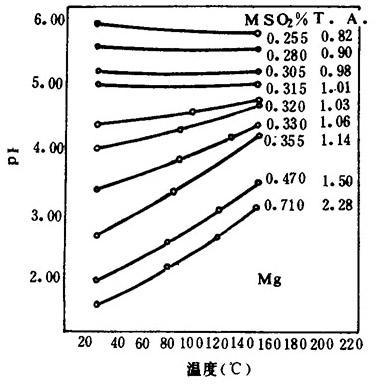
图1-3-16亚硫酸氢镁溶液的pH值与温度的关系
[0.315NMg(1.01%C.A.)]
(4)SO2分压P
【公式】
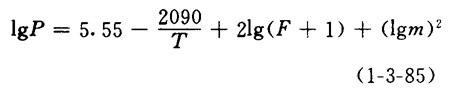
或
1gP=4.65+21gF+2.74(1gm)2
(1-3-86)
式中 P——SO2的分压(mmHg)
F——游离酸含量F.A.(%)
M——MgSO3含量(以SO2表示)(%)
T——酸液温度(°K)
【附图】50C时亚硫酸氢镁溶液的SO2等压线见图1-3-17。
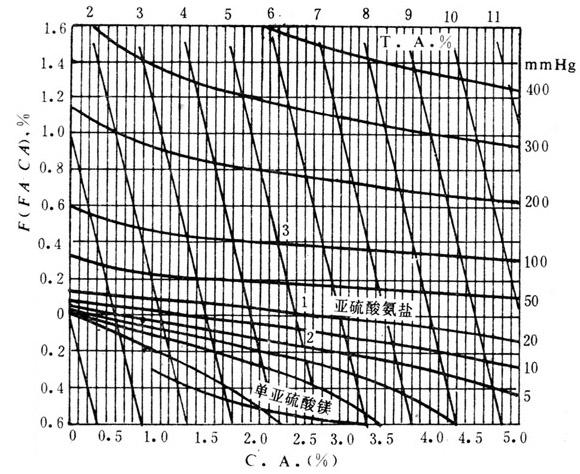
图1-3-17镁盐基亚硫酸溶液SO2等压线
(1mmHg=133.3Pa)
【图解示例】在亚硫酸氢镁线上方F.A.>C.A;下方C.A.>F.A.,即溶液中有过剩MgSO3。横坐标表示C.A.,斜主线表示T.A.,曲线为SO2等压线。
例1.查5%T.A.,2.5%C.A.的Mg(HSO3)2溶液的SO2分压。
解:从图1-3-17中查5%T.A.,2.5%C.A.与Mg(HSO3)2线三线的交点1,沿曲线查出SO2分压为20mmHg(相当于与SO2炉气浓度2.64%相平衡)。
例2.查5%T.A.,m为0.2%时溶液SO2分压。
解:从图1-3-17上查5%T.A.,斜线与0.2%(C.A.=F.A.)线相交于点2,沿等压线查出SO2分压为4mmHg。
例3.查5%T.A.,F为0.4%时的溶液SO2分压。
解:从图上查5%T.A.,斜线与0.4%(F.A.——C.A.)线相交于点3,沿等压线查出SO2分压为100mmHg。
(5)MgSO3的溶解度
【说明】含有三个结晶水的亚硫酸镁(MgSO3·3H2O)和含有6个结晶水的亚硫酸镁(MgSO3·6H2O)在水中的溶解度分别见表1-3-29和表1-3-30;在不同温度和总酸浓度下MgSO3的溶解度见图1-3-18。
表1-3-29MgSO3·3H2O在水中的溶解度
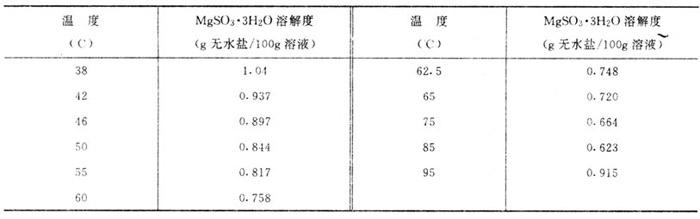
表1-3-30MgSO3·6H2O在水中的溶解度

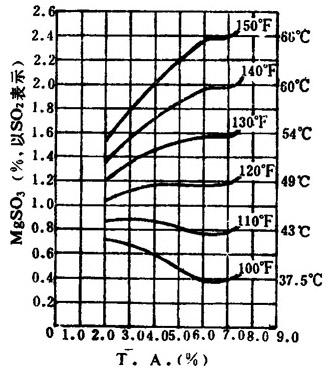
图1-3-18 不同温度和总酸浓度时MgSO3的溶解度
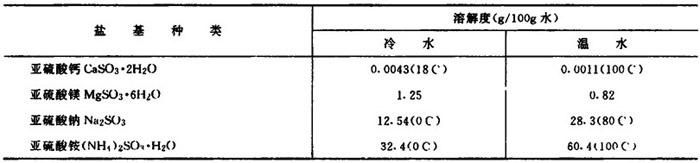
4.不同盐基的亚硫酸盐溶液的溶解度见表1-3-31
表1-3-31 不同盐基的亚硫酸盐溶解度