反应物量的增多对气体反应物转化率的影响
出处:按学科分类—文体、科学、教育 商务印书馆国际有限公司《高中数理化公式定理大全》第396页(1235字)
1.等温等容条件下:
(1)对于反应物为一种的反应,①对于气体系数减小的反应,如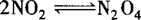 ,在原平衡的基础上,再加入NO2,会使平衡向右移动,但由于NO2增多,引起压强增大,导致平衡向右移动的趋势增大,转化率增大;②对于气体系数不变的反应,如2HBr
,在原平衡的基础上,再加入NO2,会使平衡向右移动,但由于NO2增多,引起压强增大,导致平衡向右移动的趋势增大,转化率增大;②对于气体系数不变的反应,如2HBr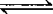 Br2+H2,在原平衡的基础上,再加入HBr,会使平衡向右移动,由于HBr的增多,引起压强增大,压强的改变对该平衡没有影响,转化率不变;③对于气体系数增大的反应,如PCl5
Br2+H2,在原平衡的基础上,再加入HBr,会使平衡向右移动,由于HBr的增多,引起压强增大,压强的改变对该平衡没有影响,转化率不变;③对于气体系数增大的反应,如PCl5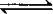 PCl3+Cl2,在原平衡的基础上,再加入PCl5气体,会使平衡向右移动,由于PCl5气体的增多,引起压强增大,抑制平衡向右移动,转化率减小.
PCl3+Cl2,在原平衡的基础上,再加入PCl5气体,会使平衡向右移动,由于PCl5气体的增多,引起压强增大,抑制平衡向右移动,转化率减小.
(2)对于反应物为两种或两种以上的气体可逆反应,如aA+bB=cC+dD,①如果只增加一种反应气体,则使另一种反应物的转化率增大,而其本身的转化率减小;②如果所有气体反应物都同等倍数增加,其转化率的变化情况与前后系数有关,其变化情况如下所述.例如:
对反应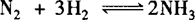 ,分别以1molN2和1molH2为起始量与以2molN2、2molH2为起始量,其转化率增大.
,分别以1molN2和1molH2为起始量与以2molN2、2molH2为起始量,其转化率增大.
对反应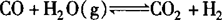 ,分别以1molCO和1molH2O(g)为起始量与以2molCO和2molH2O为起始量,其转化率不变.
,分别以1molCO和1molH2O(g)为起始量与以2molCO和2molH2O为起始量,其转化率不变.
同样,对反应系数增大的气体反应,分别以上述两种起始量反应,其转化率减小.
2.等温等压条件下,对于气体反应,对于同等倍数增加反应物量时,上述情况下平衡不移动,所以转化率不发生改变.
例 在一定温度下,一定体积的密闭容器中有如下平衡: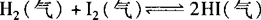
已知H2和I2的起始浓度均为0.10mol·L—1时,达平衡时HI的浓度为016mol·L—1.若H2和I2的起始浓度均变为0.20mol·L—1,则平衡时H2的浓度(mol·L—1)是( ).
A.0.16 B,0,08
C.0.04 D.0.02
解析 在恒温恒容条件下,对于反应前后气体分子数不变的可逆反应,只要反应物(或生成物)的物质的量的比例与原平衡相同,则两平衡等效.根据题给条件,若H2和I2的起始浓度均变为0.20mol·L—1,则平衡时HI的浓度为0.32mol·L—1,H2的浓度为0.20mol·L—1—0.16mol·L—1=0.04mol·L—1.
答 C.