水的电离
书籍:高中数理化公式定理大全
出处:按学科分类—文体、科学、教育 商务印书馆国际有限公司《高中数理化公式定理大全》第399页(604字)
1.水的电离方程式:水是一种极弱的电解质,
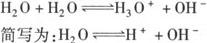
2.水的离子积:
在一定温度时,水电离产生的c(H+)与c(OH—)的乘积是一个常数,表示为:Kω=c(H+)·c(OH—).
在25℃时:
c(H+)=c(OH—)=1×10—7mol/L;
∴Kω=c(H+)·(OH—)=1×10—7×1×10—7=1×10—14.
注 ①Kω只与温度有关,与溶液的酸、碱性无关.
②温度升高,Kω也随着增大因水的电离过程是吸热过程,升高温度,促进水的电离,使c(H+)、c(OH—)同时增大,所以Kω也随着增大,但c(H+)与c(OH—)仍然相等,故水仍显中性.
③Kω不仅适用于纯水,也适用于任何酸、碱、盐的稀溶液,在25℃时,Kω都等于1×10—14.
④水的电离平衡遵循勒沙特列原理.