根据化学式的计算
出处:按学科分类—文体、科学、教育 商务印书馆国际有限公司《初中数理化公式定理大全》第347页(3231字)
根据化学式的计算主要根据下面五方面知识.

3.元素质量=一个原子质量×原子数
4.物质质量=一个分子质量×分子数
5.根据化学式的三个基本计算:计算相对分子质量、计算物质组成元素的质量比、计算物质中某元素的质量分数.
例1 已知在氮的某种氧化物中,氮元素与氧元素的质量比为7∶20.此氧化物的化学式为__.
【分析】 设此氧化物的化学式为NxOy,则有14x∶16y=7∶20
x∶y=2∶5,化学式为N2O5.
例2 两个集气瓶中各盛有纯净的二氧化硫和三氧化硫气体,若这两瓶气体的质量比为4∶1,则这两瓶气体中氧元素的质量比是__.
【分析1】 此题目传统的解法是:根据题意设这两瓶气体中二氧化硫为4克和三氧化硫为1克,所以这道题可以按计算4克二氧化硫中的氧元素与1克三氧化硫的氧元素的质量比来计算.
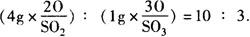
【分析2】 我们可以设两瓶气体中的分子个数比为x∶y,则它们的质量比为xSO2∶ySO3=4∶1,解此比例可得两种分子的个数比,根据不同物质中若含同一种元素,则此元素的质量比等于物质中该元素的原子个数的比.则这两瓶气体分子中所含氧原子的个数比也就是两瓶气体中的氧元素的质量比为x∶y.
设:二氧化硫与三氧化硫的分子个数比为x∶y.
则:xSO2∶ySO3=4∶1,
即64x∶80y=4∶1.
x∶y=5∶1.
即两瓶气体中的分子个数比为5∶1,两瓶气体中的氧原子个数比为10∶3,两瓶气体中的氧元素的质量比为10∶3.
例3 二氧化硫与三氧化硫两种气体中的氧元素质量相同时,硫元素的质量比为____.
【分析1】 根据题意设两瓶气体中的氧元素质量均为lg,先计算出含lg氧元素的二氧化硫和含lg氧元素的三氧化硫质量比,再求这已知质量比的两种气体中的硫元素的质量比.
求:含lg氧元素的二氧化硫与三氧化硫的质量比:

求:二氧化硫与三氧化硫的质量比为6∶5时,硫元素的质量比:
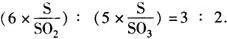
【分析2】 从两种气体中氧元素的质量相等可知这两种气体分子中的氧原子的个数相等.求出氧元素相等时的二氧化硫与三氧化硫的分子个数比后,即可根据此时的硫原子个数比求得硫元素的质量比.
求:氧元素质量相同,即氧原子个数相同时的两种气体分子个数比:
3SO2-6O-2SO3
此时硫原子的个数比为3∶2,即为这两种气体中氧元素质量相同时硫元素的质量比.
此解题方法称为关系式法.
例4 由Na2S、Na2SO3、Na2SO4组成的混合物中测得含氧元素为22%,则其中含硫元素约为( ).
A.32% B.46%
C.78% D.无法确定
【分析】 该混合物可视作由“Na2S”与“O”组成的“一种物质”.因其中O%=22%
所以Na2S%=1-22%=78%那么在不纯的组合Na2S中,S%即可求解.
Na2S——S
78 32
78% x
∴x=32%.
答案 A.
例5 已知碳酸钙和另一物质组成的混合物含碳量大于12%,则另一物质可能是( ).
A.Na2CO3 B.KHCO3
C.MgCO3 D.K2CO3
【分析】 此题乍看起来无从下手,其实就是质量分数的计算与比较.
CaCO3中碳的质量分数

题目要求混合物中碳的含量大于12%,已有CaCO3含碳量为12%,则另一种物质的含碳量必大于12%.由化学式可知,下面四种物质的一个“分子”中都只含有一个碳原子,即碳原子质量相同都为12,分母小的分数值大,分母是化合物相对分子质量,四种物质中都有CO3,可省略不计,只比较剩余部分,Ca的相对原子质量为40,比40小的含碳量高.
A.2Na~46 B.KH~40
C.Mg~24 D.2K~78
答案 C.
例6 CO和CO2的分子个数比为2∶3,求氧元素质量比__,CO和CO2的质量比__.
【分析】 本题以分子个数为纽带,元素质量比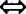 原子个数比
原子个数比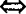 分子个数比
分子个数比
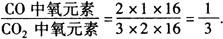
其实,不同种物质间同种元素的质量比就是两物质中该元素原子个数比,因为相对原子质量相同.
分子个数比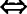 物质质量比.
物质质量比.
小结 解题的几条主线:
(1)元素质量比=相对原子质量之比×原子个数之比.
物质质量比=分子质量之比×分子个数比.
(2)元素质量比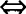 原子个数比
原子个数比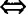 分子个数比
分子个数比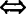 物质质量比.
物质质量比.
两种物质关于一种元素或同种原子有关系,最好用关系式法解题.
(3)求谁设谁,求化合价,先求化学式.求化学式,设通式为AxBy