生石灰
出处:按学科分类—工业技术 中国轻工业出版社《常用非木材纤维碱法制浆实用手册》第648页(724字)
石灰是由石灰石煅烧后失去二氧化碳而成的。未经消化的称为生石灰,主要成分为CaO,它与水发生作用,生成消石灰(熟石灰),主要成分为Ca(OH)2。
有效氧化钙含量的测定(蔗糖法)方法如下。
原量:石灰中的有效钙是游离的氧化钙。它之所以不同于总钙量,是由于有效钙不包括碳酸钙、硅酸钙以及其它钙盐中的钙。
此法基于氧化钙在水中溶解度不大,加入蔗糖与氧化钙结合成溶解度较大的蔗糖钙(C12H22O11、CaO、2H2O)。碳酸钙及其它钙盐和蔗糖不起作用,故可利用它的不同反应条件,以盐酸滴定。
C12H22O11·CaO·2H2O+2HCl=C12H22O11+CaCl2+3H2O
测定方法:精确称取试样0.4~0.5g于250ml锥形瓶中,加入蔗糖4g,玻璃球15~20粒和新煮沸而冷却的蒸馏水50ml,用力均匀摇动15min,加入2滴1.0%酚酞指示剂,用0.5mol/L盐酸标准溶液滴定至粉红色显着消失,30s内不重新显红为止。
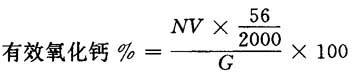
式中:N——盐酸标准溶液浓度(mol/L);
V——耗用盐酸标准溶液数(L);
G——试样重(g);
56——1mol氧化钙的克数。
上一篇:漂白粉
下一篇:常用非木材纤维碱法制浆实用手册目录