食品中琥珀酸及其盐类的测定方法
出处:按学科分类—工业技术 中国轻工业出版社《食品添加剂分析检验手册》第18页(4751字)
化学名:丁二酸(Succinic Acid)
结构式:

分子式:C4H6O4
相对分子质量:118.09
琥珀酸盐类
化学名:琥珀酸钠(Monosodium Succinate)
结构式:
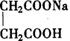
分子式:C4H5NaO4
相对分子质量:140.07
化学名:琥珀酸二钠(结晶)(Disodium Succinate)
结构式:

分子式:C4H4Na2O4·6H2O
相对分子质量:270.15
化学名:琥珀酸二钠(无水)(Disodium Succinate,Anhydrous)
结构式:

分子式:C4H4Na2O4
相对分子质量:162.06
食品中琥珀酸及其盐类,用气相色谱法测定琥珀酸的三甲基硅烷体,或用琥珀酸硫代激酶、丙酮酸激酶及乳酸脱氢酶的酶化学法,进行定量。如需计算出各种盐类,必须乘以相对分子质量比。
由于食品中存在天然的琥珀酸,所以测定值应为食品中天然的和添加的琥珀酸总量。
(一)气相色谱法
同本章第二节“三、食品中柠檬酸及其盐类的测定方法(一)”。但测定条件中,柱温改为120℃。计算按式(1-11)进行:

式中 ρ——样品溶液中1mL相当于琥珀酸微克数,μg/mL
m——取样量,g
琥珀酸钠含量(g/kg)=琥珀酸含量(g/kg)×1.186
琥珀酸二钠(结晶)含量(g/kg)=琥珀酸含量(g/kg)×2.288
琥珀酸二钠(无水)含量(g/kg)=琥珀酸含量(g/kg)×1.372
(二)比色法
1.原理
用琥珀酸硫代激酶、丙酮酸激酶及乳酸脱氢酶的酶法测定琥珀酸,其反应式如下:

由于氧化而使NADH的减少量与琥珀酸量相当,故可用来进行琥珀酸定量。按需要分别乘以相对分子质量比,即可标出各种盐类的量。
由于食品中存在天然的琥珀酸,所以测定值应为食品中天然和添加的琥珀酸总量。
2.试剂和溶液
2.1 肌苷-5′-三磷酸钠(ITP-Na3) 分析纯。
2.2 甘氨酰替甘氨酸 特级。
2.3 甘氨酰替甘氨酸缓冲溶液 将2.4g甘氨酰替甘氨酸及600mg硫酸镁(含7个水分子),溶于约50mL重蒸馏水中,用2mol/LNaOH溶液约5mL调节pH至8.4,再加重蒸馏水至60mL,此液保存于4℃,可稳定4周。
2.4 β-辅酶Ⅰ,还原型(NADH-Na2) 分析纯。
2.5 辅酶A(CoA-Li3) 分析纯。
2.6 磷酰烯醇丙酮酸氯化铵盐[PEP-(CHA)] 分析纯。
2.7 CoA/ITP/PEP混合液(辅酶A/肌苷-5′-三磷酸钠/磷酰烯醇丙酮酸氯化铵混合液) CoA60mg,ITP-Na360mg及PEP-(CHA)360mg溶解于6mL重蒸馏水中。本液保存于4℃,可稳定2周。
2.8 辅酶Ⅰ溶液 取45mg辅酶Ⅰ(NADH-Na2)及80mg碳酸氢钠溶于6mL重蒸馏水中,此液保存于4℃,可稳定4周。
2.9 丙酮酸激酶/乳酸脱氢酶(PK/LDH)混合液 用市售品丙酮酸激酶3mg/mL、乳酸脱氢酶1mg/mL[1]配制混合液。本品保存于4℃,可稳定1年。
2.10 琥珀酸激酶液(SCS液) 用分析纯琥珀酸激酶琥珀酸辅酶A盐合成酶(SCS5mg/mL)[2]。本品保存于4℃,可稳定1年。
3.仪器
分光光度计。
4.测定方法
4.1 样品溶液的制备。
4.1.1 液状食品[3]:准确称取10g以内样品,一般含琥珀酸2~40mg。将澄明无色或淡色样品加水至100mL,即为样品溶液。混浊样品,加约50~60mL水,过滤,用20~30mL水分数次洗容器及残渣,合并滤液和洗液,加水至100mL,即为样品溶液。深色样品,加约1/10样品量的聚酰胺或聚乙烯吡咯烷酮,必要时加20~30mL水,剧烈搅拌混匀,过滤,用40~50mL水分数次洗容器及残渣,合并滤液及洗液,加水至100mL,即为样品溶液。
4.1.2 固体食品:准确称取10g以内样品,一般含琥珀酸2~40mg。对于不含脂肪、蛋白质的样品(果子类),将样品置于匀浆器中,加50~60mL水,于60℃加热,匀浆5min,过滤,用20~30mL水分数次洗容器及残渣,合并滤液及洗液,加水至100mL,即为样品溶液。对于含脂肪、蛋白质样品[4],加30~40mL水并加热至60℃,匀浆5min,于60℃加温15min,冷后,于冰箱中放置20min,过滤,用20~30mL水分数次洗容器及残渣,合并滤液及洗液,加10mL0.4mol/LHClO4溶液,细心搅拌混匀,用2mol/LNaOH溶液中和,加水至100mL,冰箱中放20min,必要时过滤,即为样品溶液。
4.2 标准液的制备 准确称取1g琥珀酸,加水溶解至250mL。再取50mL此液,用1ml/LNaOH溶液调pH至8,加水至100mL,作为标准液(1mL相当2mg琥珀酸)。各取标准液1mL、5mL、10mL、15mL、20mL,分别加水至100mL,即标准曲线用标准液(此液分别含琥珀酸20μg/mL、100μg/mL、200μg/mL、300μg/mL、400μg/mL)。
4.3 测定方法。
4.3.1 测定条件:用紫外分光光度计,于波长340nm处测定吸光度。
4.3.2 测定:在2支试管中,分别标明A、B,按顺序各加入1mL甘氨酰替甘氨酸缓冲溶液、0.1mL辅酶Ⅰ溶液、0.1mL辅酶A/肌苷-5′-三磷酸钠/磷酰烯醇丙酮酸氯化铵混合液(CoA/ITP/PEP混合液),充分混合后,于A管中加入0.1mL样品溶液、1.4mL水,B管中加入1.5mL水,再于A、B管中各加入0.05mL丙酮酸激酶/乳酸脱氢酶混合液(PK/LDH混合液),搅拌混匀,于37℃保温5min,A管为样品管,B为空白管。
以水作参比,于波长340nm处,用1cm比色杯,分别测A、B管的吸光度EA和EB。再于A、B管中各加入0.02mL琥珀酸激酶液(SCS液),搅拌混匀,20min后,同样测其吸光度E′A及EB。
计算出EA与E′A之差△EA,EB与E′B之差△EB,再求出△EA与△EB之差△ET。
4.3.3 标准曲线:取标准曲线用标准液S1、S2……S5各0.1mL代替样品溶液,按4.3.2步骤进行测定,计算出△Es1、△Es2……△Es5,绘制标准曲线。
5.分析结果的表述
从标准曲线图中,查得样品溶液含琥珀酸的对应值(μg/mL),按式(1-12)计算出样品中琥珀酸含量(g/kg)。
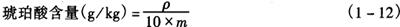
式中 ρ——样品溶液相当于标准液浓度,μg/mL
m——取样质量,g
琥珀酸钠含量(g/kg)=琥珀酸含量(g/kg)×1.186
琥珀酸二钠(结晶)含量=琥珀酸含量(g/kg)×2.288
琥珀酸二钠(无水)含量=琥珀酸含量(g/kg)×1.372
注:[1]将从兔肉中取出的结晶化酶混悬于硫酸铵溶液(3.2mol/L)中。
[2]从猪心脏提取,混悬于硫酸铵溶液(3.2mol/L)中,效价10U/mg。
[3]酱油、果汁等色深的样品,应脱色。酸性样品应调pH至8.0。澄明无色酒、果酒等不必除酒精。如为酸性应中和。葡萄酒要稀释,不脱色即可分析。
[4]豆酱、奶粉、火腿、腊肠、鱼肉制品、鱼、贝类、海带等加酱油调料煮熟的食品、干酪等。
(三)高压液相色谱法
同本章第二节“三、食品中柠檬酸及其盐类的测定方法(三)”。