维生素A的测定方法
出处:按学科分类—工业技术 中国轻工业出版社《食品添加剂分析检验手册》第230页(6569字)
化学名:反式-3,7-二甲基-9-(2,6,6-三甲基-1-环己烯基-1)-2,4,6,8-壬四稀乙酸酯〔trans-3,7-dimethyl-9-(2,6,6-trimethyl-1-cyclohexen-l-yl)-2,4,6,8-nonatetzaene-1-acetate〕
别名:视黄醇
结构式:

分子式:C22H32O2
相对分子质量:328.49
一、维生素A的鉴别
1.试剂和溶液
1.1 三氯甲烷;异丙醇。
1.2 三氯化锑溶液 取三氯化锑适量,制成250g/L的三氯甲烷溶液。
2.操作步骤
2.1 取本品的三氯甲烷溶液(1mL含维生素3μg)1mL,加三氯化锑饱和溶液5mL,溶液呈蓝该颜色随即消失。
2.2 维生素A异丙醇溶液在波长324~328nm内有最大吸收峰。
二、维生素A含量测定
1.试剂和溶液
环己烷。
2.仪器
紫外分光光度计。
3.测定方法
取本品适量,精密称定,加环己烷溶解并定量稀释成3~5μg/mL的溶液,按照维生素A测定法(《中华人民共和国药典》1990年版二部附录第66页)测定其吸收峰的波长,并在表9-7所列各波长处测定吸收度。计算各吸收度与波长328nm处的吸收度的比值和波长328nm处的 。
。
测定应在半暗室中快速进行。
表9-7
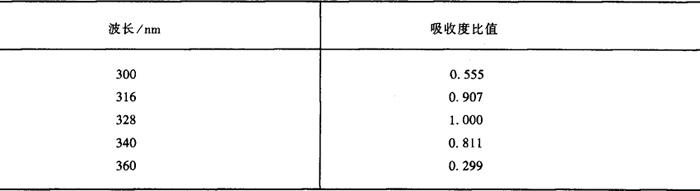
4.分析结果的表述
如果吸收峰波长在326~329nm之间,且所测得各波长吸收度比值不超过表(9-7)中规定值的±0.02,可用式(9-36)计算含量:

式中 x——每克样品中含有维生素A的单位 ——百分吸收系数
——百分吸收系数
如果吸收峰波长在326~329nm之间,但所测得的各波长吸收度比值超过表9-6中规定值的±0.02,应按式(9-37)求出校正后的吸收度,然后再计算含量。
A328(校正)=3.52(2A328-A316-A340) (9-37)
式中 A328(校正)——在波长328nm处校正后的吸收度
A328——在波长328nm处的吸收度
A316——在波长316nm处的吸收度
A340——在波长340nm处的吸收度
如果校正吸收度与未校正吸收度相差不超过±3.0%,则不用校正吸收度,仍以未经校正的吸收度计算含量。
如果校正吸收度与未校正吸收度相差在-15%~-3%之间,则以校正吸收度计算含量。
如果校正吸收度超过未校正吸收度的-15%或+3%,或者吸收峰波长不在326~329nm之间,则样品须按照《中华人民共和国药典》1990年版二部附录第66页维生素A测定法项下第二法测定。
5.允许差
本方法两次平行测定的允许相对差在3%以内。
三、食品中维生素A的测定
(一)紫外分光光度法
1.原理
维生素A为脂溶性维生素。先将样品中脂肪抽提出来,经皂化,萃取不皂化部分,再经柱层析,除去杂质,利用维生素A在紫外325nm的最大吸收特性测定。
2.试剂和溶液
2.1 乙醚 分析纯,不含过氧化物。
2.2 石油醚 30~60℃石油醚,重蒸。
2.3 无水硫酸钠 分析纯。
2.4 洗脱液 乙醚在石油醚中浓度(体积分数)分别为4%、8%、12%、16%、20%、24%、30%、35%、40%、45%和50%。
2.5 800g氢氧化钾 氢氧化钾(分析纯)400g溶于水,至500mL。
2.6 维生素A油剂。
2.7 无水乙醇 分析纯。不含醛类。
2.8 焦性没食子酸 分析纯,粉状。
2.9 氨水 分析纯,含氨25%~28%。
2.10 25%三氯化锑氯仿液 分析纯。25g三氯化锑溶于100mL氯仿,贮于棕色瓶中。
2.11 碱性氧化铝(层析用,100~200目) 碱性氧化铝在120℃烘箱烘4h后,称取100g加4mL蒸馏水于150mL试剂瓶中,用力振荡使无块状,瓶口封紧,贮入干燥器,16h后使用。
2.12 中性氧化铝(层析用,100~200目) 中性氧化铝于550℃高温炉中活化5.5h,降温至300℃左右(约1.5h),取出装瓶,冷后每100g加4mL蒸馏水于150mL试剂瓶中,用力振荡使无块状,瓶口封紧,贮入干燥器,16h后使用。
3.仪器
3.1 层析柱 2cm×30cm,具活塞,有砂芯玻璃板。
3.2 紫外分光光度计。
4.测定方法
整个步骤应避免阳光直射,层析时,须在暗室。
4.1 抽提皂化 准确称取10±0.1g(约含维生素A200~300IU)样品于烧杯中,加40mL水搅匀,移入250mL分液漏斗中,分别加氨水5mL、乙醇35mL,摇匀,用乙醚3×40mL振摇抽提,乙醚层用3×100mL水洗涤,水层用30mL乙醚再抽提一次,合并乙醚层,在氮气流下,于40℃以下减压蒸干,加30mL800g/L氢氧化钾、40mL乙醇、0.8g焦性没食子酸,在83±1℃水浴中皂化30min。
4.2 水洗蒸干 冷却后,移入250mL分液漏斗中,加60mL水,用30×40mL乙醚抽提,合并醚层,用水洗至中性按4.1中方法蒸干后溶于5mL石油醚,移入刻度试管。
4.3 层析 依次装8cm高中性氧化铝、3cm高碱性氧化铝及1cm无水硫酸钠于层析柱内,以石油醚浸透(湿法装柱),将4.2所得5mL石油醚样品液缓缓入柱,以2×1mL石油醚洗试管后并入柱内,石油醚流速为30~40滴/min,当液面下降至接近无水硫酸钠表面时,加5mL石油醚,随后再逐次加5mL4%、8%、……45%洗脱液,最后用50%洗脱液洗脱,层析柱上第一个黄色层析带一般是β-胡萝卜素,此带在12%洗脱液前后洗出,收集于10mL容量瓶中,至流出之洗脱液无黄色为止(此液可供测定β-胡萝卜素)。
维生素A一般在50%洗脱液前后洗出,用2mL刻度试管,每管准确收集1mL,吸约0.2mL于微型烧杯中,加约0.3mL25%三氯化锑氯仿溶液,如呈蓝色,表明有维生素A,分别从有维生素A的各管精确吸0.5mL于10mL容量瓶中,以石油醚定容。
4.4 测定 维生素A在323~326nm有一最大吸收峰,在石油醚中其比吸光度 为1830,用紫外分光光度计,以石油醚为空白,1cm石英比色皿,在波长325nm测吸光度。
为1830,用紫外分光光度计,以石油醚为空白,1cm石英比色皿,在波长325nm测吸光度。
5.分析结果的表述
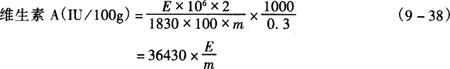
式中 E——吸光度
m——样品质量,g
每0.3μg维生素A为1IU。
(二)三氯化锑比色法
1.原理
维生素A在氯仿溶液中能与三氯化锑形成蓝色物质。此蓝色溶液在620nm处有一最大吸收光谱,且蓝色深浅与维生素A的含量成正比,此蓝色物质虽然不甚稳定,能很快褪色或变成其他颜色,但仍可在一定时间内(6s内),用分光光度计比色测定。
2.试剂和溶液
2.1 乙醚 蒸馏乙醚,弃去初馏液和残留液各10%,在1cm比色杯中,以重蒸水为参比测定吸光度,在波长300~350nm处吸光度应为零,不应含有过氧化物。
过氧化物检查方法:在有5mL乙醚的试管中,加入50%碘化钾溶液1mL,振摇0.5min,观察水层,如呈黄色,即表示有过氧化氢存在。
2.2 乙醇 应不含醛类物质。检查方法:取少量乙醇,加入银氨溶液加热,若有银镜反应发生,表示样品中有醛。
脱醛处理:取乙醇1~2L,加硝酸银2g(先溶于少量水中),振摇,再加氢氧化钠4g(先溶于温乙醇中再倒入),振摇过夜,将层清液倾入蒸馏瓶中蒸馏,弃初馏液10%。
2.3 50%氢化钾溶液。
2.4 无水硫酸钠。
2.5 氯仿 将氯仿置分液漏斗中,用蒸馏水洗涤数次后,将氯仿层取出蒸馏,然后用无水硫酸钠脱水即成。
2.6 三氯化锑溶液 20g三氯化锑及2mL无水乙酸,加氯仿溶解成100mL。
2.7 石油醚 沸程30~60℃。
2.8 95%乙醇。
2.9 浓氨水。
2.10 0.5mol/LKOH溶液。
2.11 醋酸酐。
2.12 维生素A标准溶液 1000IU/mL贮备液:取醋酸维生素A(1g=1000000IU)0.1g,用氯仿溶解,移于100mL容量瓶中,用氯仿定容。
100IU/mL中间液:精确吸取贮备液10mL于100mL容量瓶中,用氯仿定容。临用时配制。
10IU/mL工作液:精确吸取中间液10mL于100mL容量瓶中,用氯仿定容。临用时配制。
3.测定方法
3.1 样品处理 称取适量经组织捣碎或搅匀的样品,置小烧杯中,加水至10mL,再加氢氧化铵10mL,用玻璃棒搅成匀乳状,倒入100mL具塞量筒中(若为液体样品可直接吸取10mL于量筒中,加氢氧化铵1.25mL,以下步骤按鲜乳中有关脂肪测定方法处理),用10mL乙醇分数次洗入烧杯中,洗液并入量筒中,加塞振摇。再以2.5mL乙醚洗涤烧杯,并入量筒中。加塞振荡1min。静置约0.5h,待分层清晰后,分出脂肪醚层,供测定用。操做应迅速、避光。
3.2 皂化 取适量的提取醚层于蒸馏瓶中,置70℃水浴上蒸发醚层至4~5mL,加入数粒玻璃珠,加入50%氢氧化钾溶液30mL、无水乙醇40mL,在水浴上回流0.5~1h,至皂化完全,加入10mL水,振摇,皂化液澄清透明,不混浊,即表示皂化完全。
3.3 提取 将皂化瓶内溶液移入500mL分液漏斗中,用40~60mL温水(30~40℃)洗皂化瓶,洗液亦并入分液漏斗中,加入50mL乙醚振摇抽提,静置分层,如有少量乳化现象,可加入少量无水乙醇除去。醚层移入另一分液漏斗,水层继续以50mL石油醚、50mL乙醚、40mL石油醚、40mL乙醚分次振摇提取,合并醚层,然后分别用水、0.5mol/LKOH溶液反复洗至中性,弃水层,醚层过无水硫酸钠,用乙醚洗分液漏斗,漏液在三角烧瓶中于水浴上回收乙醚至5mL左右,减压至恰干,迅速加入5mL氯仿,用少量氯仿洗三角烧瓶,并用氯仿定容至10mL。
4.测定
4.1 标准曲线的绘制 精确吸取维生素A标准中间液或工作液(视样品中维生素含量高低而定)1.0mL,2.0mL,3.0mL,4.0mL,5.0mL,分别置10mL量瓶中,用氯仿定容。分别吸取上述标准液1mL,以试剂为空白,加入醋酸酐1滴,同4.2测吸光度,绘制标准曲线。
4.2 样品测定 以1mL氯仿加3mL三氯化锑氯仿液作空白,用1cm杯,于波长620nm处测样品液吸光度。先将1mL样品液加3mL三氯化锑氯仿液迅速搅匀,倒入比色皿,立即读取最大吸光度,从标准曲线上查得维生素A含量。
5.分析结果的表述

式中 ρ——从标准曲线上查得维生素A的浓度,IU/mL
V1——用氯仿定容的量,mL
V2——样品测定时所取样液的量
m——样品质量,g