防腐剂的测定
出处:按学科分类—工业技术 中国轻工业出版社《焙烤工业实用手册》第602页(9515字)
(一)山梨酸(钾)、苯甲酸(钠)的测定——薄层色谱法
1.原理
样品酸化后:用乙醚提取山梨酸、苯甲酸。将样品提取液浓缩,点于聚酰胺薄层板上展开。显色后,根据薄层板上山梨酸、苯甲酸的比移值,与标准比较定性,并可进行概略定量。食品卫生检验常要测定食品中是否添加苯甲酸及其含量是否超过卫生标准,采用薄层层析测定能达到此目的。
2.试剂
(1)异丙醇。
(2)正丁醇。
(3)石油醚:沸程:30~60℃。
(4)乙醚:不含过氧化物。
(5)氨水。
(6)1∶1盐酸:取100mL盐酸,加水稀释至200mL。
(7)无水乙醇。
(8)聚酰胺粉:200目。
(9)山梨酸标准溶液:精密称取0.20000g山梨酸,用少量乙醇溶解后移入100mL容量瓶中,并稀释至刻度,此溶液每毫升含2mg山梨酸。
(10)苯甲酸标准溶液:精密称取0.2000g苯甲酸,用少量乙醇溶解后,移入100mL容量瓶中,并稀释至刻度。此溶液每毫升含2mg苯甲酸。
(11)展开剂。
①正丁醇∶氨水∶无水乙醇(7∶1∶2)。
②异丙醇∶氨水∶无水乙醇(7∶1∶2)。
(12)显色剂:0.04%溴甲酚紫的50%乙醇溶液,用4g/L氢氧化钠溶液调pH至8。
(13)氯化钠酸性溶液(40g/L):于氯化钠溶液(40g/L)中加入少量6mol/L盐酸酸化。
3.仪器
(1)吹风机。
(2)层析缸。
(3)玻璃板:10cm×18cm。
(4)微量注射器:10μL,100μL。
(5)喷雾器。
4.操作方法
(1)样品提取:称取2.5g事先混合均匀的样品,置于25mL带塞量筒中,加0.5mL盐酸(1∶1)酸化,用15、10mL乙醚提取2次,每次振摇1min,将上层醚提取液吸入另一个25mL带塞量筒中,合并乙醚提取液。用3mL氯化钠酸性溶液(40g/L)洗涤2次,静置15min,用滴管将乙醚层通过无水硫酸钠滤入25mL容量瓶中。加乙醚至刻度,混匀。吸取10.0mL乙醚提取液分两次置于10mL带塞离心管中,在约40℃的水浴上烤干,加入0.10mL乙醇溶解残渣,加塞备用。
(2)测定:
①聚酰胺粉板的制备:称取1.6g聚酰胺,加0.4g可溶性淀粉,加约15mL水,研磨3~5min,立即倒入涂布器内制成10cm×18cm、厚度0.3mm的薄层板2块,于室温干燥后,于80℃下干燥1h,取出,置于干燥器内备用。
②点样:在薄层板下端2cm的基线上,用微量注射器点1、2μL样品液,同时各点1、2μL山梨酸、苯甲酸标准溶液。
③展开与显色:将点样后的薄层板放入预先盛有展开剂①或②的展开槽内,展开槽周围贴有滤纸,待溶剂前沿上展至10cm,取出挥干,喷显色剂,斑点成黄色,背景为蓝色。样品中所含山梨酸、苯甲酸的量与标准斑点比较定量(山梨酸、苯甲酸的比移值依次为0.82、0.73)。
5.计算

式中 x——样品中山梨酸(苯甲酸)的含量(g/kg);
A——测定用样品液中山梨酸(苯甲酸)的含量(mg);
m——样品质量(g);
V1——加入乙醇的体积(mL);
V2——测定时点样的体积(mL);
10——测定时吸取乙醚提取液的体积(mL);
25——样品乙醚提取液总体积(mL)。
例:在测定酱腌菜中苯甲酸含量时,称取2.5g样品,制成25mL乙醚提取液。取10.0mL乙醚提取液,挥干乙醚后用0.1mL乙醇溶解残渣。然后按薄层色谱法测定,已知样品液1μL与标准溶液1μL(含苯甲酸2μg)斑点相同,计算样品中苯甲酸含量。
代入公式:

6.注意事项
(1)活化聚酰胺板时,温度不要超过85℃以上。温度太高,薄板不牢固,容易脱落。薄板活化后,应立即使用。
(2)要严格按规定加入展开剂及各试剂,否则分不开。
(3)薄板如不显色,可置紫外灯下254nm处观察。
(4)展开槽一定要干燥无水,然后再倒入展开剂。
(二)山梨酸(钾)、苯甲酸(钠)的测定——气相色谱法
1.原理
样品经酸化后,山梨酸、苯甲酸用乙醚提取浓缩后,用附氢火焰离子化检测器的气相色谱仪进行分离测定,与标准系列比较定量。
2.试剂
(1)乙醚。
(2)石油醚:沸程30~60℃。
(3)盐酸。
(4)无水硫酸钠。
(5)盐酸(1∶1):取100mL盐酸,加水稀释至200mL。
(6)氯化钠酸性溶液(40g/L):于氯化钠溶液(40g/L)加少量盐酸(1∶1)酸化。
(7)山梨酸、苯甲酸标准溶液:精密称取山梨酸、苯甲酸各0.2000g,置于100mL容量瓶中,用石油醚-乙醚(3∶1)混合溶剂溶解后并稀释至刻度。此溶液每毫升相当于2mg山梨酸或苯甲酸。
(8)山梨酸、苯甲酸标准系列使用液:吸取适量的山梨酸、苯甲酸标准溶液,以石油醚-乙醚(3∶1)混合溶剂稀释至每毫升相当于50、100、150、200、250μg山梨酸或苯甲酸。
3.仪器
气相色谱仪:具氢火焰离子化检测器。
4.操作方法
(1)样品提取:按薄层色谱法中“样品提取”自“称取2.5g”至“加乙醚至刻度”依法操作。准确吸取5mL乙醚提取液于5mL带塞刻度试管中,置40℃水浴上挥干,加入2mL石油醚-乙醚(3∶1)混合溶剂溶解残渣,备用。
(2)色谱条件:
①色谱柱:玻璃柱,内径3mm,长2m,内装涂以5%DEGS+1%H3PO4固定液的60~80目Chromosorb W AW。
②气流速度:载气、氮气,50mL/min(氮气和空气、氢气之比按各仪器型号不同选择各自的最佳比例条件)。
③温度:进样口230℃;检测器230℃;柱温170℃。
(3)测定:进样2μL标准系列中各浓度标准使用液于气相色谱仪中,可测得不同浓度山梨酸、苯甲酸的峰高,以浓度为横坐标,相应的峰高值为纵坐标,绘制标准曲线。同时进样2μL样品溶液,测得峰高与标准曲线比较定量。
5.计算
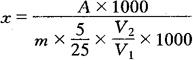
式中 x——样品中山梨酸或苯甲酸的质量分数(g/kg);
A——测定用样品液中山梨酸或苯甲酸的含量(μg);
V1——加入石油醚-乙醚(3∶1)混合溶剂的体积(mL);
V2——测定时进样的体积(μL);
m——样品的质量(g);
5——测定时吸取乙醚提取液的体积(mL);
25——样品乙醚提取液的总体积(mL)。
6.说明与注意事项
(1)由测得的苯甲酸的量乘以1.18,即为样品中苯甲酸钠的含量。
(2)通过无水硫酸钠层过滤后的乙醚提取液应达到去除水分的目的,否则5mL乙醚提取液在40℃挥去乙醚后仍残留少量水分,影响测定结果。
(3)结果表述:报告算术平均值用二位有效数。
(4)在色谱图中山梨酸保留时间为2.9min;苯甲酸保留时间为6.1min。
(三)苯甲酸的测定——中和法
1.原理
试样加入饱和氯化钠溶液在碱性条件下进行萃取,分离蛋白质、脂肪等,然后酸化,用乙醚提取试样中苯甲酸,将乙醚蒸去,溶于中性醚醇混合液中,再用标准碱液测定。
2.试剂
(1)乙醚。
(2)1∶1盐酸。
(3)10%氢氧化钠。
(4)氯化钠的饱和溶液。
(5)氯化钠。
(6)95%的中性乙醇:以酚酞为指示剂,用氢氧化钠中和至微红色。
(7)酚酞指示剂。
(8)中性醚醇混合液:将乙醚与中性乙醇按1∶1(体积分数)比例混合,以酚酞为指示剂,用氢氧化钠中和至微红色。
(9)0.05mol/L氢氧化钠:取纯氢氧化钠3g,加少量蒸馏水使溶去其表面部分,弃去这部分溶液,随即将剩余的氢氧化钠(约2g)用经过煮沸后冷却的蒸馏水溶解并稀释至1000mL,用邻苯二甲酸氢钾标定。
3.测定方法
(1)样品处理:
①固体或半固体样品:称取切细粉碎的样品100g置于500mL容量瓶中,加入300mL水,加入分析纯氯化钠至不溶解为止(使其饱和),然后用10%氢氧化钠溶液使成碱性,摇匀,再加饱和氯化钠溶液至刻度,放置2h(要不断振摇),过滤,弃去最初10mL滤液,收集滤液供测定用。
②样品中含有多量脂肪时,用上述制备好的滤液中加入氢氧化钠溶液使成碱性,加入20~50mL乙醚提取,振荡3min,静置分层,溶液供测定用。
(2)提取:吸取以上滤液各100mL于250mL分液漏斗中,加6mol/L盐酸至呈酸性(用石蕊试纸试验),再过量3mL,依次用40、30、30mL乙醚用旋转方法小心提取,每次摇动不少于5min,三次提取液合并,置另一250mL分液漏斗中。
用蒸馏水洗涤乙醚抽提液至不呈酸性(以石蕊试纸试验),将乙醚提取液置于锥形瓶中,于45℃水浴回收并挥干乙醚。
(3)滴定:加入30mL中性醚醇混合液及10mL水,加酚酞2滴,以0.05mol/L氢氧化钠标准液滴定至微红色为止。
4.结果计算

式中 c——氢氧化钠标准溶液的摩尔浓度(mol/L);
V——消耗氢氧化钠的体积(mL);
m——试样质量(g);
0.1441——1mol/L氢氧化钠标准溶液1mL相当于苯甲酸钠的克数;
0.1221——1mol/L氢氧化钠标准溶液1mL相当于苯甲酸的克数。
5.注意事项
(1)试样用NaCl饱和,其主要作用是除去试液中所含蛋白质及水解产物,以免在用乙醚进行提取时产生乳化,造成两相分离的困难,同时避免氨基酸对滴定的影响。另一个作用是由于NaCl的加入可降低苯甲酸的溶解度,以减少在提取及水洗过程中的损失。
(2)用乙醚提取时不要上下振荡以免生成乳浊液而不易分离,应旋转分液漏斗进行提取,若形成乳浊液,可用一玻璃棒搅拌,或进行一二次上下的激烈振荡,或进行离心分离。
(3)当苯甲酸含量低时,氢氧化钠标准液的浓度应配成0.01mol/L为宜。本法适用于样品含苯甲酸为0.1%以上的分析。
(四)山梨酸(钾)的测定——分光光度法
1.原理
提取样品中山梨酸及其盐,在硫酸及重铬酸钾的氧化作用下形成丙二醛,丙二醛与硫代巴比妥酸形成红色化合物,于波长530nm处有最大的吸收,测定吸光度以定量。
2.试剂
(1)重铬酸钾-硫酸溶液:0.5%重铬酸钾与0.15mol/L硫酸按1∶1比例混合。
(2)硫代巴比妥酸溶液:准确称取0.5g硫代巴比妥酸于100mL容量瓶中,加入20mL水,加10mL 1mol/L氢氧化钠溶液,充分摇匀,使之完全溶解后再加入11mL 1mo1/L盐酸,用水定容(临用时配制,不超过6h内使用)。
(3)山梨酸钾标准液:准确称取250mg山梨酸钾于250mL容量瓶中,用蒸馏水溶解并定容,此溶液1mL含山梨酸钾1mg。使用时再稀释为0.1mg/mL(取25mL用蒸馏水定容250mL)。
3.仪器
(1)分光光度计。
(2)组织捣碎机。
(3)10mL比色管。
4.测定方法
(1)样品处理 称取100g样品,加水200mL,于组织捣碎机内捣成匀浆。称取匀浆100g,加水200mL继续捣1min,称取10g于250mL容量瓶中定容,摇匀,过滤备用。
(2)标准曲线绘制 吸取0、2.0、4.0、6.0、8.0、10.0mL浓度为0.1mg/mL的山梨酸钾标准液于200mL容量瓶中,用水定容,分别吸取2.0mL于相应的10mL比色管中,加2mL重铬酸钾-硫酸溶液,于100℃水浴中加热7min,立即加入2mL硫代巴比妥酸,继续加热10min,立即用冷水冷却,在分光光度计中以530nm测定吸光度,绘制标准曲线。
(3)试样测定 吸取试样处理液2mL于10mL比色管中,按标准曲线绘制操作,于分光光度计中,以530nm测定吸光度,从标准曲线上查出相应浓度。
5.结果计算


式中 c——试样液中含山梨酸钾浓度(mg/mL);
m——称取匀浆相当于试样质量(g);
2——用于比色试样体积(mL);
250——试样处理液总体积(mL)。
6.说明
(1)山梨酸标准溶液应贮于冰箱内,可使用数月。
(2)氧化、显色过程应严格控制条件。
(五)禁用防腐剂定性试验
1.硼砂、硼酸
(1)试剂:
①盐酸(1∶1)。
②碳酸钠溶液(40g/L)。
③氢氧化钠溶液(4g/L)。
④姜黄试纸(称取20g姜黄粉末,用冷水浸渍4次,每次各100mL,除去水溶性物质后,残渣在100℃干燥,加100mL乙醇,浸渍数日,过滤。取1cm×8cm滤纸条,浸入溶液中,取出,于空气中干燥,贮于玻璃瓶中)。
(2)样品处理:称取3~5g固体样品,加碳酸钠溶液充分湿润后,于小火上烘干,炭化后再置高温炉中灰化。量取10~20mL液体样品,加碳酸钠溶液至碱性后,置水浴锅上蒸干,炭化后置高温炉中灰化。
(3)定性试验:
①姜黄试纸法:取一部分灰分,滴加少量水与盐酸至微酸性,边滴边搅拌,使残渣溶解,微温后过滤。将姜黄试纸浸入滤液中,取出试纸置表面皿上,于60~70℃干燥,如有硼酸、硼砂存在时,试纸显红色或橙红色,在其变色部分熏以氨即转为绿黑色。
②焰色反应:取灰分置于坩埚中,加硫酸数滴及乙醇数滴,直接点火,硼酸或硼砂存在时,火焰呈绿色。
2.水杨酸
(1)试剂:
①三氯化铁溶液,10g/L。
②亚硝酸钾溶液,100g/L。
③乙酸(50%)。
④硫酸铜溶液,100g/L:称取10g五水硫酸铜,加水溶解至100mL。
(2)样品提取:焙烤食品中含蛋白质、脂肪、淀粉多的食品:称取25.0g均匀试样,置于透析用玻璃纸中,放入大小适当的烧杯中,加50mL氢氧化钠溶液(0.8g/L),调成糊状,将玻璃纸口扎紧,放入盛有200mL氢氧化钠溶液(0.8g/L)的烧杯中,盖上表面皿,透析过夜。量取125mL透析液(相当于12.5g样品),加约0.4mL盐酸(1∶1)使之成中性,加20mL硫酸铜溶液,混匀,再加入4.4mL氢氧化钠溶液(40g/L)混匀,静置30min,过滤。取120mL(相当于10g样品),置于250mL分液漏斗中,加2mL盐酸(1∶1),用30、20、20mL乙醚提取3次,合并乙醚提取液,用5mL盐酸酸化的水洗涤一次,弃去水层。乙醚层通过无水硫酸钠脱水后,挥发乙醚残渣备用。
(3)三氯化铁法定性:残渣加1~3滴三氯化铁,水杨酸存在时呈紫堇色。
确证试验:溶解残渣于少量热水中,冷后加4~5滴亚硝酸钾溶液,4~5滴乙酸及1滴硫酸铜,混匀,煮沸0.5h,放置片刻,水杨酸存在时呈血红色(苯甲酸不显色)。