食品中柠檬酸及其盐类的测定方法
出处:按学科分类—工业技术 中国轻工业出版社《食品添加剂分析检验手册》第4页(7763字)
化学名:柠檬酸
结构式:
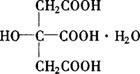
分子式:C6H8O7·H2O
相对分子质量:210.14(结晶);192.13(无水)
一、柠檬酸的鉴别
1.试剂
1.1 稀硫酸。
1.2 高锰酸钾。
1.3 硫酸汞。
1.4 溴水。
1.5 吡啶-醋酐(3∶1)。
2.操作步骤
2.1 取本品少许,用直火炽灼,即缓缓分解,但不发生焦糖臭(与酒石酸的区别)。
2.2 本品显柠檬酸盐的反应。
2.2.1 取试品溶液2mL(约相当于柠檬酸10mg),加稀硫酸数滴,加热至沸,加高锰酸钾试液数滴,振摇,紫色即消失。溶液分成2份∶1份中加硫酸汞试液1滴;另1份逐滴加入溴试液,均生成白色沉淀。
2.2.2 取试品约5mg,加吡啶-醋酐(3∶1)约5mL,振摇,即生成黄色到红色或紫红色的溶液。
二、柠檬酸含量的测定
取本品约1.5g,精密称定,加新沸过的冷水40mL溶解后,加酚酞指示液3滴,用1mol/LNaOH滴定液滴定。每毫升的氢氧化钠滴定液(1mol/L)相当于64.04mgC6H8O7。
柠檬酸盐类
化学名:柠檬酸钠(Sodium Citrate)
结构式

分子式:C6H5Na3O7·2H2O
相对分子质量:294.10
化学名:柠檬酸钙(Calcium Citrate)
结构式

分子式:C12H10O14Ca3·4H2O
相对分子质量:570.48
化学名:柠檬酸铁(Ferric Citrate)
分子式:FeC6H5O7
相对分子质量:245
化学名:柠檬酸铁铵(Ferric Ammonium Citrate)
分子式:(NH4)3C6H5O7·FeC6H5O7
相对分子质量:488
三、食品中柠檬酸及其盐类的测定方法
(一)气相色谱法
1.原理
食品中柠檬酸及其盐类按气相色谱法定量柠檬酸的三甲硅烷来定量柠檬酸。按需要以相对分子质量比求出各种盐类的量。食品中由于有天然柠檬酸存在,所以定量值应为食品中固有的和添加的总量。
2.试剂和溶液
2.1 离子交换柱 将20g阴离子交换树脂以湿法充填在Φ1.5cm×30cm的柱子中。
2.2 三甲基甲硅烷化液(TMS) 采用市售的气相色谱用的N,O-双(三甲基硅烷)乙酰胺。
2.3 吡啶 硅烷化用吡啶。
3.仪器
带有氢火焰检测器的气相色谱仪(FID-GC),按以下条件测定:
填充剂:用60~80目色谱纯的硅藻土,涂以1.5%SE-30
柱:玻璃柱,内径3mm,长1.5m
柱温:180℃
载气:氮气
4.操作步骤
4.1 样品制备在含柠檬酸5~50mg范围内,准确称取20g以下样品。若是液体样品,可将样品直接注入离子交换柱内。若是固体样品,加30mL水,于捣碎机中进行匀浆。用20mL水将样品洗入带塞离心管中,加50mL正己烷(含脂肪样品先脱脂),充分振摇混合,离心,弃己烷层,分取水相,过滤,用少量水洗离心管及残渣,过滤。合并滤液及洗液,必要时用0.1mol/LNaOH溶液调节pH至7,注入离子交换柱,用100mL水冲洗后,用2mol/LHCl溶液、丙酮(1∶1)混合液洗脱,洗脱液盛于50mL容量瓶中,并加水至刻度。取此液5mL,置梨形瓶中,于水浴上减压浓缩至干。加0.5mL吡啶及TMS化液0.5mL,密盖后于12.5℃加热10min[注],冷至室温,用5mL吡啶洗入10mL容量瓶中,加吡啶定容至刻度,即为样品溶液。
注:三甲基硅烷化时,最好溶剂为吡啶,加热反应混合液时,TMS化物的生成率是稳定的。TMS化时,若
有无机盐存在,则TMS化物生成率下降。加热时,必须注意不能飞溅,而应平稳。
4.2 标准液的制备 准确称取100mg无水柠檬酸,加水溶解至100mL。取此液10mL,加水至1000mL,即为标准液(含柠檬酸10μg/mL)。取标准液5mL、10mL、20mL、30mL、40mL及50mL,分别置梨形瓶中,于水浴上减压浓缩至干,各加入0.5mL吡啶及0.5mLTMS化液,密塞,于12.5℃加热10min,冷至室温,即为标准曲线用标准液(此液分别各含柠檬酸50μg/mL、100μg/mL、200μg/mL、300μg/mL、400μg/mL及500μg/mL)。
5.测定方法
5.1 标准曲线绘制 取标准曲线用标准液各5μL,注入色谱仪中,以峰高绘制标准曲线。
5.2 分析结果的表述 将5μL样品溶液注入色谱仪中,测得峰高,查标准曲线求得样品液中柠檬酸浓度(μg/mL),按式(1-3)计算出样品中柠檬酸含量(g/kg)。

式中 ρ——样液中柠檬酸浓度,μg/mL
m——取样量,g
柠檬酸(结晶)含量(g/kg)=柠檬酸含量(g/kg)×1.094
柠檬酸钠含量(g/kg)=柠檬酸含量(g/kg)×1.531
(二)比色法
1.原理
食品中柠檬酸及其盐类以柠檬酸分解酶、乳酸脱氢酶和苹果酸脱氢酶来定量柠檬酸。由于食品中存在有天然柠檬酸,所以测定值应为天然和添加的柠檬酸总量。
2.试剂和溶液
2.1 氯化锌 分析纯。
2.2 氯化锌溶液 取80mg氯化锌加水溶解至100mL。
2.3 柠檬酸分解酶(CL) 分析纯。
2.4 柠檬酸分解酶溶液 取21mg冻干的柠檬酸分解酶(约5mg酶朊蛋白),冰冷后加1mL重蒸馏水溶解。此液保存于4℃,可稳定1周,冰冻保存,可稳定4周。
2.5 甘氨酰替甘氨酸 特级。
2.6 甘氨酰替甘氨酸缓冲液 取7.13g甘氨酰替甘氨酸,加约70mL重蒸馏水溶解后,用5mol/LNaOH溶液调节pH至7.8,加10mL氯化锌溶液,加水至100mL。保存于4℃,可稳定4周。
2.7 酶混合液(MDH/LDH) 苹果酸脱氢酶及乳酸脱氢酶混合液(MDH0.5mg/mL,LDH2.5mg/mL)。将0.1mL(5mg/mL)MDH、0.4mL3.2mol/L〔 (NH4)2SO4〕溶液和0.5mLLDH(5mg/mL)混合配制。保存于4℃,可稳定1年。
(NH4)2SO4〕溶液和0.5mLLDH(5mg/mL)混合配制。保存于4℃,可稳定1年。
2.8 碳酸氢钠 特级。
2.9 β-辅酶Ⅰ二钠(还原型)(NADH-Na2) 分析纯。
2.10 乳酸脱氢酶(LDH) 分析纯。
2.11 硫酸铵 特级。
2.12 苹果酸脱氢酶(MDH) 分析纯。
2.13 NADH溶液(辅酶Ⅰ) 取30mgNADH-Na2及60mg碳酸氢钠,溶于6mL重蒸馏水中。保存于4℃,可稳定4周。
3.仪器
紫外分光光度计。
4.操作步骤
4.1 样品溶液的制备。
4.1.1 液体食品:柠檬酸含量在2~40mg,准确称取样品10g以下。若是无色澄明或色淡样品,加水至100mL,即为样品溶液。若是混浊样品,加入50~60mL水,过滤,用20~30mL水分数次洗容器及残渣,合并滤液及洗液,加水至100mL,即为样品溶液。对于着色样品,加样品量1/10的聚酰胺粉末或聚乙烯吡咯环酮,必要时加20~30mL水,剧烈搅拌混合,过滤,用40~50mL水洗容器及残渣数次,合并滤液及洗液,加水至100mL,作为样品溶液。
4.1.2 固体食品:含柠檬酸在2~40mg,准确称取10g以内样品。不含蛋白质、脂肪的样品,则将样品放入匀浆器中,加50~60mL水,加热至60℃后,搅拌5min,过滤,用20~30mL水分数次洗容器及残渣,合并滤液及洗液,加水准确成100mL,作为样品溶液。含脂肪、蛋白质样品,放入搅拌器,加入30~40mL水,加热至60℃,搅拌5min后,以60℃加热15min,冷却,于冰箱中放置20min,过滤,用20~30mL水洗容器及残渣数次,合并滤液和洗液,加入0.4mol/LHClO410mL,摇匀,加2mol/LNaOH溶液中和后,加水定容至100mL,在冰箱中放置20min,按需要过滤,作为样品溶液。
4.1.3 标准液的制备:准确称取200mg无水柠檬酸,加水溶解至100mL,即为标准液(含柠檬酸2mg/mL)。分别取标准液1mL,5mL,10mL,15mL,20mL于100mL容量瓶中,加水至刻度,即为标准曲线用标准液(此液分别含柠檬酸20μg/mL、100μg/mL、200μg/mL、300μg/mL、400μg/mL)。
5.测定方法
5.1 测定条件 用紫外分光光度计,在波长340nm处测定吸光度。
5.2 测定 用2只10mL的试管,分别标明A、B,各加入1mL甘氨酰替甘氨酸缓冲液,0.1mLNADH溶液(辅酶Ⅰ)、0.02mL酶混合液[(苹果酸脱氢酶/乳酸脱氢酶(MDH/LDH)]及1.8mL水,A管加0.2mL样品溶液,B管加0.2mL水,混匀,放置5min,A为样品管,B为空白管。
用1cm比色杯,于波长340nm处,以水为参比,分别测定A、B管的吸光度EA及EB。然后于A、B管中分别加入0.02mL柠檬酸分解酶,混匀,放10min后,再测吸光度E′A和E′B。
求出EA与E′A之差△EA,EB与E′B之差△EB,再计算出△EA与△EB之差△ET。
5.3 标准曲线绘制 分别取0.2mL标准曲线用标准液S1、S2、S3……S5代替样品溶液,按5.2同样步骤操作,求出△Es1、△Es2、△Es3……△Es,,绘制标准曲线图。
5.4 分析结果的表述 根据样品溶液的△ET,从标准曲线图中查得样品溶液含柠檬酸量(μg/mL),按式(1-4)计算出样品中柠檬酸含量(g/kg)。

式中 ρ——样品溶液中柠檬酸浓度,μg/mL
m——取样量
柠檬酸(结晶)含量(g/kg)=柠檬酸含量(g/kg)×1.094
柠檬酸钠含量(g/kg)=柠檬酸含量(g/kg)×1.531
(三)高压液相色谱法
1.原理
样品经处理后,直接注入反相化学键合相色谱体系,用0.5%(NH4)2HPO4为流动相,有机酸在两相中分配分离,按照含碳数多少由少到多从柱中流出。经紫外检测器(214nm)或示差折光检测器测定,与标准比较定量。
2.试剂
2.1 有机酸标准溶液 取单个有机酸标准(酒石酸、苹果酸、乳酸、醋酸、柠檬酸、延胡索酸、琥珀酸)于50mL容量瓶中,用0.01mol/LNaOH溶液溶解后定容,并配制标准系列。
2.2 流动相 0.5%磷酸氢铵,用磷酸调节pH至2.8,经0.45μm微孔滤膜过滤,脱气后使用。
3.仪器和设备
3.1 高压液相色谱仪。
3.2 检测器 紫外检测器或示差折光检测器。
3.3 液相色谱柱 8mm×10cmRadial-PAK C18Cartridge,5μm(Waters公司)。
3.4 净化柱 SEP-PAK C18Cartridge(Waters公司)。
3.5 Z型加压组件或RCM-100型加压组件(Waters公司)。
3.6 微量注射器25μL。
4.操作步骤
4.1 液体样品 如清凉饮料、酒精饮料、咖啡溶液等,酱油、醋等需稀释10倍以上。用SEP-PAK C18Cartridge净化柱处理,收集馏出液,经0.45μm微孔滤膜过滤后,备用。
4.2 固体或半固体样品 如水果、蔬菜、腌制的农产品、蛋黄酱、咖啡等。将样品捣碎、均质后,加入一定量的0.01mol/LNaOH溶液提取,经离心分离或过滤后收集提取液,用SEP-PAK C18Cartridge净化柱处理,收集馏出液,经0.45μm微孔滤膜过滤后,备用。
5.测定条件和色谱图
测定和计算 注入有机酸标准系列溶液各10μL,进行高压液相色谱分析;同样注入试样溶液10μL,进行高压液相色谱分析,以保留时间定性,以峰高或峰面积结合标准曲线定量。
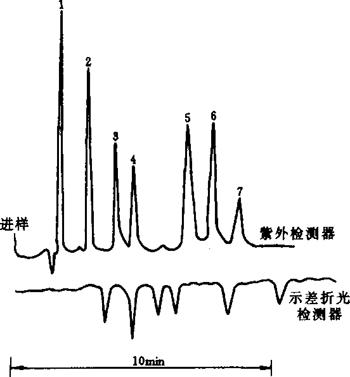
图1-1 有机酸的分离
1-酒石酸 2-苹果酸 3-乳酸 4-醋酸 5-柠檬酸 6-延胡索酸 7-琥珀酸
测定条件:
色谱柱:8mm×10cmRadial-PAK C18 Cartridge 5μm
流动相:0.5%(NH4)2HPO4用H3PO4调至pH2.81,2mL/min
进样量:10μL
检测器:紫外检测器214nm 0.1AUFS;示差折光检测器,4x;温度:室温
样品:标准溶液