配碱浓度和蒸煮初期碱液浓度的计算
书籍:制浆造纸工业计算手册上册
出处:按学科分类—工业技术 中国轻工业出版社《制浆造纸工业计算手册上册》第37页(971字)
【例】25m3蒸球的装料量为3500kg绝干麦草,已知草片水分含量为15%,蒸煮用碱量为10.4%(Na2O计),硫化度为11.1%,液比为1∶3,试按下列情况计算配碱浓度和蒸煮开始碱液浓度。①采取单独溶解Na2S的办法。已知Na2S纯度为64%,纯Na2S的溶解度(90C)为57.3g/100g水,加过量10L的水溶解。②采用固体NaOH溶解。③采用液体NaOH,其浓度为320g/L(NaOH计)。
解:总液量=3500×3=10500(L)
草片中含水量=3500× =620(L)
=620(L)
送入蒸球的碱液量=10500-620=9880(L)
用碱量=3500×10.4%=366.2(kg)(Na2O计)
硫化钠量=366.2×11.1%=40.7(kg)(Na2O计)
=40.7× =51.2(kg)(Na2S计)
=51.2(kg)(Na2S计)
氢氧化钠量=366.2-40.7=325.5(kg)(Na2O计)
=325.5× =420(kg)(NaOH计)
=420(kg)(NaOH计)
①如采取单独溶解硫化钠的办法,则应根据硫化钠的溶解度,加用过量热水,溶解硫化钠。
加入64%的Na2S的量=51.2÷64%=80(kg)
需加90℃溶解热水的量=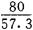 ×100+10=150(L)
×100+10=150(L)
硫化钠的浓度= ×1000=341(g/L)(Na2S计)
×1000=341(g/L)(Na2S计)
②如采用固体NaOH溶解,则
溶解NaOH的水量=9880-150=9730(L)
