胰腺癌
出处:按学科分类—医药、卫生 科学技术文献出版社《肝胆胰外科疾病诊断标准》第250页(10285字)
一、概述
胰腺癌最早由Mondiare及Battersdy叙述。1888年Bard和Pis在文献上做了临床报道。1935年,美国着名外科学家Whipple首先报道胰、十二指肠切除术成功,从而确立了手术治疗胰、十二指肠和壶腹部恶性肿瘤的方式。1943年,Rockeg首先实行了全胰切除术。国内余文光于1954年首先报道胰头、十二指肠切除的病例。近年来,胰腺癌的发病率逐年上升,在美国1988年发病率为9.0/10万,男∶女为1.3∶1。多见于45岁以上者。瑞典发病率较高,为125/10万,并且在过去20年里保持不变。英国和挪威各增加了1倍。70年代与60年代相比,加拿大、丹麦和波兰的标准化发病率增加了50%以上。在我国,胰腺癌已成为我国人口死亡的十大恶性肿瘤之一。北京协和医院近年来收住院的胰腺癌患者比50年代增加了5~6倍。而且据北京地区7家医院354例病例分析,患者中41~70岁者占80%,近年来,年轻的胰腺癌患者也较10年前有明显增加的趋势,而且恶性度更高,预后更差。就胰腺癌的发生部位而言,仍以胰头部位最多见,约占70%,胰体次之,胰尾部更次之,有的头体尾部均有,属于弥漫性病变或多中心性病变。
二、病因
目前,胰腺癌的病因及发病机制尚不十分清楚。最近的大量研究表明,胰腺癌的发生可能与以下因素有关。
1.吸烟 大量的研究支持胰腺癌与吸烟之间有密切联系。吸烟引起胰腺癌的可能机制:①吸烟促使致癌物质烟草特异性N—亚硝酸盐分泌到胆管,随后反流入胰管;②烟草特异性N—亚硝酸盐对器官的特异性作用可随血流入胰腺;③吸烟增加血脂水平,促发胰腺癌。吸烟者可能因细胞甲基化水平低而易致癌。Stolzenberg等的实验证实,保持足够的叶酸和吡哆醛浓度,可减少与吸烟相关的胰腺癌的危险性。
2.饮酒 不同种族饮酒后其胰腺癌发病率亦有不同。据Silverman等观察饮酒与美国黑人和白人胰腺癌发病率关系的研究显示,与白人相比,黑人男性嗜酒者及女性中度饮酒者均有较高发生率。
3.糖尿病 实验研究表明,胰岛素在体外或体内能促使胰腺癌细胞生长;高浓度胰岛素能使胰岛素样生长因子—1受体活化,产生包括细胞周期进程改变的生长促进效应。
4.慢性胰腺炎 流行病学和分子流行病学的研究大多支持慢性胰腺炎可以发展为胰腺癌。Friess的研究显示,在5600个基因中,34个基因在胰腺癌和慢性胰腺炎患者中的表达减少,157个基因在慢性胰腺炎中表达增强,而其中的152个基因在胰腺癌中也表达增强。这项研究从分子水平证明了慢性胰腺炎与胰腺癌可能存在某些联系。
5.幽门螺旋杆菌(Hp) 研究显示,胰腺癌患者中有Hp血清阳性结果,与对照组相比有显着差异,提示Hp感染与胰腺癌有相关性。
6.非类固醇类抗炎药(NSAID) 有研究显示,服用阿司匹林的妇女,胰腺癌的发病率降低。但也有研究显示,常规服用阿司匹林并不会降低胰腺癌的发生率,且胰腺癌发病风险可能增大,对这一现象的可能机制是:①阿司匹林对不同组织的脂肪氧合酶的影响不同,可能降低一些癌症的风险,又增加另一些癌症的风险;②阿司匹林可能与胰腺炎风险增加有关,而胰腺炎又与高胰腺癌风险有关。事实上,应用包括非特异性COX抑制剂和特异性COX—2抑制剂预防和治疗诸多消化道肿瘤,如食管癌、胃癌、结肠癌等,均取得较好的临床和实验结果。但NSAID对胰腺癌的确切作用还需进一步研究。
7.咖啡 调查发现,咖啡能使患胰腺癌的危险增加4倍。研究证明,咖啡可以抑制DNA修复并在DNA复制完成前诱导有丝分裂过程,是其致癌的主要原因。
肿瘤的发生和发展是一个复杂的多阶段过程,是多种肿瘤相关基因表达失常或许多肿瘤抑制基因失活所致。DNA芯片技术可直接检测mRNA的种类及丰富度,是研究基因表达的有力工具。
三、病理
胰腺癌致死性特高,可能由于它发病诡秘隐匿,确诊时多已进入晚期之故。早期即可转移到区域淋巴结(90%),甚至转移到纵隔及锁骨上淋巴结,确诊时半数以上患者已有肝转移,1/4以上患者已有腹膜种植,1/3患者已侵犯十二指肠并可溃破。胰腺癌的组织学类型以导管细胞癌最多,约占90%。其组织学分类尚无统一方案,下列分类法可作为参考:导管细胞癌如乳头状腺癌、管状腺癌、囊腺癌、鳞形上皮癌、腺鳞癌、黏液癌等,腺泡细胞癌,胰岛细胞癌,其他未分化癌、胰母细胞癌、癌肉瘤等。
1.导管腺癌 导管腺癌占胰腺癌的80%~90%,主要由分化不同程度的导管样结构的腺体构成,伴有丰富的纤维间质。高分化导管腺癌主要由分化较好的导管样结构构成,内衬高柱状上皮细胞,有的为黏液样上皮,有的具有丰富的嗜酸性胞浆。此癌性腺管有时与慢性胰腺炎时残留和增生的导管很难鉴别。中分化者由不同分化程度的导管样结构组成,有的与高分化腺癌相似,有的可出现实性癌巢。低分化者则仅见少许不规则腺腔样结构,大部分为实性癌巢,细胞异形性很大,可从未分化小细胞到瘤巨细胞,甚至多核瘤巨细胞,有时可见到梭形细胞;在有腺腔样分化的少区域,可有少量黏液,肿瘤的间质含有丰富的Ⅰ型和Ⅳ型胶原。
2.特殊类型的导管起源的癌
(1)多形性癌:亦称巨细胞癌,可能为导管癌的一种亚型。由奇形怪状的单核或多核瘤巨细胞,甚至梭形细胞构成,有时可类似于破骨细胞的巨细胞或绒癌样细胞。瘤细胞排列成实性巢状或呈肉瘤样排列。
(2)腺鳞癌:偶见于胰腺,可能为胰管上皮鳞化恶变的结果。肿瘤有腺癌和鳞癌成分。纯粹的鳞癌在胰腺相当罕见。
(3)黏液癌:切面可呈胶冻状,极相似于结肠的胶样癌。光镜下,肿瘤含有大量黏液,形成黏液池。细胞可悬浮其中或散在于黏液池的边缘。
(4)黏液表皮样癌和印戒细胞癌:在胰腺中偶可见到。
(5)纤毛细胞癌:形态与一般导管癌相同,其特点是有些细胞有纤毛。
3.腺泡细胞癌 仅占1%,肿瘤细胞呈多角形、圆形或矮柱形,核圆,常位于基底部。瘤细胞排成腺泡状或条索状,胞浆强嗜酸性颗粒状。电镜和免疫组织化学均显示瘤细胞的腺泡细胞特征,如丰富的粗面内质网和酶原颗粒。腺泡细胞癌主要转移至局部淋巴结、肝、肺或脾。
4.小腺体癌 为少见类型的胰腺癌。胰头部较为多见。镜下,肿瘤由很多小腺体结构及实性癌巢组成,其间有纤细的纤维间隔。细胞可为立方或柱状,核较为一致,常见小灶性坏死,在小腺体的腔缘可见少量黏液。近来研究表明,此型胰腺癌可能为腺泡细胞和内分泌细胞复合性肿瘤。
5.大嗜酸性颗粒细胞性癌 此型肿瘤罕见,其肿瘤细胞具有丰富的嗜酸性颗粒性胞浆,核圆形或卵圆形,排列成小巢状。其间有纤维间隔分隔。电镜瘤细胞胞浆内充满肥大的线粒体。
6.小细胞癌 胰腺的小细胞癌形态上与肺小细胞癌相似,占胰腺癌的1%~3%。由一致的小圆细胞或燕麦样细胞构成,胞浆很少,核分裂很多,常有出血坏死,NSE免疫组化染色阳性,此型预后很差。多在2个月内死亡。其起源尚不清楚。
四、分期
胰腺癌的临床分期对手术选择及治疗方法的优劣具有重要的意义。
(一)日本胰腺学会将其分为4期
Ⅰ期:肿瘤直径小于2cm,无区域淋巴结转移,未浸润胰腺包膜、后腹膜、门静脉、肠系膜上静脉及脾静脉。
Ⅱ期:肿瘤直径2.1~2.4cm,紧靠肿瘤的淋巴结有转移,胰包膜、后腹膜和前述血管有可能转移。
Ⅲ期:肿瘤直径4.1~6cm,第1站和第3站之间的淋巴结有转移,胰腺包膜和后腹膜有浸润。
Ⅳ期:肿瘤直径大于6.1cm,第3站淋巴结转移,侵犯邻近内脏、后腹膜及前述静脉有广泛浸润。
(二)1974年Hermreck等制定的分期标准
Ⅰ期:肿瘤仅位于胰腺原位。
Ⅱ期:肿瘤已浸润及周围组织(如十二指肠、门静脉、肠系胰血管等)。
Ⅲ期:肿瘤已转移到局部淋巴结。
Ⅳ期:伴远处转移或腹腔种植。
(三)根据Kloppel等的TNM分期法(1979年)
T1:肿瘤局限于胰腺内。
T2:肿瘤生长扩展已超越胰腺,肿瘤已浸润十二指肠、胃、胆管等,仍可被手术切除。
T3:肿瘤己浸润及邻近器官(如胆管、胃、肾上腺、脾)和(或)腹膜,手术已无法切除。
T3D:肿瘤扩展超过胰腺且浸润及十二指肠。
TX:肿瘤大小无法判定,或未作记录。
N0:但均无淋巴结转移。
N1:局部(胰腺周围)淋巴结已转移。
N2:局部旁淋巴结(肠系胰、腹腔、肝门区等淋巴结)已有转移。
NX:淋巴结已有转移,但未判明何组。
M0:但均无远处转移。
M1:远处转移。
(四)日本胰腺学会制定的分期标准
日本分期法:如表22—1所示,T仅指肿瘤的最大直径(cm);N指淋巴结转移情况,N0指无淋巴结转移,N1、N2、N3分别指第1、2、3站淋巴结转移;S指直接前包膜侵犯,Rp指腹膜后侵犯,PV指门脉系统受侵,其中0为无侵犯,1为可疑,2为肯定受犯,3为严重侵犯至邻近器官、后腹膜或门静脉。至于远处转移者,均归入Ⅳ期。
表22—1 日本分类法(凡有一项属1、2、3者分别归入Ⅰ、Ⅱ、Ⅲ期)

(五)UICC的胰腺癌分期标准
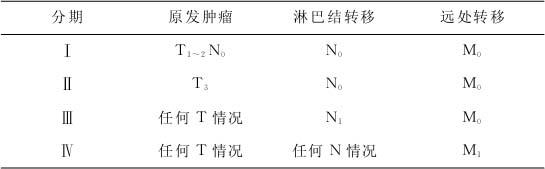
UICC分期(表22—2):T指肿瘤大小以及侵犯邻近组织情况,其第Ⅰ期包括肿瘤局限于胰腺组织(T1)以及侵犯十二指肠、胆管或胰周围组织但无淋巴结转移者(T2);第Ⅱ期包括肿瘤已侵犯胃、脾、结肠或邻近大血管而无淋巴结转移(T3N0);第Ⅲ、Ⅳ期分别指淋巴结和远处转移。
表22—2 UICC分期(按TNM分期法)
五、分类及分线
(一)胰腺癌的分类(日本胰腺癌处理规约)
1.上皮性肿瘤
(1)外分泌肿瘤
1)浆液性囊性肿瘤:浆液性囊腺瘤、浆液性囊腺癌。
2)黏液性囊性肿瘤:黏液性囊腺瘤、黏液性囊腺癌。
3)胰管内肿瘤:胰管内乳头状腺瘤、胰管内乳头状腺癌、原位癌。
4)浸润性导管癌:乳头状腺癌、管状腺癌(高、中、低分化)、腺鳞癌、黏液癌、未分化性胰管癌、巨细胞癌(多形细胞癌)、来源于黏液性囊腺癌、浸润性导管癌、纺锤细胞癌、来源于胰管内乳头状腺癌的浸润性导管癌。
5)腺泡细胞肿瘤:腺泡细胞腺瘤、腺泡细胞癌。
(2)内分泌肿瘤。
(3)依存肿瘤。
(4)分化不明的上皮性肿瘤。
(5)不能分类的肿瘤。
(6)其他。
(7)异形增生。
2.非上皮性肿瘤
(二)胰腺癌的分级
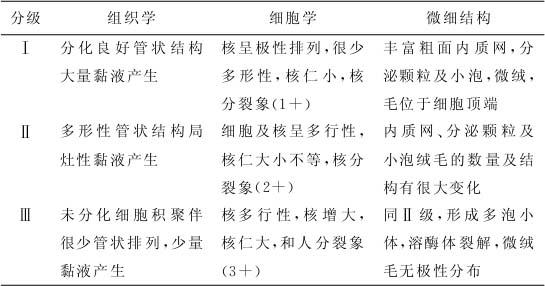
Kloppel等的分级见表22—3。
表22—3 胰腺癌的分级(Kloppel et al.1982)
六、临床表现
1.上腹部不适及隐痛是胰腺癌最常见的首发症状 肿瘤常致胰管或胆管梗阻,尽管尚未引起黄疸,但胆汁排泄不畅,胆管内压力升高,胆管及胆囊均有不同程度的扩张,患者可觉腹部不适及隐痛。以往强调胰头癌的典型症状是无痛性黄疸,实际上无痛性黄疸作为首发症状仅出现10%~30%的患者。腹痛在胰头癌患者还是很常见的症状。至于胰体尾部癌,腹痛发生率更高,且可由于累及腹腔神经丛而呈显着的上腹痛和腰背痛。这种症状的出现,常提示病变已进入晚期。
2.食欲减退和消瘦也是胰腺癌的常见表现 肿瘤常使胰液及胆汁排泄受阻,因此影响患者食欲,且有消化吸收不良,致体重明显减轻。
3.梗阻性黄疸是胰头癌的突出表现 肿瘤部位若靠近壶腹周围,黄疸可较早出现。黄疸常呈持续且进行性加深。大便色泽变淡,甚至呈陶土色。皮肤黄染呈棕色或古铜色,有皮肤瘙痒症。
4.胰头癌除致梗阻性黄疸外,亦常致胆囊肿大,可在右上腹清楚扪及。梗阻性黄疸伴胆囊肿大常提示壶腹周围肿瘤的可能。
5.晚期胰腺癌者可出现上腹固定的肿块,腹水征阳性。进一步可有恶病质及肝、肺或骨骼转移等表现。
七、转移扩散症状
胰腺由于被膜很薄,除先转移至腹膜后、胰腺周围的淋巴结外,因肿瘤位置不同而转移的区域亦不同。胰头癌常转移到幽门下及肠系膜上动脉周围淋巴结,胰体尾癌则先转移至脾门淋巴结,肝门淋巴结也并非少见。最后可广泛转移至腹腔动脉周围、胃大弯和胃小弯及腹主动脉周围淋巴结,还可转移到纵隔及锁骨上淋巴结。一级指转移到纵隔及锁骨上淋巴结,二级指转移到远离胰头部的腹腔淋巴结,三级指转移到锁骨上等远隔部位的淋巴结。
(1)血行转移:多经静脉至肝脏再转移至肺,最终可转移至骨、肾、脑、肾上腺及皮下组织等周身多数器官。
(2)直接浸润:最常侵及邻近器官。胰头癌易侵及总胆管下端、门静脉、十二指肠以及横结肠;胰体尾癌可侵犯脾静脉,导致门静脉栓塞而发生门静脉高压症;胰腺被膜受侵后,癌细胞脱落可造成腹腔内种植转移。
(3)沿神经周围转移:以胰头癌多见。由于其侵及腹腔神经丛后,沿腹膜后神经周围的淋巴管转移(实际上是淋巴转移的一种特殊方式),从而导致顽固的后背疼痛。
八、检查
1.实验室检查 血清胆红素明显升高,有时可超过342μmol/L,其中以直接胆红素升高为主。血碱性磷酸酶值升高亦很显着。尿胆红素试验呈阳性或强阳性。血淀粉酶测定,在少数早期胰腺癌,因胰管梗阻可有一过性升高;后期胰腺组织萎缩,血淀粉酶值不会有变化。胰腺癌患者可能有空腹血糖升高,糖耐量试验阳性率高。癌胚抗原(CEA)测定,约70%胰腺癌患者可升高,但亦无特异性。消化道癌相关抗原CA19—9)被认为是诊断胰腺癌的指标。
2.B超 胰腺癌的直接影像可见到低回声的肿瘤,间接的所见往往成为发现小胰癌的线索,如扩张的胰管、胆管等。除主胰管外,还要仔细观察胰管的分支。有些小胰癌可首先引起胰管分支的局限性扩张,如钩突部胰管扩张。超声内镜因超声探头仅隔胃、十二指肠壁对胰腺体尾和头部扫描,不受胃肠道气体干扰。所以,可清晰地描出胰内结构,发现早期病变。
3.CT CT可以显示胰腺肿块的正确位置、大小及其与周围血管的关系,但<2cm的胰腺肿块约1/3不能发现影像学改变。除费用昂贵的因素外,CT扫描应该列为目前诊断胰腺癌的主要方法。胰腺癌的CT图像为:①胰腺肿块呈普遍性或局限性肿块,肿块中心可有不规则的轮廓模糊的低密度区,若低密度区较大,可为肿瘤坏死或液化表现;②癌肿侵入或压迫胆管或胰管时可使其扩张;③癌肿可侵及胰背脂肪层及包绕肠系膜上血管或下腔静脉。
4.磁共振成像(MRI) MRI可显示胰腺轮廓异常,根据T1加权像的信号高低,可以判断早期局部侵犯和转移,对判断胰腺癌,尤其是局限在胰腺内的小胰癌以及有无胰周扩散和血管侵犯方面MRI优于CT扫描,是胰腺癌手术前预测的较好方法。但价格昂贵。
5.内镜逆行胰胆管造影(ERCP) ERCP能同时显示胰管、胆管和壶腹部,对不明原因的阻塞性黄疸很有价值,此外还能直接观察十二指肠乳头,并收集胰液作细胞学检查。但在已有阻塞性黄疸的情况下作ERCP有引发胆管感染的危险,应控制好注入造影剂的数量、速度和压力。
胰腺癌的ERCP影像所见为:①主胰管不规则性狭窄、梗阻,其末端呈鼠尾状截断影;②主胰管侧支破坏、断裂、稀疏和移位;③造影剂外溢入肿瘤区;④胆总管可有包绕狭窄和梗阻表现,如同时有胰管的狭窄和梗阻,则呈“双管征”。
6.胃肠钡餐检查(GI) 常见的GI对胰腺癌的诊断价值有限。在胰头癌晚期可有十二指肠圈扩大,或十二指肠呈反“3”形改变。低张GI检查使十二指肠平滑肌松弛,蠕动减少从而利于观察十二指肠黏膜的变化,如纹理紊乱、黏膜中断、壁僵硬等。
7.细胞学检查 目前多主张术前在B超或CT引导下经皮细针穿刺抽吸胰腺肿块作细胞学检查,对胰腺癌有很高的诊断价值,是一种简单、安全而有效的方法。其主要诊断作用在于晚期不能手术患者,可以明确诊断。细针穿刺细胞学检查也可以在术中应用,并可代替胰腺活检,从而避免因活检引起出血、胰瘘、急性胰腺炎等并发症发生。
九、诊断标准
(一)Moosa认为胰腺癌的诊断应具备以下几点
1.40岁以上数月至半年来呈上腹部持续性隐痛不适。
2.40岁以上既不肥胖,又无家庭史,而突然发生胰腺炎和糖尿病者。
3.间歇性上腹部和(或)腰背部隐痛不适,胃肠道钡餐检查无异常,初步排除胃肠道或肝胆疾病者。
4.原因不明的消瘦、体重减轻超过10%或呈阻塞性黄疸者,应怀疑有本病的可能,并应及早剖腹检查,以期早期诊断。部分患者在早期可以出现抑郁、忧虑等症状。
(二)胰腺癌的诊断标准
1.进行性加重的中腹部或左上腹部疼痛与闷胀,放射至腰背部。仰卧与侧卧时疼痛加重,坐位时疼痛可减轻,可有进行性梗阻性黄疸及严重消瘦等。
2.上腹深部肿块,肝脏、胆囊肿大。
3.血清癌胚抗原(CEA)检测阳性。
4.实验室和其他检查
(1)B超检查有胰头或胰尾部肿块表现。
(2)CT检查显示胰腺癌。
(3)内镜逆行胰胆管造影(ERCP)显示胰管狭窄变形、阻塞、对比剂漏出管外等。
(4)X线检查平片见有钙化;十二指肠低张造影见十二指肠圈增大,胃幽门部或十二指肠受压、狭窄、充盈缺损或胃体后壁受压移动;横结肠、空肠受压向下移位;选择性腹腔及肠系胰上动脉造影见围绕的动静脉变形及移位。
(5)75Se标记氮氨酸或67Ga胰腺扫描有占位性病变。
十、鉴别诊断
胰腺癌应与胃部疾病、黄疸型肝炎、胆石症、胆囊炎、原发性肝癌、急性胰腺炎、壶腹癌、胆囊癌等病进行鉴别。
1.各种慢性胃部疾病 胃部疾患可有腹部疼痛,但腹痛多与饮食有关,黄疸少见,利用X线钡餐检查及纤维胃镜检查不难作出鉴别。
2.黄疸型肝炎 初起两者易混淆,但肝炎有接触史,经动态观察,黄疸初起时血清转氨酶增高,黄疸多在2~3周后逐渐消退,血清碱性磷酸酶多不高。
3.胆石症、胆囊炎 腹痛呈阵发性绞痛,急性发作时常有发热和白细胞增高,黄疸多在短期内消退或有波动,无明显体重减轻。
4.原发性肝癌 常有肝炎或肝硬化病史、血清甲胎蛋白阳性,先有肝肿大,黄疸在后期出现,腹痛不因体位改变而变化,超声和放射性核素扫描可发现肝占位性病变。
5.急慢性胰腺炎 急性胰腺炎多有暴饮暴食史,病情发作急骤,血白细胞、血尿淀粉酶升高。慢性胰腺炎可以出现胰腺肿块(假囊肿)和黄疸,酷似胰腺癌,而胰腺深部癌压迫胰管也可以引起胰腺周围组织的慢性炎症。腹部X线平片发现胰腺钙化点对诊断慢性胰腺炎有帮助但有些病例经各种检查有时也难鉴别,可在剖腹探查手术中用极细穿刺针作胰腺穿刺活检,以助鉴别。
6.壶腹周围癌 壶腹周围癌比胰头癌少见,多骤然起病,也有黄疸、消瘦、皮痒、消化道出血等症状。而壶腹癌开始为息肉样突起,癌本身质地软而有弹性,故引起的黄疸常呈波动性;腹痛不显着,常并发胆囊炎,反复寒战、发热较多见。但两者鉴别仍较困难,要结合超声和CT来提高确诊率。壶腹癌的切除率在75%以上,术后5年存活率较胰头癌高。