食糖的检验
出处:按学科分类—工业技术 中国轻工业出版社《焙烤工业实用手册》第685页(17318字)
焙烤食品中用的蔗糖主要有白砂糖、赤砂糖、绵白糖等。以甘蔗、甜菜等为原料生产的白砂糖的试验方法按GB 317-1998《白砂糖》试验方法操作;绵白糖的检验按GB/T 1455.2-1991《绵白糖试验方法》操作;赤砂糖的检验按QB/T 2343.2-1997《赤砂糖试验方法》操作;麦芽糖饴(饴糖)的检验按QB/T 2347-1997《麦芽糖饴(饴糖)》试验方法操作。果葡糖浆按QB 1216-1991《果葡糖浆》及其试验方法操作。液体葡萄糖按QB/T 2319-1997《液体葡萄糖》中试验方法操作。
(一)白砂糖(GB 317-1998)和绵白糖(GB/T 1445.2-1991)检验方法
1.采样规则
(1)白砂糖抽样以堆为单位,从糖堆的四个侧面及上面共5个面抽样。上面抽中心一个点,每个侧面在其中一条对角线上按如下规定均匀抽取若干点;300t以下(含300t)为三个点;300t以上每增加100t增加一个点,也即300t以下(含300t)的糖堆每堆抽13个点;300t以上的堆抽取的点数按下式计算。

式中 m——样品质量(t),m/100取整数;
n——抽样点数,取整数。
(2)每点抽取白砂糖样品150g,每堆各点抽样混匀后作为该堆样品,若每批有多个糖堆,则各糖堆的抽样混匀后作为该批样品。
(3)抽样器以不锈钢管加工而成,抽样器、盛装容器应干净无菌。
2.感官检验
白砂糖的晶体应均匀,干燥松散,颜色洁白,无带色糖粒、糖块,绵白糖质地绵软。糖的晶体或水溶液味甜,纯正,无异臭味,无异味。
3.粒度的测定(GB 317-1998)
(1)原理:用一套试验筛将样品在一定的条件下进行筛选,将各个筛中截留的糖颗粒称量,求得留在筛网上糖颗粒的百分数对筛孔的关系。
(2)仪器、设备:
①试验筛:筛孔0.280~2.5mm一套,直径200mm。
②振筛机:其振动频率,以防止磨损糖晶体为准。
③天平:精确度为±0.1g。
(3)操作步骤:
①取样:样品按四分法进行二次分离,使二次分出的样品能满足筛分检验之用。
②筛分:称取白砂糖样品100g,准确至0.1g。将经过选择并称量的筛子,按筛孔尺寸由小到大自下而上叠装好,然后,将样品放入最上层的筛中,用盖盖好,将套筛装于振筛机上,并开动时钟或计时表,振动10min,待振动完全停止后,将筛取下,称出每一个筛子及截留糖样质量,准确到0.1g。
③计算及结果表示:计算出粒度上下限相对应孔径的两层筛之间所截留的糖样质量百分数,结果以孔径上下限及其质量百分数表示,计算结果取整数。
4.黑点的测定(GB/T 1445.2-1991)
(1)试验程序:用表面积约0.25m2的白瓷盘盛满样品,用玻璃板压平,然后在强光照耀下,检查黑点(长度大于0.2mm)的个数。
(2)计算和结果表示:
样品黑点个数(个数/m2)用下式计算:
X=黑点个数×4
5.蔗糖分的测定(GB 317-1998)
(1)在规定条件下采用以国际糖度标尺刻制读数为100°Z的检糖计,测定规定量糖样品的水溶液的旋光度。
(2)溶液的配制:称取一规定量糖样品26.000g±0.002g于干洁的小烧杯中,加蒸馏水40~50mL,使其完全溶解。移入100mL的容量瓶中,用少量蒸馏水分3~5次冲洗烧杯及玻璃棒,每次倒入洗水后,摇匀瓶内溶液,直至加蒸馏水至容量瓶量标线附近。至少放置10min使达到室温,然后加蒸馏水至容量瓶量标线下约1mm处,确保容量瓶颈部已洗净。有气泡时,可用乙醚或乙醇消除。用长嘴的滴管加水至标线,用干净的滤纸吸干容量瓶颈的内壁,将塞子塞紧,充分摇匀。
如发现混浊,用滤纸过滤,漏斗上须加表面玻璃,将最初10mL滤液弃去,收集以后的滤液50~60mL。
(3)旋光度的测定:用待测的溶液将旋光观测管至少冲洗2次,然后将溶液装满观测管,注意不使观测管内夹带空气泡。将旋光观测管置于检糖计中,目测的检糖计测定5次,读数至0.05°Z;如用自动检糖计,在测定前,应有足够的时间使仪器达到稳定。
测定旋光读数后,立即测定观测管内溶液的温度,并记录至0.1℃。
(4)计算及结果表示:测定旋光度的温度应尽可能接近20℃,一般应在15~25℃的范围。如果旋光度不是在20.0℃±0.2℃时测定的,则应校正到20℃。
白砂糖样品的蔗糖分按下面两式计算,以百分数表示,计算结果取到一位小数。
采用石英楔补偿器的检糖计:
蔗糖分=Pt[1+0.00032(t-20)]
没有石英楔补偿器的检糖计:
蔗糖分=Pt[1+0.00019(t-20)]
式中 Pt——观测旋光度读数(°Z);
t——观测Pt时糖液温度(℃)。
(5)允许误差:两次测定值之差不得超过其平均值的0.05%。
6.还原糖分的测定(GB 317-1998)
(1)原理:本法是基于碱性铜盐溶液中金属盐类的还原作用,用碘滴定法定量奥氏试剂与糖液作用生成的氧化亚铜,从而确定样品中的还原糖分。
本法各项试验条件(包括试液量、奥氏试剂量、煮沸时间、碘液耗用量及碘的反应时间等)都应严格按标准规定。
(2)试剂:
①奥氏试剂:分别称取硫酸铜(CuSO4·H2O)5.0g,酒石酸钾钠300g及无水碳酸钠(Na2CO3)10.0g,磷酸氢二钠(Na2HPO4·12H2O)50g(或无水盐19.8g),溶于900mL蒸馏水中,如有必要可将其微微加热。待完全溶解后,放入沸水浴中,加热杀菌2h,然后冷却至室温,稀释至1000mL,加入少量活性炭或硅藻土过滤,贮于棕色试剂瓶中。
②硫代硫酸钠贮备溶液:取硫代硫酸钠(Na2S2O3·5H2O)20g及无水碳酸钠0.1g(或1mol/L氢氧化钠溶液1mL),用经煮沸灭菌蒸馏水溶解,稀释至500mL,保存于棕色试剂瓶中,放置8~14d后过滤备用。
③0.032mol/L硫代硫酸钠溶液,需用时配制如下:吸取硫代硫酸钠贮备溶液100mL,移入容量瓶中并用经煮沸灭菌的蒸馏水稀释至500mL,该试剂用重铬酸钾标定,并校正其浓度。
④0.01615mol/L碘液:称取10g左右的碘化钾(无碘),先溶解于数毫升的水中,另称取纯碘2.050g,溶于碘化钾溶液,将溶液全部移入500mL容量瓶中并加水至标线,贮藏于具有玻璃塞密封的棕色瓶内。
⑤淀粉指示剂:称取可溶性淀粉1.0g,加10mL水,搅拌下注入200mL沸水中,再微沸2min,静置,取上层清液使用,溶液于使用前制备。
(3)操作步骤:称取白砂糖样本10.00g,用50mL蒸馏水溶解于300mL锥形瓶中,糖液含转化糖不超过20mg,然后加入50mL奥氏试剂,充分混合,用小烧杯盖上,在电炉上加热,使在4~5min内沸腾,并继续准确地煮沸5min(煮沸开始的时间,不是从瓶底发生气泡时算起,而是从液面上冒出大量的气泡时算起)。取出,置于冷水中冷却至室温(不要摇动)。取出,加入冰乙酸1mL,在不断摇动下,加入准确计量的碘溶液,视还原的铜量而加入5~30mL,其数量以确保碘化钾过量为准,用量杯沿锥形瓶壁加入1mol/L的盐酸15mL,立即盖上小烧杯,放置约2min,不时地摇动溶液,然后用硫代硫酸钠溶液滴定过量的碘,滴定至溶液呈黄绿色时,加入淀粉指示剂2~3mL,继续滴定至蓝色退尽为止。
(4)计算及结果表示:白砂糖样品的还原糖分按下式计算,以百分数表示,计算结果取到两位小数。

式中 A——加入碘液体积(mL);
B——滴定耗用硫代硫酸钠溶液体积(mL);
I——10g蔗糖还原作用的校正值(见表4-2-22)。
表4-2-22 以碘液实耗用量(即A-B)求毫克转化糖的校正值
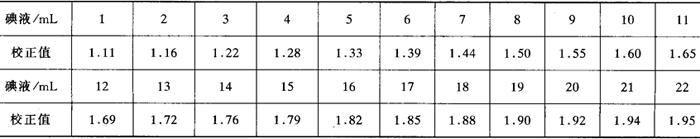
(5)允许误差:两次测定值之差不得超过其平均值的15%。
7.电导灰分的测定(GB 317-1998)
(1)原理:电导率表示离子化水溶性盐类的浓度。测定已知糖液的电导率,然后应用转换系数可算出电导灰分。电导灰分有它本身的特殊意义,不能直接与由灼烧和称量测出的质量法灰分比拟。
本标准使用的浓度为31.3g/100mL。
(2)仪器、设备:
电导率仪:应符合以下规格。
频率:低周,约140Hz。测量范围:0~300μs/cm。此范围至少应分为8个量程。测量准确度:不应大于满量的1.5%,刻度单位:μs/cm。
(3)试剂:
①蒸馏水或去离子水:精制白砂糖、优级白砂糖必须用电导率低于2μs/cm的重蒸馏水(蒸馏过2次)或去离子水。对于一级或一级以下白砂糖允许用电导率低于15μs/cm的蒸馏水。
②0.01mol/L氯化钾溶液:取分析纯等级的氯化钾,加热至500℃(呈暗红炽热)脱水30min后,称取745.5mg,溶解于1000mL容量瓶中,并加水至标线。
③0.0025mol/L氯化钾溶液:吸取0.01mol/L氯化钾溶液250mL于1000mL容量瓶内,加水稀释至标线。此溶液在20℃时的电导率为328μs/cm。
(4)操作步骤:称取白砂糖31.3g±0.1g于干洁烧杯中,加蒸馏水溶解并移入100mL容量瓶中,用蒸馏水多次冲洗烧杯及玻璃棒,洗水一并移入容量瓶中,加蒸馏水至标线,摇匀。先用样液冲洗测定电导率用的电导电极及干洁小烧杯2~3次,然后倒入样液,用电导率仪测定样液电导率,记录读数及读数时的样液温度。
电导常数应用0.0025mol/L氯化钾溶液校正计量。
(5)计算及结果表示:白砂糖样品的电导灰分按下式计算,以百分数表示,计算结果取到两位小数。
电导灰分=6×10-4(C1-0.35C2)
式中 C1——31.3g/100mL糖液在20℃时的电导率(μs/cm);
C2——溶糖用蒸馏水在20℃时的电导率(μs/cm)。
(6)温度校正:测定电导率的标准温度为20℃,若不在20℃则按下式校正,但测量温度范围一般不要超过20℃±5℃。至于溶糖用蒸馏水电导率的温度校正,因影响甚微可忽略不计。
C1=Cit[1+0.026(20t)]
式中 Cit——在t℃糖液的电导率(μs/cm);
t——测定糖液电导率时,糖液的温度(℃)。
(7)允许误差:2次测定值之差不得超过其平均值的10%。
8.干燥失重的测定(GB 317-1998)
(1)原理:采用常压烘箱干燥技术,烘干后,在统一的条件下冷却。本法主要是测定样品的“表面”水分。
(2)仪器、设备:
①干燥箱:测定过程中,离称量瓶上面2.5cm±0.5cm处的温度要保持在105℃±1℃或130℃±1℃。
②带温度计干燥器。
(3)操作步骤:将干燥箱预热至105℃(a法)或130℃(b法)。将已打开盖的干洁空称量瓶及其盖子一同放入干燥箱中,干燥30min,然后将称量瓶盖上盖子,从干燥箱中取出,放入干燥器中冷却至室温,将称量瓶称量并称取20~30g(a法)或9.5~10.5g(b法)样品(应准确至±0.1mg),样品在称量瓶中要摊平,然后将盛有样品已开盖瓶及盖子一同放入预热至105℃(a法)或130℃(b法)的干燥箱中,准确地干燥3h(a法)或18min(b法),将称量瓶盖上盖子,从干燥箱中取出,放入干燥器中冷却至室温,称量,应准确至±0.1mg。
不必干燥到恒重。但必须确保在测定的任何阶段,都不能有砂糖的有形损失。盛皿均需用干洁的坩埚夹夹拿。
注:a法为仲裁法;b法为常规法。
(4)计算及结果表示:白砂糖样品的干燥失重按下式计算,以百分数表示,计算结果取到两位小数。

式中 m1——称量瓶的质量(g);
m2——称量瓶及干燥前样品的质量(g);
m3——称量瓶及干燥后样品的质量(g)。
(5)允许误差:两次测定值之差不得超过其平均值的15%。
9.色值的测定(GB 317-1998)
(1)原理:以pH7.0缓冲溶液溶解白砂糖样品,经滤膜过滤后,在420nm波长条件下测量溶液的吸光系数,将吸光系数的数值乘以1000,即为ICUMSA色值,结果定为ICUMSA单位(IU)。
(2)仪器、设备:
①分光光度计应符合下列规格。测量范围:透过率0~100%。波长误差:在420nm处波长误差不大于±1nm。
②比色皿:厚度应选择使仪器透光度读数在20%~80%,可以使用配套的比色皿,查明配套使用的同一光径比色皿间的透光度之差不大于0.2%(在440nm波长下,用含铬量30μg/mL的重铬酸钾标准溶液进行检定)。
③阿贝折射仪应符合:折射度测量范围1.300~1.700。分划板上折射率最小分度值:0.001。糖量浓度测量范围0~95%。分划板上糖量浓度(%)最小分度值:0.5。
④pH(酸度)计:分度值或最小显示值0.02pH。
⑤滤膜过滤器:滤膜应当厚薄均匀,膜面上分布着对称、均匀、穿透性强的微孔,孔径为0.45μm,孔隙度达80%,孔道呈线性状而互不干扰,滤膜与直径150mm糖品过滤器配套使用。
(3)试剂:
①0.1mol/L盐配溶液:用吸量管吸取8.4mL浓盐酸(相对密度为1.19)于预先放有适量蒸馏水的1000mL容量瓶中,然后稀释至刻度。
②三乙醇胺-盐酸缓冲溶液:称取三乙醇胺[(HOCH2CH2)3N]14.920g,用蒸馏水溶解并定溶于1000mL容量瓶中,然后移入2000mL烧杯内,加入0.1mol/L盐酸溶液约800mL,搅拌均匀并继续用0.1mol/L盐酸调到pH7.0(用酸度计的电极浸于此溶液中测量pH)。贮于棕色玻璃瓶中。
(4)操作步骤:称取白砂糖样品100.0g于200mL烧杯中,加入三乙醇胺-盐酸缓冲溶液135mL,搅拌至完全溶解。倒入预先铺好0.45μm孔径微膜的过滤器中,在真空下抽滤,弃去最初50mL滤液,收集滤液应不少于50mL,用折射仪测定滤液的折光锤度,然后用比色皿装盛糖液,在分光光度计上用420nm波长测定其吸光度。并用经过过滤的三乙醇胺-盐酸缓冲溶液作为零点色值的参比标准。
(5)计算及结果表示:白砂糖样品的色值按下式计算,单位为IU,计算结果取整数。
国际糖色值=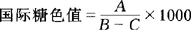 ×1000
×1000
式中 A——在420nm波长测得样液的吸光度;
B——比色皿厚度(Cm);
C——样液浓度(由改正到20℃的折光锤度乘上一系数0.9854,然后查表4-2-23求得)(g/mL)。
表4-2-23 蔗糖溶液折光锤度与每毫升含糖克数(在空气中)对照表

(6)允许误差:两次测定值之差不得超过其平均值的4%。
10.混浊度的测定(GB 317-1998)
(1)原理:当单色光透过含有悬浮粒子(混浊)的溶液时,由于悬浮粒子引起光的散射,单色光强度产生衰减,以光的衰减程度减去颜色的影响表示溶液的混浊度。
(2)仪器、设备:同本节5(2)色泽的测定。
(3)操作步骤:取待测色值的未过滤糖液,在与测定色色值相同条件下(420nm波长),测其吸光度,并按下式计算其衰减指数。

式中 A——在420nm波长测得未过滤的样液吸光度;
B——比色皿厚度(cm);
C——样液浓度(由改正至20℃的折光锤度乘上一系数0.9854然后查表求得)(g/mL)。
(4)计算及结果表示:白砂糖样品的混浊度按下式计算,单位为度,计算结果取到个数位。

式中 x1——过滤前溶液衰减指数(IU);
x2——微孔膜过滤后糖液色值指数(IU)。
注:色值指数即国际糖色值。
(5)允许误差:两次测定值之差不得超过其平均值的10%。
11.不溶于水杂质的测定(GB 317-1998)
(1)原理:用过滤孔径不大于40μm的坩埚式玻璃过滤器,上面铺一层约5mm厚经稀盐酸溶液洗涤并以水冲洗干净的玻璃丝(或与滤板相配合的紧密绒布或毛布),将糖液减压抽滤,再以较大量的蒸馏水进行减压过滤洗涤滤渣,然后干燥至恒重。
(2)仪器、设备:
①坩埚式玻璃过滤器:孔径40μm。
②干燥箱。
③带温度计干燥器。
④分析天平:精确度达±0.001g。
(3)试剂:
①1%α-萘酚乙醇溶液:称取α-萘酚1g,用95%乙醇溶解至100mL。
②浓硫酸:含硫酸95%~98%。
(4)操作步骤:称取样品500.0g于1000mL烧杯中,精制白砂糖则称取1000g于2000mL烧杯中,加入不超过40℃的蒸馏水,搅拌至完全溶解,倾入干燥至恒重的玻璃过滤器中进行减压过滤。以水充分洗涤滤渣,用α-萘酚乙醇溶液检查,至洗涤液不含糖分为止,将过滤器连同滤渣置于125~130℃的干燥器中干燥后,取出置于干燥器中,冷却至室温,进行首次称量,以后每继续烘干约30min,冷却称量一次,直至相继2次质量差不超过0.001g,可认为达到恒重,记录其质量。
微糖检验方法:取2mL洗涤液于试管中,加入数滴1%α-萘酚溶液,再沿管壁缓缓加入2mL浓硫酸。蔗糖在浓硫酸存在下与酚类起极强的呈色反应,在水与酸的界面出现紫色环,说明有蔗糖存在,若为黄绿色环说明无蔗糖存在。
(5)计算及结果表示:每千克白砂糖样品所含不溶于水杂质毫克数按下式计算,计算结果取到个数位。

式中 m1——干燥过滤器连同过滤介质质量(g);
m2——干燥过滤器连同过滤介质与不溶于水杂质质量(g);
m0——所称取白砂糖样品质量(g)。
(6)允许误差:两次测定值之差不得超过其平均值的15%。
12.二氧化硫、砷、铅的测定
参见第二章第二节。
13.微生物检验
参见第二章第三节。
14.螨的检验(GB 317-1998)
(1)原理:白砂糖中螨的检验采用漂浮法。将白砂糖溶解于蒸馏水中,镜检糖液表面的漂浮物,以确定是否有螨及螨的数目。
(2)仪器、设备:
①显微镜。
②放大镜。
③玻片。
④三角瓶(1000mL)。
(3)步骤:
①称取250g白砂糖样品,放入1000mL三角瓶中,加入不高于25℃的蒸馏水并不断搅拌,使其完全溶解,补充蒸馏水至瓶口处,以不使水溢出为止。
②用洁净的玻片盖在瓶口上,使玻片与液面接触,静置15min,取下镜检。这一操作重复若干次,以镜检所有的漂浮物。
③检出螨的数目即为250g白砂糖中的总螨数。
(二)麦芽糖饴(饴糖)(GB/T 2347-1997)和果葡糖浆(QB 1216-1991)检验方法
1.抽样方法和数量
凡在同一生产期内生产且经包装出厂的并具有同样质量证明书的产品为一批。按批取样和验收。
(1)罐装或槽车装 以罐或槽车为样本单位,从液面10cm以下抽取样品。
(2)瓶装产品 按表4-2-24抽取样本,从每箱中任取1瓶。
(3)桶装产品 根据批量(桶数)大小,按表4-2-24规定从液面10cm以下随机抽取样本。
表4-2-24 抽样量
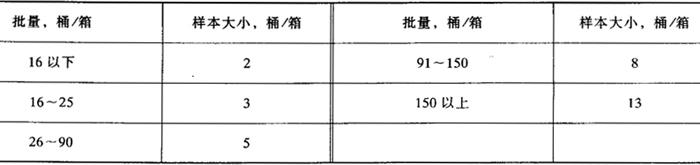
(4)从每个样本中等量取样,取样总量不得少于1kg。混匀,分装于两个洁净、干燥的具塞玻璃瓶中,签封。粘贴标签,在标签上注明产品名称、生产厂名及地址、等级、批号(罐、槽车、桶号)、取样日期及地点、取样人姓名。一瓶送化验室进行检验,另一瓶由交货方保管一个月备查。
2.感官检验
(1)色泽与外观:取样约30mL于无色洁净的样品杯(或50mL小烧杯)中,置于明亮处,用肉眼观察其色泽、透明度,并检查其有无可见杂质。
(2)香气:用嗅觉仔细鉴别样品气味。
(3)滋味:用玻璃棒取适量样品放入口中,品尝第二个样品前,必须用清水漱口。
3.干物质(固形物)
(1)仪器:
①阿贝折光仪 精度为0.0001单位;
②恒温水浴 精度为±0.1℃。
(2)试验步骤:
①将折光仪放在光线充足的位置,与恒温水浴相连。用恒温水浴将折光仪棱镜的温度调至20.0℃±0.1℃,以重蒸馏水调整折光率为1.3330。此时干物质(固形物)百分含量为零。
②打开折光仪棱镜,用脱脂棉将水拭干,加1~2滴试样于棱镜面中心,迅速闭合棱镜。使试样均匀布满棱镜面,无气泡并充满视野。
③待试样达到20.0℃±0.1℃后,通过目镜读取折光率即为干物质(固形物)百分含量。清洗并控干棱镜,将同一样品进行第二次测定。取2次测定值的算术平均值报告其结果。
4.pH
(1)仪器:
pH计(酸度计):精度±0.02。
(2)试验步骤:
①按仪器使用说明书调试和校正酸度计。
②称取样品20g于50mL小烧杯中,加入新煮沸、冷却至室温的水20mL溶解。调节样液温度及pH计的温度补偿到25℃±1℃,测定样液的pH,在1min内pH稳定,读数。先用水、再用样液冲洗电极数次,重复测定(两次测定值之差不得超过0.05pH),取算术平均值报告其结果。
5.DE值(还原糖测定法)
(1)试剂:
①次甲基蓝指示剂(10g/L):称取次甲基蓝0.5g,加水溶解并稀释至50mL。
②标准葡萄糖溶液(2g/L):准确称取于100℃±2℃烘干至恒重的基准无水葡萄糖0.5000g,加水溶解并稀释至250mL,摇匀,备用。
③费林溶液(Ⅰ Ⅱ):按GB 603-1988的规定配制与标定。
(2)试验步骤:
①样液的制备:称取一定量的样品,称准至0.0001g(取样量以每100mL样液中含有还原糖量125~200mg为宜),置于50mL小烧杯中,加热水溶解后移入250mL容量瓶中,冷却至室温,加水稀释至刻度,摇匀,备用。
②预滴定:先后吸取费林溶液Ⅱ和费林溶液Ⅰ各5.0mL于150mL锥形瓶中混匀,准确加入样液10mL和少量水。将三角瓶置于电炉上加热至沸,用样液滴定(滴加速度为10~15s加入1mL),直至溶液蓝色即将消失,加10g/L次甲基蓝指示液2滴,继续用样液滴定至蓝色消失为终点,记录消耗样液的总体积;
③正式滴定:按预滴定程序吸取费林溶液Ⅱ和费林溶液Ⅰ各5.0mL于150mL锥形瓶中混匀,加入比预滴定约少1.0mL的样液,置于电炉上加热,使其在2min内沸腾。加10g/L次甲基蓝指示液2滴,继续用样液滴定至终点。滴定全过程需在3min内完成,始终保持沸腾。
(3)计算:

式中 X——样品的DE值;
RP——1mL费林溶液(Ⅱ、Ⅰ)相当于葡萄糖的质量(g);
m——取样量(g);
250——配制样液的总体积(mL);
V——正式滴定消耗样液的体积(mL);
DMC——试样中干物质(固形物)的含量(%)。
6.熬糖温度
称取试样200g于500mL烧杯中,置于1000W电炉上(垫石棉网)。在杯中心插入一支150℃水银温度计(温度计水银头距杯底约0.5cm),加热熬煮。待沸腾后加入2滴植物油,继续加热熬煮,当杯内试样出现焦化点时,记录温度,即为熬糖温度。
7.硫酸灰分
(1)试剂:浓硫酸。
(2)仪器:
①铂坩埚(或石英坩埚、瓷坩埚):50mL;
②高温炉:525℃±25℃;
③干燥器(内装变色硅胶);
④分析天平:感量0.1mg。
(3)测定:
①坩埚先用盐酸加热煮沸洗涤,再用自来水冲洗,然后用蒸馏水漂洗干净。将洗净的坩埚置于高温炉内,在525℃±25℃下灼烧0.5h,冷却至200℃以下,取出,放入干燥器中,冷却至室温,精确称量,并重复灼烧至恒重。
称取样品2g(称准至0.0001g),置于上述恒重的坩埚中滴加浓硫酸5mL,缓缓转动,使其均匀,置于电炉上小心加热,直至全部炭化,然后,放入高温炉内,在525℃±25℃下灼烧,保持此温度直至炭化物全部消失为止(至少2h)。
取出冷却,加几滴浓硫酸润湿残留物,重新放入高温炉内焚烧,直至完全灰化,冷却至200℃左右,取出,放入干燥器中,冷却至室温,精确称量。重复灼烧至前后2次称量值之差不超过0.5mg为恒重。
②计算:
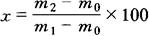
式中 x——样品的硫酸灰分,%;
m0——坩埚的质量,g;
m1——坩埚加样品质量,g;
m2——坩埚加灰分的质量,g。
8.果糖含量测定
(1)原理:在一定条件下,果糖与半胱氨酸盐酸盐——咔唑反应生成紫色物质,而在此条件下,葡萄糖呈浅蓝色。用比色法测定,选择合理的比色波长,可以减少其他糖的干扰。
(2)仪器:
①分光光度计:波长560nm。
②恒温水浴。
③具塞比色管:25mL。
④分析天平:感量0.1mg。
(3)试剂:
①70%硫酸溶液(体积分数)。
②半胱氨酸硫酸溶液:称取半胱氨酸盐酸盐(C3H7O2NS·HCl·H2O)150mg,加10mL水溶解,然后再加入70%硫酸溶液200mL。
③咔唑硫酸溶液:称取咔唑(C12H9N)12mg,加1.0mL无水乙醇溶解,然后加入70%硫酸溶液100mL。
④果糖标准溶液:取一定量的D-果糖(C6H12O6)放入真空干燥箱内,在55℃下真空干燥至恒重。迅速称取果糖300mg,用水定容至100mL,贮于冰箱内。使用时用水稀释100倍,即含果糖30μg/mL。
(4)分析步骤:
①试样制备:称取样品约1g(称准至0.0002g),用水定容至100mL,吸取1mL此液,再用水稀释定容至100mL。此时试样含果糖为25~40μg/mL。
②试样测定:取4支25mL具塞比色管,一支吸入1mL水,另一支吸入1mL果糖标准溶液,其余两支各吸入1mL试样。将比色管置于冰水浴中,分别加入4mL半胱氨酸硫酸溶液和2mL咔唑酸溶液,剧烈摇匀,置入40℃水浴中保温30min,移入冰水浴中冷却,然后置入室温水中约0.5min,于560nm波长下,用1cm比色皿测其吸光度。蒸馏水管为空白试验,以此管调节零点。取两份试样的吸光度的算术平均值进行计算。结果表示至一位小数。
(5)计算:

式中 x——样品的果糖含量[%(对固形物)];
A1——果糖标准溶液的吸光度;
A2——试样的吸光度;
m——样品的质量(g);
G——样品的固形物含量(%);
30——30μg/mL果糖标准溶液。
9.砷、铅的测定
参见第二章第二节。
10.微生物的测定
参见第二章第三节。
(三)蜂蜜的掺假的检验
1.感官检查(GB/T 5009.55-1996)
(1)在常温下呈黏稠、透明或半透明的胶状液体,温度较低时,可发生结晶现象。
(2)在液态的颜色呈浅琥珀色至深琥珀色。
(3)应具有蜜源植物特有的花香气味,味甜、无异味。
(4)肉眼观察应无死蜂、幼虫、蜡屑及其他杂质。
2.蜂蜜中酶的测定
(1)原理:蜂蜜中含有多种酶,检查蜂蜜中有无酶的存在和多少,可以鉴别蜂蜜的真假,本法是用蜂蜜中淀粉酶来作用已知的淀粉溶液,用碘液来鉴定。
(2)试剂:淀粉溶液(0.5%)。
碘液:称取1g碘、2g碘化钾加入300mL水。
(3)操作步骤:取10g蜂蜜,加入20mL蒸馏水,混合均匀后分成2份于试管中,各加入0.5%淀粉溶液1滴,一管放45℃水浴中加温1h,然后滴定碘液(相同量)于2支试管中,比较所产生的颜色。真正蜂蜜含有淀粉酶(将淀粉分解),未经加热或未十分成熟的呈淡橙绿色、淡褐色,含糊精时呈赤褐色,人工蜂蜜因不含淀粉酶,所以人工蜂蜜或加热过的蜂蜜呈深蓝色、蓝黑色。观察颜色,以加入碘液时立即呈现的色泽为准。
3.蜂蜜的掺假、掺杂的检验
用干净的木棍在桶内将中、下层搅拌均匀,先用口尝、鼻嗅、眼看,如发现不纯可做如下试验。
(1)检查蜂蜜中有无面粉或其他淀粉。取蜜2g加净水20mL,煮沸后放冷,加碘液2滴如有蓝色,绿色或呈红色,证明有淀粉存在。蜂蜜掺有淀粉时,则外观混浊,味不甜。
(2)有无掺饴糖。取蜜一份装入试管内,加净水4份,使其成稀液,然后逐渐加入乙醇(95%)。如有饴糖掺入,则呈现许多白色絮状物;否则略呈混浊或没有白色絮状物。蜂蜜中掺有饴糖,则口尝时感觉味不甜。
(3)鉴别有无蔗糖(砂糖)混入。
尝味法:纯净的蜂蜜甜度浓厚,有花香味。掺有蔗糖则甜度差,后味时间短,花香差或无花香。
观察法:蜂蜜的结晶颜色发白,结晶粒不透明,放入嘴里容易溶化,用手捻没有砂粒感。而蔗糖结晶则颜色透明,入口后不易溶化,手捻不易碎,有硬砂粒状,结晶块较坚硬。
烘干法:取样品蜜5g,放在酒精灯下,将水分蒸发干后,取下冷却,纯蜂蜜发软,而掺有蔗糖的则发硬,呈脆性。