乙型肝炎的病原学和特异性诊断
出处:按学科分类—医药、卫生 军事医学科学出版社《病毒性肝炎防治手册》第6页(6639字)
乙型肝炎是由乙型肝炎病毒(HBV)引起的传染病。1970年由Dane发现,故称为Dane颗粒。后确认此颗粒为完整病毒颗粒。据统计,全球携带乙肝表面抗原(HBsAg)者超过2.8亿。我国是乙型肝炎的高流行区,有40%~60%的人群受过HBV感染,约1亿人口为HBsAg携带者。
一、生物学性状
(一)HBV形态与结构
HBV归属嗜肝脱氧核糖核酸(DNA)病毒科。完整的HBV是双层结构的球形颗粒,直径为42nm。外壳厚7nm,由蛋白质和脂膜质组成,为病毒的包膜。内核直径28nm,为病毒的核心。核心内除含有HBV的DNA外,还含有DNA聚合酶(HBV-DNA-P)。包膜蛋白构成HBsAg,核壳蛋白构成乙肝病毒核心抗原(HBcAg)和乙肝病毒e抗原(HBeAg)。
在电镜下,乙肝病毒除Dane颗粒外,还有直径22nm的小球形颗粒和长度为20~100nm的管形颗粒。小球形颗粒及管形颗粒只具有HBsAg性质而无核心结构,即没有核酸HBcAg和HBeAg,它们不是完整的乙肝病毒,而是HBV复制过程中产生的过剩的病毒外壳。在乙肝患者或HBV感染者血清中病毒颗粒数可达1013/ml,其中完整的HBV颗粒约占1/10000,只有少数是具有全基因感染性病毒颗粒。
(二)HBV基因结构与复制
完整的HBV核酸(基因组)是由3200个左右的核苷酸环组成。环由一条长链和一条短链绞扎而成。从固定点形成一个缺口,由恒定长度的双链小分子组成的DNA称长链(又叫负链),能编码全部病毒蛋白质;比长链少15%~50%核苷酸,而长度不恒定的另一条链称短链(或叫正链)。
HBV基因组负链含有4个主要的开放读码框架(ORF),分别命名为S、C、P和X基因区。4段基因区互相有重叠现象。S区编码病毒外壳蛋白,可再分为S基因、前S1区和前S2区,S基因编码HBsAg,其上游的前S1和前S2区编码前S蛋白。C区编码HBcAg和HBeAg,其上游的一段核苷酸序列称之为前C区。X区编码X抗原(HBxAg)可能是一种转录调节蛋白。P区编码DNA聚合酶同时具有逆转录酶活性。
HBV是DNA病毒,但其复制过程有RNA逆转录病毒的特性,需要逆转录酶活性产生RNA/DNA复制中间体。HBV的逆转录特性使其RNA具有双重功能,一是作为合成DNA的模板,二是作为mRNA指导病毒蛋白的合成。
(三)HBV的稳定性
HBV在外界环境中具有较强的抵抗力,37℃60min稳定,能耐受60℃达4h,在100℃10min时感染性消失,而仍有抗原性。-20℃贮存20年以上仍具有抗原性及传染性。
总之,HBV对外界理化因素抵抗力较强,但实验室常用的煮沸消毒(10min)、高压蒸汽消毒以及160℃干烤消毒2h等措施足以将其杀灭,破坏其传染性及抗原性。
二、特异性诊断
(一)乙肝表面抗原(HBsAg)
HBsAg是机体感染HBV后最先出现的血清学指标。人感染HBV后4~7周血清中开始出现HBsAg,整个急性期中均可检出,恢复期浓度开始下降或转阴。HBsAg阳性可见于急性乙肝患者的潜伏期、急性期、慢性乙肝患者、无症状HBsAg携带者、部分肝硬变和肝癌患者的血清中和受HBV感染的肝细胞浆中。HBsAg由多肽组成,具有抗原性,本身无传染性,但由于完整的Dane颗粒也具有由HBsAg组成的脂蛋白外壳,故是HBV的感染指标之一。
HBsAg阴性是否可排除HBV感染,近几年的研究表明,HBsAg阴性并不能完全排除HBV感染,HBsAg阴性在慢性肝炎中仍有相当部分为HBV感染。HBV感染而HBsAg阴-性可能为S基因突变或HBsAg低水平表达而用常规方法难以检出所致。
HBsAg的亚型及意义:HBsAg按其抗原性分出8个亚型和2个混合型。亚型的不同可能代表乙肝病毒所穿外衣的不同。HBsAg的抗原决定簇“a”是共同的;亚型决定簇d和y,w和r互为等位基因,互相排斥。w亚型又可分为w1、w2、w3和w4。目前已发现的HBsAg亚型有ayw1、ayw2、ayw3、ayw4、ayr、adw2、adw4、adr、adyw、adyr。我国汉族以adr为主(60.28%),adw次之(34.59%);少数民族以ayw居多,ayr罕见。长江以南以adw为主,长江以北以adr多见。近年来用亚型单克隆抗体研究表明,d与y、w与r可以共同存在于同一抗原颗粒上;形成adwr、aywr、adyw或adyr等复合亚型。其形成机理有:一是不同亚型病毒的双重感染;二是单一亚型病毒感染后,有的病毒DNA可发生点突变。
HBsAg主要和共同决定簇a的免疫原性可形成不同亚型间的有效保护,但不完全,如作计划免疫,以选用本地区流行的亚型作疫苗较宜。
(二)乙肝病毒表面抗体(抗-HBs)
抗-HBs是HBsAg刺激机体产生的特异性抗体,是保护性抗体。常在乙型肝炎恢复后期、既往乙肝病毒感染和乙肝疫苗免疫后出现。血清中抗-HBs浓度越高,保护力越强,持续时间也越长(3~5年以上),再次感染乙肝病毒后,表面抗体可在2周内浓度明显升高。但也有表面抗体阳性而又发生乙型肝炎者,可能是不同亚型感染。
极少数情况下,可以同时出现HBsAg和抗-HBs阳性。这种非典型的HBV血清学标志类型是由HBV变异株引起所致,称之为HBV-2感染。其特点是单项HBsAg阳性。恢复期无抗-HBs血清标志转换;或同时在血清中检出HBsAg和抗-HBs。前者被认为是HBV-2感染HBV易感者引起,后者是HBV感染已产生抗-HBs的非易感者引起HBV-2和HBV的表面抗原有部分差异,以致于抗-HBs对HBV-2感染无保护作用。
(三)乙肝病毒核心抗原(HBcAg)和核心抗体(抗-HBc)
HBcAg存在于细胞核内,外周血中没有游离的HBcAg,HBcAg阳性常表示有Dane颗粒存在,有传染性。但目前检测方法尚不规律。
抗-HBc是乙肝病毒核心抗原的总抗体。感染乙肝病毒后最早出现的抗体是抗-HBc IgM,它是乙肝病毒急性感染的重要指标,在慢性活动性肝炎和HBsAg阳性携带者往往呈阳性。核心抗体不是中和抗体,抗-HBc IgM可持续多年,成为既往感染的指标,常用于乙型肝炎流行率的调查。抗-HBc IgM阳转或滴度增长4倍以上,表明为乙型肝炎病毒感染,可作为诊断指标。
单项抗-HBc阳性的发生率各地报道不同(0.9%~11.9%),有以下几种情况:①假阳性。②急性乙肝恢复早期,HBsAg消失而抗-HBs尚未出现的所谓“窗口期”。③自然感染若干年后,抗-HBc滴度下降无法检出而呈单项抗-HBc阳性。④抗-HBc被动转移:输用抗-HBc阳性血液制品,注射由HBV感染后出现免疫反应者血液制备的乙肝免疫球蛋白(HBIG)均可呈单项抗-HBc阳性。此外,母体抗-HBcIgG可经胎盘传给胎儿可持续一年以上。⑤远期感染伴低水平HBsAg。
区别自然免疫状态和低水平携带,具有重要临床意义。可采用以下方法:①随访观察,定期检测HBsAg及HBVDNA,如一项阳性,即为低水平携带。②采用敏感方法检测HBsAg或用PCR等检测HBV-DNA,如一项阳性,即为低水平携带。③接种乙肝疫苗:自然感染而有免疫力者2周后即见抗-HBs出现且滴度较高;如对HBV疫苗无反应,为HBsAg低水平携带者。因此,有学者提出把单项抗-HBc阳性列为疫苗接种对象。
(四)乙肝病毒e抗原(HBeAg)和e抗体(抗-HBe)
1.HBeAg的产生及性质 HBeAg是分泌型蛋白质(P15),是前C及C基因编码的P25c蛋白经酶切后产生的。HBeAg的C端经蛋白酶降解后也可产生HBeAg。
2.临床意义
①可作为急性乙型肝炎辅助诊断和预后的指标。HBeAg在乙型肝炎潜伏期的后期出现,略晚于HBsAg。进入恢复期,它随着HBsAg的消失而消失。若急性乙型肝炎发病3~4个月后HBeAg转阴,表示预后良好。
②确定乙肝患者的传染性:HBeAg大多数伴有Dane颗粒、HBVDNA、DNA聚合酶活性阳性。HBeAg阳性传染性强,抗-HBe阳性者传染性低。
③HBeAg阳性,表示HBV在体内复制。HBeAg消失前后出现抗-HBe,称为血清转换期即由复制期转为非复制期。出现抗-HBe,预示HBV繁殖终止或减弱。但有部分HBeAg阴性,血中仍有HBV颗粒,经核苷酸序列分析证明,是由于前C基因发生变异,亦可HBeAg消失而乙肝病毒持续复制,故HBeAg转阴并不能说明无传染性。抗-HBe可存在于无症状携带者及无活动性肝病患者中,但如果抗-HBe存在于慢性活动性肝炎患者中,则有可能继续发展成肝硬变。
①在血清转换期,如果用敏感方法检测HBeAg和抗-HBe,有可能二者均为阳性,但滴度均较低。
3.对HBsAg阴性而HBeAg阳性原因的分析
①检测HBsAg的方法不够灵敏。
②血清中类风湿因子(RF)的干扰。HBV各项指标均为阴性,仅HBeAg阳性者,应进一步检测RF,若为阳性,可能是RF的干扰,其血清用热聚IgG中和后HBeAg转为阴性可证实。用F(ab)段制备酶结合物,可以去除RF的干扰作用。
③HBsAg已与抗-HBs形成免疫复合物形式存在,故测不出HBsAg。
④在HBsAg消失或抗-HBs出现后,HBV仍存在于血清中,其Dane颗粒表面的HBsAg被抗-HBs所包裹,以致检测不出来。
⑤试剂盒试剂差异及操作原因,也可导致假阳性反应。
(五)前S(Pre-S)和前S抗体(Ab-Pre-S)
前S2抗原中含有多聚人血清白蛋白受体(PHSA-R)。由于肝细胞表面也有这种受体,也能和多聚人血清白蛋白(PHSA)结合,因此,乙肝病毒可以通过PHSA粘附到肝细胞表面,从而进入并感染肝细胞。故血清中前S2抗原阳性或PHSA-R阳性均说明有传染性。其抗体(Ab-Pre-S)具有清除乙肝病毒的作用,急性乙肝患者血清中出现Ab-Pre-S2常预示乙肝病毒的清除。
近年来研究发现,乙肝病毒粘附到HepG2细胞及人外周血白细胞是通过前S1抗原,故认为前S1抗原及其抗体与前S2抗原、抗体有类似的作用。
(六)乙肝病毒脱氧核糖核酸(HBV-DNA)及DNA聚合酶(DNAP)
目前应用PCR灵敏度比核酸杂交技术高100倍。同一组抗-HBe阳性的无症状病毒携带者,核酸杂交HBV-DNA阳性率仅为5%,而PCR的阳性率为73%。有活动性肝脏病理损害,但核酸杂交法阴性者,PCR的阳性率为83.7%。有的患者即使HBsAg阴性,而HBV-DNA阳性,仍可确定为HBV感染,并具有复制和传染性。
HBV DNAP是HBV核心所具有的DNA聚合酶,DNAP活性是表示HBV复制活力的最重要指标,DNAP活性越高,表明病毒复制越活跃。测定DNAP可以较灵敏地反映抗病毒药物的疗效。
(七)Dane颗粒检测
用免疫电镜技术可在乙肝患者血清中检出Dane颗粒,Dane颗粒至少有两种:高密度颗粒含HBV-DNA和HBV DNAP,称“实心”Dane颗粒;低密度颗粒无HBV-DNA和HBV DNAP,称“空心”Dane颗粒。从电镜中发现Dane,即可确定为HBV感染,也是HBV复制及传染性的直接证据。
HBV感染后血清学标志组合模式与临床意义见表2。
表2 “两对半”常见组合模式
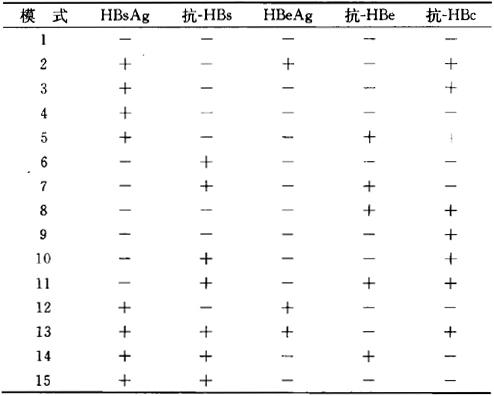
临床意义:①过去和现在未感染过乙肝病毒,即正常状态。有可能感染乙肝,可以注射乙肝疫苗进行预防。②俗称“大三阳”。表示急慢性肝炎,或提示乙肝病毒不断复制,有传染性,且很强。③感染乙肝病毒后,先出现HBsAg阳性,随后抗-HBc阳性,提示急慢性乙肝,病毒复制,有传染性;如果是“三阳”转变而来,则提示病毒复制趋于停止,传染性小。④乙肝病毒感染早期,HBeAg及抗-HBe出现在血清中,提示病毒复制,有传染性,如由“三阳”转变而来,提示病毒复制趋于停止,传染性小;或病毒核心部分与人体肝细胞核心部分整合为一体,成为病毒携带者,无传染性。⑤一般为急慢性乙肝,e抗原-抗体系统发生转换,提示病毒复制停止,或有一定程度复制,无传染性或传染性相对较小。⑥感染乙肝病毒后,病毒已清除,无传染性,且有免疫力;或注射乙肝疫苗后产生保护性抗体,从而获得免疫力。⑦感染乙肝病毒后,病毒已清除,故无复制与传染性,且有免疫力。⑧提示曾感染乙肝病毒,现病毒已清除,或有低度的复制与传染性。⑨既往感染过乙肝病毒;也可是急性乙肝的窗口期。⑩既往乙肝病毒感染,仍有免疫力;非典型恢复型,急性乙肝病毒感染。⑾急性HBV感染后康复或既往感染过HBV。⑿亚临床型或非典型性感染早期或急性乙肝早期,有较强传染性。⒀提示有新的不同亚型的再感染。⒁提示急慢性乙肝已处于恢复阶段。如过一段时间在血中仅能查到抗-HBs(+),表示对乙肝有一定免疫力。⒂可见于暴发性乙肝或慢性活动性乙肝,多同时伴有大量的抗-HBc存在,一般提示预后不佳。HBsAg和同型抗-HBs均阳性,见于免疫功能减退的乙肝患者;HBsAg和异型抗-HBs同时阳性,常见于不同亚型乙肝病毒感染。
但须指出,血清中“两对半”各标志是动态的,而不是静态的。要根据一系列动态指标进行综合分析、评判。另外,血清中“两对半”标志阳性与乙肝病情轻重程度无一定关系,有的病毒高度复制已停止,也无传染性,但乙肝病情却较重,如慢性活动性肝炎、肝硬变。这都需要根据具体情况具体分析。