主要理化因子存量和变动的有关参数
出处:按学科分类—农业科学 农业出版社《水产养殖手册》第26页(7386字)
一、海水中主要离子的浓度
表2-5 不同盐度下海水中主要离子的浓度(g/kg)

此表引自:(1)R.A.COX,and F.Culkin,Deep-Sea Res(1967)。
(2)J.P.Riley,and M.Tongudai,Chem(1967)。
(3)A·W·Morris,and J.P.Riley,Deep-Sea Res(1966)。
二、氯度比值
表2-6 海水主要成分氯度比值(S‰=35)

三、氯度与体积氯度对应值
表2-7 氯度与体积氯度对应值

四、氯度、盐度与P17.5的对应值
表2-8 氯度、盐度与P17.5的对应值

五、海水中盐类含量及其百分比
表2-9 海水中盐类含量及其百分比

六、不同氯度、盐度时的海水冰点
表2-10 不同氯度、盐度时的海水冰点

七、海水在不同盐度下最大密度时的温度
表2-11 海水在不同盐度下最大密度时的温度(℃)

八、25℃时不同氯度海水的渗透压和蒸气压下降
表2-12 25℃时不同氯度海水的渗透压和蒸气压下降

*(P°-P)/P°,式中P和P°分别为海水的蒸气压和纯水的蒸气压(P°=23.75 mmHg,25℃)。
表2-13 人工海水的密度与温度和氯度的关系

九、人工海水的密度与温度和氯度的关系
十、海水的电导率
表2-14 海水的电导率(10-3s/cm)

十一、几种典型物质的电导率(25℃)

电导率是反映水中存在电解质的程度。在淡水中为了了解矿化度的大小,应用电导法测定结果来推算淡水的矿化度,这是一种比较简便的方法。以日本河水为例:日本河水中盐分(包括非导电性SiO2)总浓度的平均值为76mg/L,电导率之平均值K(18℃)为111.5μs/cm,因此可由河水的平均电导率来推算其溶解性蒸发残渣的含量。溶解性蒸发残渣(mg/L) 0.7×K(μs/cm)。可参考:(1)南开大学化学系编写《仪器分析》(上册),人民教育出版社,338,(1978)。(2)日本分析化学会北海道分会,《水的分析》,孙铁珩等译,中国建筑工业出版社,176,(1979)。
0.7×K(μs/cm)。可参考:(1)南开大学化学系编写《仪器分析》(上册),人民教育出版社,338,(1978)。(2)日本分析化学会北海道分会,《水的分析》,孙铁珩等译,中国建筑工业出版社,176,(1979)。
十二、海水的折射率
表2-15 海水的折射率

十三、典型海水的光吸收
表2-16 典型海水的光吸收(10cm长光路消光度)

十四、氧在不同温度和氯度的海水中的饱和含量
表2-17 氧在不同温度和氯度的海水中的饱和含量表(ml/L)
〔在标准大气压下与无CO2的空气处于平衡〕

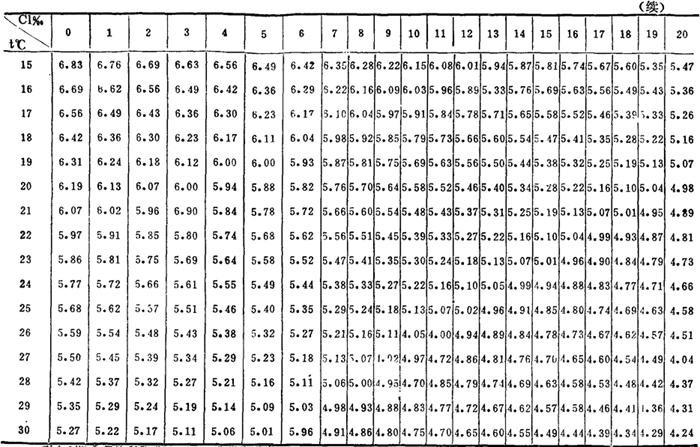
* 引自〔英〕J.P赖利G.斯基罗:《化学海洋学》.
十五、我国各海区和河口区氯度(Cl‰)与盐度(S‰)的分布
氯度:
渤海:15-17‰;黄海、东海:17-18‰;
南海:19‰以上。
海河口区:13.8‰;长江口区:8.5‰;
钱塘江口区:6.9‰;珠江口区:5.5‰。
盐度:
渤海:28-31‰;黄海,东海:31-32‰;
南海:35‰以上。
海河口区:25‰;长江口区:15.4‰;
钱塘江口区:12.4‰;珠江口区:10.0‰;
台湾沿岸:34‰以上;南沙群岛:33‰以上。

图2-2 我国沿岸各地2、8月及年平均表层盐度的地理分布的示意图
上述各海区与河口区Cl‰和S‰的地理分布,只是大致的范围。即使是沿岸海水也会受潮汐的影响,高潮时与低潮时也有一定的差异;至于河口区的海水情况就更为复杂,它不仅受潮汐效应的影响,而且也受到径流量、降雨量及蒸发量的影响,因此其变化范围也就更大。以黄河口区S‰变化为例:季节变化,春季低盐度区表层S‰最低值可达4.2‰,日平均S‰在21‰以下,高盐度区日平均S‰值在31‰以上,秋季,表层日平均S‰值在13‰以下:日变化,5月份,S‰为0.2-24.0‰,8月份,S‰为0.1-12.6‰,10月份,S‰为0.2-21.2‰。有时由于淡水过境,S‰值在2h内变化幅度,可由24.9‰,下降为4.2‰。
十六、陆地水的组成
(一)河水 大部分河流都是淡水,但也有咸水的河流。从河水的主要化学成分来看,绝大多数河流属于重碳酸盐类型,属于硫酸盐类型的河流是少数,而属氯化物类型则更少。
河水的化学组成在天然水中,可以说是最不稳定的。它最容易受到当地水文、气象条件的影响而变化。例如河水矿化度的高低与径流量的大小直接相关,洪水期与枯水期相比较就有很大的差别.河水化学组成的特点主要表现在:其一,一般河水矿化度较低;其二,生物作用对河水组成的影响较小;其三,上下分层现象不明显;其四,常含有大量有机物与悬浮物。
我国主要河流的化学成分与上述世界各地区成分相近,若以Cl-为例,世界各地区河水Cl-含量范围是4.9-12.1mg/L,而我国主要河流Cl-的含量范围是2.74-48.9mg/L,如长江(宜昌)水Cl-含量范围是9.9-33.37mg/L,黑龙江(黑河)水Cl-含量范围是2.74-3.33mg/L,黄河(龙门)水Cl-含量为48.9mg/L,松花江(哈尔滨)水Cl-含量为6.38mg/L。
表2-18 世界各地区河水化学成分平均组成(mg/L)

(二)湖水 湖水与河水相比较,不仅在化学成分上存在着一定的差异,而且在水化学动态特性上也有着明显的区别。湖水的化学组成,一般来说与补给湖泊的水源的成分有着密切的联系,显然在成因上湖水的化学成分主要决定于湖盆地带的气候、水文、土壤、地质等条件的总和。虽然说湖水大多是由注入的河流所补给,但有时它的化学成分与补给的河水化学成分差别很大。
湖泊不同于河流,它的径流较为滞缓,因此水在湖泊中停留的时间远较在河床中长。显然,在适当的气候条件下,这一情况会促使湖水的矿化度增大(由于蒸发所致)。矿化度增大的结果,也就会引起改变湖水成分的其他作用,如盐类的析出,湖水与淤泥的离子交换过程加强等。
湖水化学组成的特点主要表现在:其一,矿化度变化幅度大,可由数百毫克至数十克,例如梁子湖(湖北)矿化度为66.90-156.51mg/L,而达里湖(内蒙)含盐量可达5.56g/L;其二,径流量较小;其三,水在湖中停留时间较河水为久,受气候、生物的影响要比河水大。
表2-19 我国若干湖泊水化学成分(mg/L)

注 括弧内为CO32-的含量(mg/L)。
(三)水库水 水库常呈延伸的形状。自水库上端延向下端库底逐渐加深;同时,在水库上部保持着半河半湖的动态。按其水文化学动态来说,水库与湖泊很相似。
水库形成初期,由于森林、草地、农田、沼泽等地区被淹没,植物的枯死与腐烂以及有机物从土壤、树叶、树干之中分离出来,往往使库水含有大量的有机物质。水的矿化度的变化与水库修建所在地区有关,假如在潮湿地带,在建成初期水的矿化度将有某种程度的增大,但变化可能不很明显。但如修建在干旱地区,则水库中水的矿化度与流入的河水相比较,将会有明显的增大,尤其当水库中水的蒸发量大时则更甚。
表2-20 河南三门峡水库水的化学组成(mg/L)

(四)地下水 地下水中常溶有各种离子、分子化合物以及各种气体。常见的阳离子有H+、Na+、K+、NH4+、Mg2+、Ca2+、Fe2+等,阴离子有OH-、Cl-、SO42-、NO2-、NO3-、HCO3-、CO32-、SiO32-、PO43-等;以分子状态存在的化合物有Fe2O3、Al2O3、H2SiO3等;气体有N2、O2、CO2、CH4、H2S以及镭射气(Rn)等;另外还含有微量的Br、I、Li、F、B以及其他金属元素。
地下水化学成分的复杂性,主要取决于起源及其以后形成的过程。不同起源的地下水,其原始成分就不同。例如,在地壳中广泛分布的来自大气降水或地表水渗入的地下水,其含盐量一般就较小,并含有大气中的O2、N2等气体;而沉积水则由于经历了长期的地质历史过程,经受了不同程度的变质,因此含盐量就高,富含有硫化氢、溴、碘等物质;对于初生水一般富集了硼、氟等微量元素并富含CO2气体。
地下热水的温度要比一般地下水高。根据地下热水化学成分分析资料表明,在地下热水中含有70种以上的元素,其中包括许多稀有元素和放射性元素如Li、Sr、Rb、Cs、Ra等,而且有些元素含量甚至很高。
表2-21 山东韩庄地下水化学成分(mg/L)

十七、大气降水的组成
大气降水常溶解着各种离子。但与其他天然水相比较,其含量较低,尤其是雪水更是这样。因此,也可以说雪水在天然水中是最为纯粹的水。
表2-22 大气降水化学成分(mg/L)*

* 苏联境内大气降水的平均含量。
十八、我国河水矿化度的地理分布
我国江河水的矿化度的地理分布,由东南向西北内陆有递增的趋势。东南沿海(如闽江)矿化度仅为36.4mg/L,接近子雨水的平均矿化度。东南沿海河水矿化度一般低于50mg/L,属重碳酸盐类、钙组或纳组水,是全国河水矿化度最低的地区;而西北内陆河水的矿化度可达1000mg/L以上,是全国河水矿化度最高的地区。
十九、天然水的pH值
(一)天然水的pH值范围 对于绝大多数的天然水来说,其pH值范围一般在6.5-9.5。各类水的pH范围为:江河水:6.8-8.4;湖泊水:7.0-9.6;水库水:7.0-8.4;地下水:7.2-8.5;海水:7.5-8.4。
表2-23 不同pH值的淡水中某些弱酸间的关系

(二)pH值对鱼类的安全范围 鱼类对pH值的安全范围大致是6-9。最适范围,鲤科鱼类为7.0-8.5,鲑科鱼类在7.0左右。
pH值致死极限:高限为9.5-10,低限为4.0-5.0,均会造成鱼类的死亡。
(三)不同pH值的淡水中某些弱酸间的关系
(四)非离子态氨在不同水温、pH值时,在总氮中所占的百分比
表2-24 非离子态氨在不同水温、pH值时,在总氨中所占的百分比

二十、营养元素
含量
1.海水
NO3-N 0-600mg/m3
NH4-N 5-50mg/m3
未受污染的海水很少超过此上限。
NO2-N 0-30mg/m3
磷酸盐(P)0-60mg/m3
硅酸盐(Si) 10-30000mg/m3
2.淡水
硝酸盐的含量,一般每升为百分之几至十分之几毫克。但有时每升可达数毫克,甚至每升数十毫克。
亚硝酸盐的含量,一般低于硝酸盐的含量。在大多数的情况下,亚硝酸盐的含量每升为千分之几至百分之几毫克。但在地下水中,特别是在上部含水层中,其含量则有明显上升的趋势。在被污染的水体中,有时每升也可达十分之几毫克。在洁净水中,含量十分贫瘠,常出现零值。
铵盐的含量,一般每升不超过百分之几毫克,很少达到每升十分之几毫克。但在个别情况下,也可达每升数毫克。
磷酸盐的含量,一般为千分之几至百分之几mg/L,有时可达十分之几mg/L。在含量十分贫乏时,可出现零值。
硅酸盐的含量,在地下水中,特别在初生的地下水中,硅酸盐的含量最高,而在地表水中,由于植物的吸收,使之含量降低。一般在地表水中,其含量变化于十分之几mg/L(海水)到10mg/L(大陆水)之间。在个别情况下,其含量可达数百mg/L。
三价铁几乎只存在于地表水中,它的含量一般只有百分之几mg/L,而十分之几mg/L的情况则较少。亚铁则主要存在于地下水中(主要以重碳酸铁的形式存在),含量较高,但也很少超过1mg/L。在个别情况下,亚铁的含量可达数十至数百mg/L。
二十一、波美度(°Be′)与比重之间的换算
波美比重计有轻表和重表两种,液体比重大于1的用重表;小于1的用轻表。刻度的基准是以4℃水的比重1.000为0°Be′。
波美计读数值(n)与比重(d)的关系:
比水重的液体:

或

例如:同种海水用波美度计测得海水的波美度为3.0,求得d=1.02123,查得S‰为:27.79,但用光学盐度计测得的海水S‰为34.5。
(编者:李三庆 审者:雷衍之、黄仿元)