心动过速性心肌病
出处:按学科分类—医药、卫生 上海科学技术文献出版社《临床心律失常诊疗手册》第151页(4036字)
长期心动过速常可使心脏呈现类似心肌病的病理学改变,称之为心动过速心肌病(tachycardiomyopathy,TCMP)。心室扩张及收缩功能障碍程度随心率增减显示可逆的改变为其特征性临床表现。然而,病程过久,心脏解剖重构将难以逆转。1913年首先就1例年轻男性,由房颤快室率逐渐出现左心室扩张,并心力衰竭作过报道。至1937年,另一病例在转复窦性心律后,心力衰竭成功逆转。嗣后,类似病例相继见诸文献,已引起医学界的关注。
【发病机制】
(一) 解剖学基础
由快速性心律失常所致心肌病患者的心脏形态学主要改变为心脏四腔均呈显着扩大,其中以左室舒张期增大最为显着。Ausma(1997年)报道一组心房颤动动物模型(山羊)心房解剖的研究结果,85%(11/13只)有显着的亚细胞结构改变,包括心肌纤维缺失、糖原蓄积、线粒体形态异常、肌浆网破裂、核染色体离散,并伴肌细胞增大等表现。继后的实验动物(犬)模型研究显示,室壁厚度正常或变薄、房室扩张而心肌重量变化甚微。光镜检查示心肌结构和细胞外基质重构,前者具肌细胞数减少,细胞体积长度延伸,伴肌原纤维错位等特征;后者则表现为细胞外基质错位引起的肌小节数减少。据此提示,基底膜处心肌细胞减少、排列异常以及压力耦联更迭为导致心室扩张、室壁变薄及收缩功能障碍的主要原因。另有报道,部分患者的冠状动脉形态、功能亦有异常变化,包括心内膜和心外膜下血流比值下降、冠状动脉血流储备减退等。但迄今尚无确切证据表明,心肌缺血为心动过速性心肌病的主要原因。
(二) 分子生物学基础
分子生物学研究发现,实验动物模型所呈现的钙通道及肌原纤维钙转运异常见于心动过速后24h,并持续至心动过速终止后4周。届时,可显示肌原纤维Ca2+ATP酶及肌浆网Ca2+ATP转移酶活性降低,并肌浆网Ryanodin含量及稳定性下降等心肌细胞肌浆内钙离子转运的异常表现,使肌浆网摄取钙离子能力下降,进而导致肌浆内钙离子超载。Goett等证实心房颤动所致电重构(ERM)的过程可被维拉帕米减慢,也有助于确认异常离子流的分子生物学改变为构筑本病发病机制的基础。此外,并见本病患者伴β肾上腺素能受体密度下调,受体后腺苷酸环化酶活性改变及钙离子调节致心脏交感活性下降的报道。
(三) 电生理学基础
有资料表明,长时间的房颤可引起心房内传导延迟,窦房结结构及功能的减退。Leisla等研究指出,即使短期房颤(5min),亦可引起动物模型(猪)心房的收缩功能损害。快速心房率(尤其是房颤),复律后的“心房顿抑”(atrial stunning)现象更是快速心房率对心房收缩力所具抑制作用的有力佐证。此外,本病尚呈现线粒体结构损伤及功能紊乱,克雷布斯循环氧化酶活性增强,以及包括精氨酸、磷酸肌酸和三磷酸腺苷在内储能减少及能源利用障碍等病理生理改变。当患者处于容量负荷超载和(或)细胞因子刺激时,可继心肌收缩力的减退,出现明显充血性心力衰竭的临床表现。
【诊 断】
收缩性心力衰竭为本病特征性的临床表现,诸如重度双心室收缩功能障碍,心室充盈压升高,心输出量降低以及全血管阻力增加等。病程久暂及病情轻重需视心动过速类型、心室率以及持续时间而定。此外,尚与患者年龄及基础心脏病变有关,尤其是动脉粥样硬化病变。其时,常可因心动过速使业已减弱的心功能更趋恶化。鉴于正常心脏及病态心脏均可发生心动过速,Fenelon等建议将TCMP分为两类:Ⅰ类(单纯型):除心动过速外心脏无其他异常;Ⅱ类(不纯型)兼有其他心脏病变和(或)导致心功能恶化的因素。
心动过速心肌病可见于房颤、房扑、自律性房速、房室结折返性心动过速、房室旁道折返性心动过速等快速性室上性心律失常,以及室性快速性心律失常,后者损及心室功能较室上性为甚,尤多见于右室流出道室速及先天性室速患者。
有认为25%~50%左心室功能不全的房颤患者存在程度不等的TCMP。鉴于房颤患者的心室率每随活动的增加而递升,故仅检测其静息状态时的心率多不能用为临床观察的客观标志。患者可于休息状态下心率正常,而稍事活动后,心率迅即增速,遂诱发心动过速心肌病。因此,检测患者运动心率及24小时动态心电图多有助于TCMP诊断的建立。
频发室性期前收缩也可引发心肌病,曾见一例重度左心室收缩功能障碍年轻患者,经右室流出道病灶射频消融治疗后,左心室功能恢复正常。患者术前24小时动态心电图检获室早数高达56000次,术后24小时低于2000次。
基于上述,凡临床遇左心室收缩功能障碍伴心动过速患者,当心室率持续超逾100bpm,且于发病前心脏收缩功能正常,并能除外其他原因所致者,即须高度疑有TCMP可能。及时行超声心动图或放射性核素心室造影术有助于心脏形态及收缩功能障碍的判定。然而,快速性心律失常转复为窦性心律后,心力衰竭随之成功逆转者方为TCMP确诊之主要依据。
患者经心律失常控制后,心功能恢复程度及时间不尽一致,除与心动过速致心肌损害有关外,尚涉及患者的基础心脏病变状况。一般认为,左室功能改变多发生在心动过速终结后1个月,且恢复进程缓慢,需在6~8个月后方能达最大程度的恢复。
【治 疗】
TCMP经转复窦性心律后,不仅左心室收缩功能障碍得以改善,而且并可逆转心力衰竭的临床症状。因此,转复心律为本病主要的治疗对策,所给具体治疗方案应按心律失常类型不同而异。然而,较多资料表明TCMP尤多见于室率频速的心房颤动患者。现临床采用转复窦性心律,控制心室率以及特殊疗法为本病之主要方法。
(一) 转复窦性心律
晚近,多数学者认为,阵发性房颤以及早期易于达到节律控制的持续性房颤,尤其是不能耐受发作症状的患者,仍应优先选择节律控制治疗。
1.药物转复 通常孤立性心房颤动患者的心功能颇佳,且无确切器质性心脏病基础,故选择用为转复窦性心律的药物甚多,但临床以疗效着,不良反应少Ⅰc类中的氟卡尼(氟卡胺)及普罗帕酮为首选。晚近,有报道部分房颤患者,口服较大剂量氟卡尼300mg或普罗帕酮600mg后,约80%患者可在2h终止心房颤动发作。但患者须以适用于β受体阻滞剂治疗,且无明显器质性心脏病基础或充血性心力衰竭临床表现,为其给药指征作前提。届时,多不宜以胺碘酮为一线药物,系与该药有许多潜在性不良反应有关。然而房颤并发充血性心力衰竭时,则仅有多非利特(Dofetilide)及胺碘酮两种药物最为安全。至于Ⅰa类的奎尼丁,多项试验指示其死亡率明显高于安慰剂组,现已弃用。据此,研究显示静脉注射伊布利特(Ibutilide)及多非利特转复窦性心律的成功率为35%,可供临床选用。
2.电转复 直流同步电转复为一项安全、有效的治疗方法。通常除临床因血流动力学失代偿,严重心肌缺血或充血性心力衰竭需行紧急电转复外,一般均为择期进行。房颤反复发作者尽管可成功地实施电转复,但复发率高,故应于术前配伍抗心律失常药物治疗。现认为一次电转复的最低能量是200J,可避免低能量多次电击,若患者经体外最大能量(双相200J、单相360J)未能使之转复为窦性心律者,则可在增用伊布利特以降低房颤阈值后,再予实施电转复术,可明显提高成功率。
(二) 控制心室率
心房颤动伴室率频速者,若与严重心力衰竭或心源性休克相关,应立即直流电复律治疗,但遇患者的血流动力学仍属稳定时,则应以控制心室率为其针对性治疗。通常,临床多采用抑制房室结传导的药物,以使静息时心室率在60~80bpm,中等量运动时90~115bpm为宜。洋地黄制剂、钙通道阻滞剂(维拉帕米或地尔硫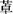 )以及β受体阻滞剂为其常用药物。钙通道阻滞剂及β受体阻滞剂尤适用于室率频速的房颤,远优于洋地黄制剂。曾有认为心房颤动经洋地黄治疗可在短期内恢复窦性心律,但研究显示,与安慰剂比较两者并无区别。现认为心房颤动并充血性心力衰竭患者,控制心室率的最佳药物选择为洋地黄或静注胺碘酮。尽管有报道房颤并中度心力衰竭患者静注地尔硫
)以及β受体阻滞剂为其常用药物。钙通道阻滞剂及β受体阻滞剂尤适用于室率频速的房颤,远优于洋地黄制剂。曾有认为心房颤动经洋地黄治疗可在短期内恢复窦性心律,但研究显示,与安慰剂比较两者并无区别。现认为心房颤动并充血性心力衰竭患者,控制心室率的最佳药物选择为洋地黄或静注胺碘酮。尽管有报道房颤并中度心力衰竭患者静注地尔硫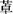 是安全有效的,但若系房颤伴预激综合征者,则洋地黄及静注钙通道阻滞剂治疗,视为禁忌之列。
是安全有效的,但若系房颤伴预激综合征者,则洋地黄及静注钙通道阻滞剂治疗,视为禁忌之列。
(三) 特殊疗法
包括心房起搏、植入式心房除颤器以及射频消融方法等,后者有肺静脉消融术、微创迷宫射频消融术以及房室结消融并植入心脏起搏器等方案。现临床对其他治疗皆难以奏效者,多植入起搏器,同时行房室结消融方法以控制心室率。术后患者心输出量增加、心功能改善、生活质量提高,但未能消除房颤及栓塞并发症,需长期抗凝治疗。