钙盐基红液燃烧工艺
出处:按学科分类—工业技术 轻工业出版社《制浆造纸手册第五分册酸法制浆》第355页(2220字)
1.镁盐基红液燃烧资料
镁盐基红液蒸发浓缩后,送红液燃烧炉燃烧。炉气中有SO2,干基浓度约为1%左右,炉尘的主要成分是MgO,经捕集后洗去可溶性钙、钠及钾盐,冉将Mg()于90℃处理3小时,消化成Mg(OH)2,再用来吸收冷却后炉气中的SO2。
(1)镁盐基回收工艺示例
镁盐基回收工艺示例见表6-7-1。
表6-7-1 镁盐回收工艺示例

(2)亚硫酸镁法苇浆红液燃烧计算示例
基数:1公斤固形物含量
红液固形物组成(元素分析):

①理论空气用量

②炉气组成、密度及露点

炉气组成:

2.钙盐基红液燃烧资料

钙盐基红液燃烧资料见表6-7-2。
表6-7-2 钙盐红液燃烧资料

3.钙基、镁基红液燃烧热分解过程中化学反应热力学的比较
在红液固形物燃烧热分解的过程中,钙基和镁基化学反应大致有以下三组主要的反应:

镁盐基红液燃烧化学反应平衡关系见图6-7-1。

图6-7-1 镁盐基红液回收平衡关系
①-MgSO4+2C=MgS+2CO2 ②-MgSO4+C=MgO+SO2+CO ③
在相同条件下,镁盐基红液热分解反应所需温度较高,在一般条件下反应不够完全,灰分在较高温度下易结焦熔结(表6-7-3)。
表6-7-3 CaSO4热分解的灰分成分分析

镁盐基、钙盐基红液中MgSO4及CaSO4热分解与空气量及温度关系见图6-7-2及图6-7-3。

图6-7-2 MgSO4分解与空气量及温度关系
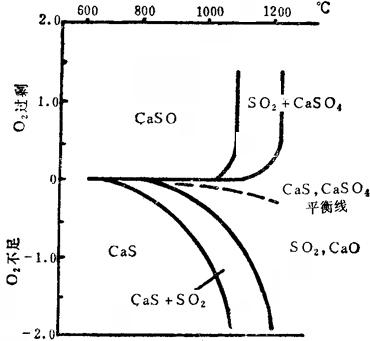
图6-7-3 CaSO4分解与空气量及温度关系
从图6-7-3、图6-7-4可以看出,MgSO4的热分解在稍有过剩空气时,可以分解为SO2+MgO,温度需在900℃以上。而CaSO4的热分解则需更高温度,例如在1200℃以上。空气不足,分解物中有H2S。如果加入二次空气,H2S可燃烧为SO2。
4.炉气中氧含量,炉温与回收率关系
炉气中氧含量(与过剩空气率有直接关系)越多,则炉气中SO3越多,实测结果见表6-7-4。
表6-7-4 炉气中O2含量与SO3形成的关系
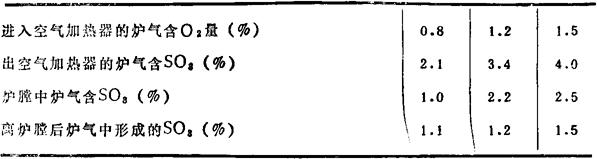
炉气中SO3的形成还与炉气温度有密切关系。锅炉各处积灰中 量与各处温度关系见表6-7-5。
量与各处温度关系见表6-7-5。
表6-7-5 锅炉各处积灰中SO4与温度关系
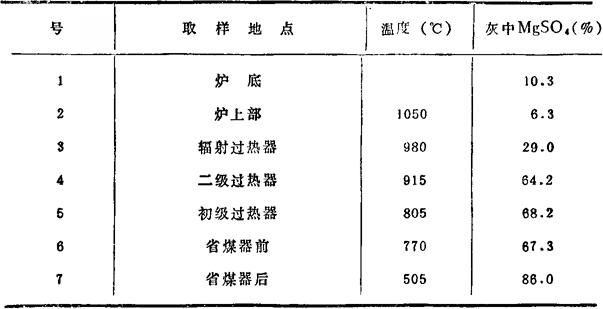
将表6-7-5数据画成曲线,见图6-7-4。图中虚线为 的化学平衡线。温度大于870℃,SO3开始分解为SO2+O2。由SO4的生成情况来看,炉温应在900℃以上。
的化学平衡线。温度大于870℃,SO3开始分解为SO2+O2。由SO4的生成情况来看,炉温应在900℃以上。
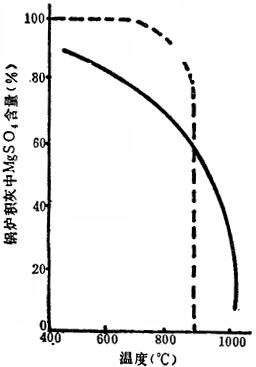
图6-7-4 锅炉积灰中MgSO4含量与温度的关系
炉气中SO3越多,说明SO2的含量减少,MgSO4生成量增多使酸回收率下降。
根据炉气分析的结果,用下式计算过剩空气率(α):

O2,CO,RO2分别表示炉气中该气体的容积%,当炉气中CO=0%,RO2+O2=21%时
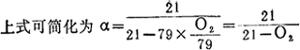
例当
