酸液中盐基含量的计算
书籍:制浆造纸工业计算手册上册
出处:按学科分类—工业技术 中国轻工业出版社《制浆造纸工业计算手册上册》第119页(837字)
【说明】对酸液中的盐基,常以它们各自的氧化物或易见形式来表示。它们的含量均可通过各自化合酸(C.A.)的含量算得。
【公式】
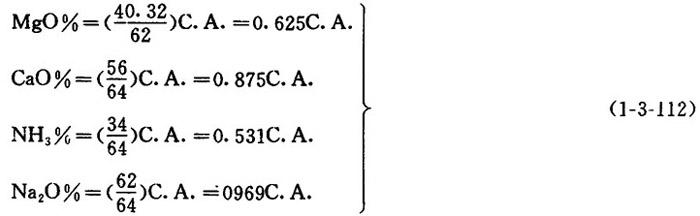
【例】已知某药槽亚硫酸盐药液中,每升药液内含有化合SO2为32克,游离SO2为1克,求:①此药液中各种酸的含量;②求各种盐基组分的含量;③判断药液的组成。
解:①化合酸含量C.A.= ×100=3.2(g/100mL)=3.2%
×100=3.2(g/100mL)=3.2%
游离酸含量F.A.= ×100=1.6(g/100mL)=1.6%
×100=1.6(g/100mL)=1.6%
总酸T.A.=C.A.+F.A.
=3.2+1.6=4.8(g/100mL)
=4.8%
②若为铵基药液,则其盐基浓度为:
NH3%=0.531C.A.=0.531×3.2%=1.70%
若为钠盐基药液,则其盐基浓度为:
Na2O%=0.969×3.2=3.10%
同理,若为镁盐时,其盐基浓度为:MgO%=0.625×3.2=2.00%
③因为C.A./F.A.=3.2/1.6>1,所以,镁盐基药液有酸式盐和正盐存在,而有可能因有沉淀而显混浊。此外,也正因如此,钙盐基不能具有这种组成的药液,否则,药液将会含有大量正盐沉淀。
上一篇:沸腾焙烧炉的计算
下一篇:制浆造纸工业计算手册上册目录