维生素B6的测定
出处:按学科分类—医药、卫生 中国科学技术出版社《食物营养分析实用手册》第155页(6249字)
方法一:维生素B6的荧光测定法
样品在硫酸存在下,加压加温水解,采用CGS树脂,用柱层析分离,以氯化钾的磷酸缓冲液洗脱。洗脱液在二氧化锰和乙醛酸钠溶液存在下,可使维生素B6一次转化为吡哆醛,它在氰化钾作用下,生成荧光物质吡哆醛氰醇衍生物。用荧光分光光度计测定之,从而计算出维生素B6的含量。
试剂
(1)0.44N硫酸溶液。
(2)0.055N硫酸溶液。
(3)6N氢氧化钾溶液。
(4)6N硫酸溶液。
(5)2M乙酸钾溶液:取2M乙酸钾溶液,以醋酸调节pH至4.0。
(6)CGS树脂(100~120目)处理:称250克CGS树脂置烧杯中,加入3N盐酸750毫升。室温下搅拌30分钟,静置过夜,弃去上清夜。再加入6N氢氧化钾500毫升,室温搅拌30分钟,静置分层后弃去上清液,水洗至中性。弃去上清液,加入3N盐酸750毫升,于沸水浴搅拌30分钟,弃去上清液,再重复用盐酸处理二次,水洗至中性,加入6N氢氧化钾溶液500毫升,室温搅拌1小时,水洗至中性,贮于pH4.0的2M乙酸钾溶液中,摇匀备用。
(7)0.01M醋酸缓冲液(pH4):称1.36克醋酸钠溶于水中并定容至1000毫升,以醋酸调节至pH4.0。
(8)0.02M醋酸缓冲液(pH5):称2.72克醋酸钠,溶于水中并定容至1000毫升,以醋酸调节至pH5.0。
(9)1.5M氯化钾-0.1M磷酸氢二钾缓冲液(pH8.0):称112g氯化钾,22.8g磷酸氢二钾,溶于水并定容至1000毫升。以醋酸调节至pH8.0。
(10)0.02M醋酸缓冲液(pH5.5):称2.72克醋酸钠,溶解于水并定容至1000毫升。以醋酸调节至pH5.5。
(11)0.05M乙醛酸钠;
(12)二氧化锰催化剂:
①饱和高锰酸钾:称25克高锰酸钾,加入250毫升水,搅拌溶解,温度维持在25℃~28℃备用。
②硫酸锰溶液:称15克硫酸锰,置200毫升90℃水中搅拌均匀。
③将②硫酸锰溶液于90℃溶解后,边搅拌边加入260毫升高锰酸钾溶液,搅拌反应15分钟,冰水冷却,以布氏漏斗过滤。用80℃热水分二次洗滤瓶,每次用100毫升,再用甲醇分二次洗涤滤瓶,每次用150毫升。过滤后于50℃烘箱烘2.5小时,然后,取出研碎,继续烘干。用100目筛过筛,贮于磨口瓶内备用。
(13)0.1M EDTA-二钠溶液。
(14)1M氰化钾溶液。
(15)硫酸奎宁溶液:称6毫克硫酸奎宁溶于100毫升0.1N硫酸溶液中。
(16)1M磷酸氢二钾溶液。
(17)5mM明矾溶液。
(18)维生素B6标准溶液。
①盐酸吡哆醛溶液(10.0微克/毫升):称盐酸吡哆醛65毫克,用0.44N硫酸溶解,并于10毫升容量瓶中用0.44N硫酸定容。取以上溶液0.469毫升置250毫升容量瓶中,以0.4N硫酸溶液定容。
②盐酸吡哆醇溶液(10微克/毫升):称盐酸吡哆醇65毫克,溶于0.44硫酸溶液中,定容于10毫升容量瓶中,取以上溶液0.468毫升,定容于250毫升容量瓶中(用0.44N硫酸定容。)
③盐酸吡哆胺溶液(10微克/毫升):称盐酸吡哆胺75毫克,溶于0.44N硫酸溶液中,定容于10毫升容量瓶中,取以上溶液0.478毫升,定容于250毫升容量瓶中(用0.44N硫酸溶液定容)。
(19)荧光分光光度计。
(20)手提式高压灭菌锅。
(21)pH酸度计。
操作步骤
1.样品液的制备:称粉碎研细样品1.00克,置150毫升三角瓶中。
取另一150毫升三角瓶,加入维生素B6标准溶液,即盐酸吡哆醛0.8毫升,盐酸吡哆醇0.8毫升和盐酸吡哆胺溶液0·8毫升。
将以上样品瓶和标准瓶中,分别加入90毫升0.44N硫酸溶液,摇匀,置高压灭菌锅中,于温度121℃,压力670KPa水解2小时(动物样品用0.055N硫酸水解5小时)。停止加热40分钟后,取出三角瓶冷却,用6N氢氧化钾调至pH4·0,定容至100毫升,过滤,滤液备用。
2.装柱:取二支1×30cm的层析柱,用经过处理的CGS树脂进行湿装柱,每支装高度为9cm,装完柱后,柱内无气泡。然后用70℃~80℃热去离子水约200毫升洗柱。用电子微量泵控制流速为5毫升/分,再用70℃~80℃的0.01M,pH4·0的醋酸缓冲液洗柱,用量约80毫升。流速同上。待冷至室温时,即可进样。
3.进样和洗脱:准确吸取10~50毫升样品液(约含维生素B61~7.5微克)进样。流速控制在0.25毫升/分)。
用pF5.0,0.02M醋酸缓冲液50毫升洗脱,洗脱流速为0.6毫升/分,最后用70℃~80℃的,pH8.0,0.1M磷酸氢二钾缓冲液洗脱。流速为0.6毫升/分。
收集约48毫升洗脱样液,置50毫升容量瓶中,用6N盐酸调节至pH5.0,定容至刻度。
准确吸取25毫升标准维生素B6水解液,过第二根柱,操作同上。
4.样液制备:分别吸取18毫升样品层析液和标准维生素B6层析液,置50毫升三角烧瓶中,各加入0.02M,pH5.5的醋酸缓冲液2毫升。5mM明矾液0.25毫升,0.05M乙醛酸钠0.7毫升,二氧化锰40毫克,将三角瓶置一小漏斗于100℃恒温水浴中不断振荡30分钟,取出冷却,过滤至25毫升比色管中,以2×1.5毫升1M磷酸氢二钾洗涤小漏斗,移入比色管中,加入0.3毫升0.1MEDTA-二钠溶液,定容至25毫升。
5.荧光性物质吡哆醛氰醇衍生物的形成:取10毫升比色管4支,分别编号。1号管加入9.0毫升上述样品液作为样品对照管。2号管加入9.0毫升样品液后,再加入0.2毫升1M氰化钾溶液作为样品反应管。
3号管加入9.0毫升上述制备的标准维生素B6溶液作为标准对照管。4号管加入9.0毫升标准维生素B6溶液,再加入0.2毫升1M氰化钾溶液,作为标准反应管。
然后将第1~4号管分别滴加6N盐酸或氢氧化钾调节pH为7.2~7.4。于50℃恒温水浴中反应90分钟,取出冷却,再滴加6N氢氧化钾调节至pH9.5后,加水稀释至刻度,摇匀,静置30分钟。
6.测定:用荧光分光光度计,以每毫升0.6微克的硫酸奎宁(以1cm石英比色皿)调节100,激发波长(λEX)=355nm,发射波长(λEM)=434nm。
分别依次取标准维生素B6或样品溶液的对照管和反应管,置1cm石英比色皿中,在波长355nm光激发下,测定434nm发射荧光强度。
7.计算:

式中:F:样品反应管的发射荧光强度;
F′.样品对照管的发射荧光强度;
F0:标准维生素B6反应管的发射荧光强度;
F′0:标准维生素B6对照管的发射荧光强度;
C:25毫升标准维生素B6比色管中的维生素B6(PL、PN、PM)之浓度(微克/毫升);
W:样品重量(克);
V:样品水解后定容体积(毫升);
V1:进层析柱的样品溶液的体积(毫升)。
方法二:维生素B6的比色测定
维生素B6与2,6-二氯醌氯亚胺反应生成蓝色靛酚,在650nm处具有最大吸收,维生素B6含量在3~8微克/毫升时,符合比尔定律。
试剂
(1)2,6一二氯醌氯亚胺溶液:称2,6-二氯醌氯亚胺40毫克溶于100毫升异丙醇中。冰箱贮存一个月,如果变成粉红色不能再用。
(2)氢氧化铵-氯化铵缓冲液:将16克氯化铵溶于70毫升水中,再加浓氨水(27%)16毫升,加水定容至100毫升。过滤后使用。
(3)标准维生素B6贮备液:称盐酸吡哆醇25毫克,溶解在250毫升0.1N盐酸中,置棕色瓶中,冰箱可保存三个月(此液为0.1毫克/毫升)。
标准维生素B6应用液:取贮备液10.0毫升,用蒸馏水定容至100毫升。(此液10微克/毫升)。
(4)4N盐酸和浓盐酸。
(5)2N氢氧化钠。
(6)异丙醇。
(7)20%醋酸钠溶液。
(8)2.5%硼酸溶液。
(9)磷酸氢二钠-柠檬酸缓冲液:称73克磷酸氢二钠(Na2HPO4·2H2O),167克柠檬酸溶于水中,稀释至1000毫升(pH3)。
(10)吸附剂:水合硅酸铝。
(11)酸化水:合0.001N盐酸。
操作步骤
1.样品液的制备:称粉碎研细的样品1克(约含维生素B630~200微克),置20毫升离心管中,加10毫升4N盐酸,置沸水浴中1小时并不时搅拌。冷却后调pH至3。加入磷酸氢二钠-柠檬酸缓冲液(pH3)3毫升。再加入2.5克吸附剂(水合硅酸铝),塞紧离心管,振荡5分钟。离心并弃去上清液。用15毫升酸化水洗涤沉淀物1次。离心弃去上清液。再加入5毫升2N氢氧化钠溶液,并加水至20毫升。剧烈振摇3分钟,使吸附剂分散呈悬浮状态,离心,吸取5毫升离心液,加入25毫升异丙醇,混合后离心,收集上清液,用浓盐酸调节pH至6(此为样品液)。
2.测定
(1)取四支带塞试管。每管加入5毫升样品液,2毫升氢氧化铵-氯化铵缓冲液。
(2)第一管加2毫升2.5%硼酸溶液。
第二、三管各加蒸馏水2毫升。
第四管中加2毫升维生素B6标准工作液。
(3)第一管中快速加入1毫升2,6-二氯醌氯亚胺溶液,混匀振摇10秒钟使其显色。加入显色剂后,准确60秒钟,立即在650nm处,调光密度为零(1cm比色皿)。
第二管快速加入1毫升2,6-二氯醌氯亚胺溶液,振摇混匀10秒钟,从加入显色剂后计算60秒钟,立即进行比色测定,记下光密度值。
第三、四管也同样处理,测定其光密度值。
3.计算
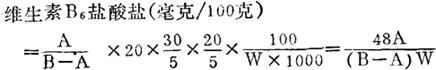
式中:A:样品液(2和3管)光密度平均值;
B:标准维生素B6工作液及样品液(4管)光密度值:
W:样品重量(克);
20:标准维生素B6盐酸盐含量(微克);
5:样品测定液的体积(毫克);
30:样品稀释液的体积(毫升);
5:用于稀释的样品液体积(毫升);
20:样品液体积(毫升);
1000:换算微克为毫克的系数;
100:换算为百分含量。