用硫酸钠和氯化钾转化法生产硫酸钾
出处:按学科分类—工业技术 中国轻工业出版社《制盐工业手册》第1682页(2273字)
在盐化工业中,硫酸镁和硫酸钠的资源都比较丰富,用硫酸钠和氯化钾配料,同样可用转化法制取硫酸钾,其工艺方法与硫酸镁、氯化钾转化法制硫酸钾的工艺极为相似。Na2SO4和KCO发生如下的复分解反应:
Na2SO4+2KCl=K2SO4+2NaCl
有关Na+,K+//Cl-,SO]--H2O体系的相平衡数据见表6-6-2,并根据表中数据绘制成图6-6-3。

图6-6-3 Na+.K+//CI-,SO42--H2O体系不同温度时的平衡图
表6-6-2 Na+,K+//Cl-,SO42--H2O体系相平衡数据
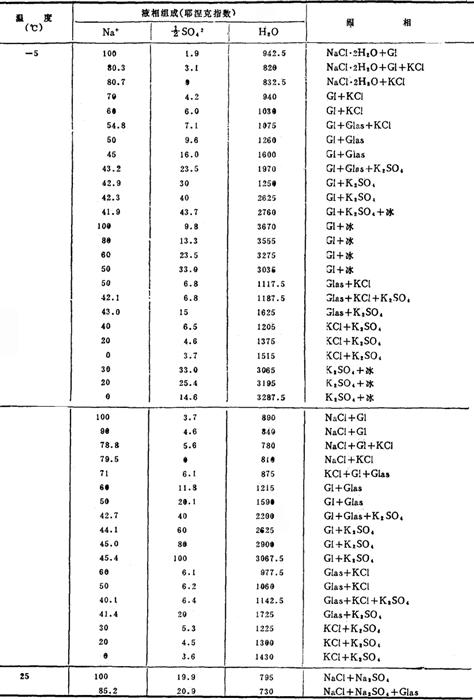
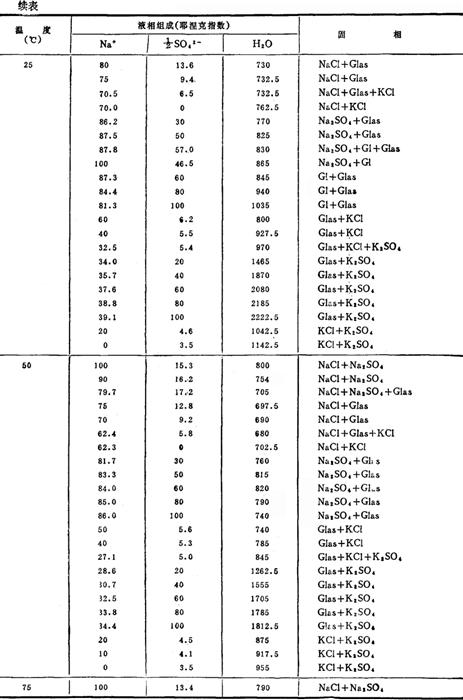
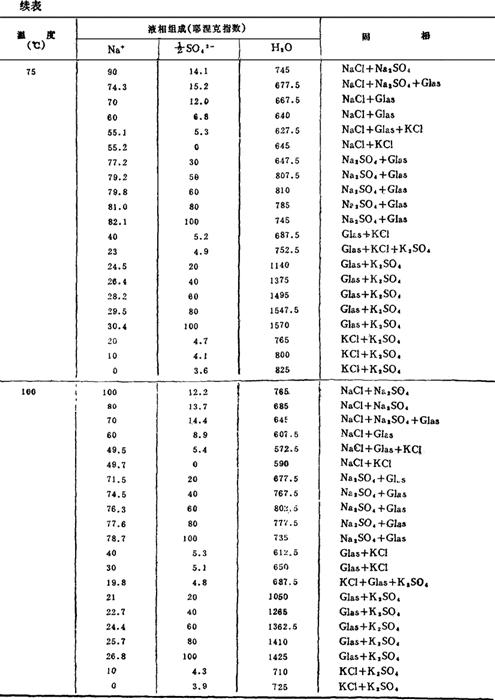
注:Gl-Na2SO4·10H2O Glas-Na2SO4·3K2SO4
(一)一段转化法
见图6-6-4。图中G点为钾芒硝Na2SO4·3K2SO4的固相点。水图中各小写字母与干盐图中各大写字母一一对应。

图6-0-4 Na+,K+//Cl-,SO42--H2O体系25℃时平衡图
(用N22SO4·10H2O和KCl配料制K2SO4的工艺分析)注:G点为Na2SO4·3K2SO4的固相点.
KCl与Na2SO4·10H2O的配料点为AB线与DM线的交点E。E点落在K2SO4的结晶区,故控制适当的加水量,使液相点为D点,使K2SO4有最大的产率。在水图上配料体系点为e点,加水后使e点升至e′点时,液相点恰到d点(干盐图上为D点),此时固相点为纯K2SC2的M点。此时K2SO4的产量可用杠杆法求得:
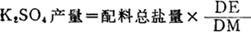
通过计算得知:
制ltK2SO4用KCl 2.96t,Na2SO4·l0H2O 2.22t,加淡水为6.16t。配料重量(kg)比如下:

K的转化率为:28.9%
随着温度的降低,钾转化率要上升,如-5℃时钾转化率为38%。
(二)二段转化法
见图6-6-4。通过中间产物Na2SO4·3K2SO4再转化成K2SO4。
第一段配料体系点为AB线与GC线交点F。为获得Na2SO4·3K2SO4最大产率,液相点应控制在C点。在水图上配料体系点为f点,加水后使f点升至f′点,此时液相点恰好为C点,固相为G点,即纯Na2SO4·3K2SO4固相点。
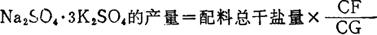
通过计算得知:
制1t Na2SO4·3K2SO4需用0.419t的KCl,1.21t的Na2SO4·10H2O、加水0.25t
配料比例(kg)

K的转化率为:80.3%
第二段转化:将第一段转化出的Na2SO4·3K2SO4再与KCl配料,加适量的水,转化平衡后可得K2SO4。Na2SO4·3K2SO4与KCl的配料体系点为AG线与DM线的交点H,在水图上为h点。当液相点达到D点时可使K2SO4得到最高产率。在水图上加水过程为使h→h′点。
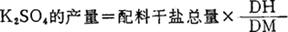
通过计算得知:
每制lt K2SO4需用0.648t KCl,用2t Na2SO4·3K2SO4加1.6t淡水。配料重量比(kg)如下:
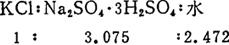
二段转化法总的结果:
每制1t K2SO4用KCl 1.48t,用Na2SO4·10H2O 2.41t,总淡水量2.1t。
K的总转化率=57.7%
二段转化法的转化温度控制在25~30℃时,钾的转化率为最大。
计算结果表明在25℃条件下,二段转化法的K转化率高于一段法,加的淡水量也明显低于一段转化。故工业生产多采用二段转化法。