容量法
出处:按学科分类—农业科学 农业出版社《土壤农化分析手册》第404页(2374字)
(一)方法要点 样品经氢氧化钾熔融分解后,在强碱性条件下,二氧化硅即转为可溶性硅酸盐,在硝酸溶液中,可溶性硅酸在过量氟离子存在下,生成氟硅酸钾沉淀。此氟硅酸钾在水中有较大的溶解度,但如果溶液中有过量的钾离子,则氟硅酸钾的溶解度即大大降低,甚至难溶于水,可过滤得纯净的氟硅酸钾沉淀。反应如下:

氟硅酸钾在水中水解,生成氢氟酸,最后以氢氧化钠滴定所生成的氢氟酸,根据消耗的氢氧化钠,即可求得二氧化硅的含量。
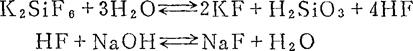
(二)试剂配制
1.浓硝酸(比重1.42,分析纯)。
2.氯化钾(分析纯固体)。
3.氢氧化钾(分析纯固体)。
4.5%中性氯化钾酒精溶液:溶解5g分析纯氯化钾于50m水中,用酒精稀释至100ml。
5.15%氟化钾溶液:将15g氟化钾(KF·2H2O)溶于水中,稀释至100ml,贮存于塑料瓶中备用。
6.1%酚酞指示剂:1%酒精溶液。
7.0.15N氢氧化钠标准溶液:称取6g化学纯NaOH溶于无CO2蒸馏水后,再用无CO2蒸馏水稀释至1L。此液必须标定,方法为:准确称取经900℃灼烧1h的分析纯二氧化硅0.0500-0.1000g,用与样品相同测定步骤进行熔融、沉淀、过滤,最后用以标定氢氧化钠准确浓度。
(三)测定步骤 称取2gKOH放入镍坩埚内,在通风橱中的四孔小电炉上加热,将水分先蒸发掉,然后开始低温熔融,使氢氧化钾逐渐熔化,待全部熔化后,逐渐加高温度,至镍坩埚内氢氧化钾成微红色,过5min后取下坩埚,冷却后,立即准确称取通过140号筛的烘干土样品0.1500g于氢氧化钾熔融物上面,再在样品上盖2-3粒固体氢氧化钾。然后放在四孔小电炉上熔融,由低温逐渐升高温度,至样品全部熔融后,加高温度至坩埚底部达暗红色(700-750℃),并保持5-10min,即可将坩埚取下。
冷却后,加少许蒸馏水使坩埚内样品熔解(切不可加热水,以免发热沸腾),并将坩埚转动几次,然后将样品倒入250ml塑料烧杯内,用少量蒸馏水洗坩埚,倒入杯内,再盖上表面皿,沿杯边迅速加入浓硝酸15ml。向坩埚内加几滴硝酸,再用少许蒸馏水分数次借助带橡皮头的塑料筷擦洗坩埚与盖子,每次用水约3ml。
向烧杯内加2-3g氯化钾,用带橡皮头的塑料筷搅拌至氯化钾全部溶解,并加蒸馏水使溶液总体积达30ml左右,冷却,加10ml15%氟化钾溶液,即形成氟硅酸钾沉淀,搅拌后放置5min。
用快速滤纸在塑料漏斗中过滤,滤液用塑料容器承接。用5%中性氯化钾酒精溶液将烧杯内剩余沉淀冲洗3次,每次约2ml,以洗净烧杯,溶液应一并倒入漏斗中,然后再用少量5%氯化钾酒精溶液洗漏斗中沉淀3次,每次都必须待滤液滤干后再进行,要求沉淀物中剩余酸越少越好。
将沉淀连同滤纸放入原塑料烧杯内,并加入10ml5%中性氯化钾酒精溶液以防沉淀水解,加酚酞指示剂5滴,用塑料筷将滤纸充分捣碎,再用0.15N氢氧化钠溶液边搅边中和滤纸和沉淀物中未洗净的酸(即滴至微红),此氢氧化钠用量不记。烧杯中加入沸水至200ml,然后将烧杯放入盛有沸水的600ml烧杯中,使氟硅酸钾沉淀充分水解,再加入酚酞指示剂5滴,用0.15N标准氢氧化钠溶液滴至微红色出现,记下消耗氢氧化钠溶液毫升数(V)。
用同样操作方法作空白试验,记下消耗标准氢氧化钠溶液毫升数(V0)。
(四)结果计算

式中:N——标准氢氧化钠当量浓度;
0.01502——每毫克当量二氧化硅的克数(即 ,硅为4价)。
,硅为4价)。
(五)注释
①加氟化钾进行沉淀时,总体积必须保持在40ml左右,体积太大其结果易偏低,太小则钾盐易析出,使结果不稳定。
②应小心将硝酸一次倒入塑料杯中,以免胶体硅酸析出。加入硝酸的酸度保持在3N以上,可以降低其他氟化物沉淀的影响(特别是铝)。
③沉淀氟硅酸钾的温度应低于30℃,夏天应在冷水中冷却。氯化钾用量通常夏天用3g,冬天用2g,用量太多易使结果不稳。
④在加入氟化钾沉淀剂后,要迅速过滤、洗涤、中和,以防氟硅酸钾沉淀水解。
⑤在滴定完毕后,溶液温度不应低于70-75℃,否则终点不易判断,致使测定结果误差太大。滴定终点为微红色,不要过深,否则引起结果偏高。
⑥称样重可根据二氧化硅的大致含量而定,见表15-2。
表15-2 根据二氧化硅含量百分数来估计称样重
