二氧化硫的吸收
出处:按学科分类—工业技术 轻工业出版社《制浆造纸手册第五分册酸法制浆》第150页(20254字)
1.概述
在有盐基存在的情况下用水吸收炉气(包括硫铁矿焙烧炉和红液燃烧炉)中的二氧化硫,以制备原亚硫酸盐溶液,根据所用盐基和二氧化硫的来源不同,采用的吸收装置也不尽相同。
高塔:多用于制备钙盐基酸液,在一些老厂改用可溶性盐基时,也可利用这种设备来制备镁、钠等盐基的酸液。有单塔和双塔两种。
低塔:系由多个(一般为四个)填料塔串联而成。多用于镁盐基酸液的制备,也可用粉状石灰石悬浊液来制备钙盐基酸液。其他盐基的酸液也可用这种设备来制备。
湍流塔:为一种效率较高的吸收装置。多用于制备镁、钠、铵等盐基的酸液。
文氏管吸收装置:由多个文氏管吸收器串联而成。多用于吸收红液燃烧炉的烟道气(SO2浓度~1%)中的SO2。用于镁、钠等盐基。
2.吸收过程的化学反应和热效应
用石灰石制备亚硫酸盐溶液时发生的反应如下:

用氧化镁制备亚硫酸盐溶液时发生的反应如下:
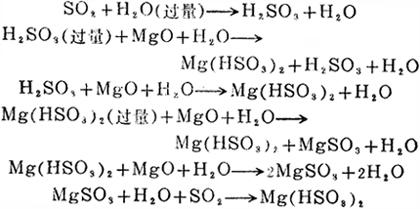
制备亚硫酸盐溶液时的化学反应热见表6-2-67,有关化合物的生成热见表6-2-68。
表6-2-67 生成亚硫酸盐溶液时的化学反应热

表6-2-68 有关化合物的生成热

一升原亚硫酸盐溶液温度升高1℃需热量1.16千卡(当原酸比重为1.035和热容量为1.120千卡/公斤·℃时)。
生成1%游离酸所产生的热量可把原酸温度提高1℃。
生成1%(以SO2计)亚硫酸氢盐(即0.5%F.A.+0.5%C.A.)所产生的热量可把原酸温度提高:

炉气温度对原酸温度的提高(假定炉气中SO2浓度为~11%,原酸中总酸浓度为4%,吸收塔出口气体温度为20℃):

3.盐基
(1)石灰石
石灰石的质量对所制成的原酸成分和纯度有很大的影响。
在采用高塔吸收装置时,石灰石不仅是盐基的来源,而目是塔的填料,使用时把不规则形状的石灰石块装入塔中,其平均直径一般在25~40厘米。但是在低塔吸收装置时,需要把石灰石粉碎成粉状,在水中制成悬浊液来使用
不管使用哪种方式,均要求石灰石具有高的化学纯度,上等石灰石应含有不少于99%的CaCO3,或55.5%CaO和不多于0.3%不溶于盐酸中的杂质,并且不应含有太多的铁和锰。
在用块状石灰石装填吸收塔时,还要求石灰石具有一定的硬度,因为松酥的和呈片状结构的石灰石,在装填吸收塔时容易破碎成小块,增加阻力、气孔率减小。上等石灰石的气孔率为0,2~1.5%;按吉列尔法测定的石灰石的有效率,即将3%的SO2水溶液同石灰石一起放置24小时所降低的浓度,好的石灰石的吉列尔有效率等于70~75%。
某亚硫酸盐制浆厂(高塔吸收装置)对石灰石质量要求如下:

(2)氧化镁
镁盐基的来源主要有:
菱镁矿经低温煅烧后所获得的氧化镁;燃烧镁盐基红液后所获得的氧化镁;在燃烧镁盐基红液时,补充硫酸镁,硫酸镁在高温下分解为二氧化硫和氧化镁:从海水中提取的氢氧化镁。
对氧化镁的质量要求除了它的化学纯度外,很重要的一点是氧化镁的化学反应活性。在煅烧菱镁矿或燃烧镁盐基红液时,高温和延长煅(燃)烧时间均会使氧化镁的化学反应活性降低。
对煅烧菱镁矿所获得的氧化镁的质量要求如下:

商品的或者回收的氧化镁应进行消化后再使用。消化的目的是:提高氧化镁的化学反应活性;减轻颗粒的沉降;减少搅拌装置的动力消耗。消化应在高的浓度(~20%)并在不断搅拌下进行,消化温度要求90~95℃,时间约2小时。消化后的浆状物用水稀释和调整到所需浓度和温度,贮存于贮槽中备用。
在有酸回收系统的工厂中,为了防止钙、钠、钾等在蒸煮液中的积累,回收的氧化镁应在真空洗涤机上进行洗涤。
4.高塔
(1)塔的结构
塔成圆柱形,直径沿塔的高度略微缩小,塔壁倾斜2°。塔的上部直径对下部直径的标准比例为0.851。在塔的下部安有木篦子以支承塔内装填的石灰石块。篦子距塔基约3~6米。在木篦的上方,塔壁开有二个掏取石灰石碎块的孔。篦子以下的地方是收容石灰石残渣的沉渣池。塔的上部安有淋洒装置、装石灰石的孔和排气管。炉气从木篦的下方进入,塔顶喷淋水或稀SO2酸。制成的原酸从沉渣室上部(进气管下方)溢流至酸液澄清槽。
塔由钢筋混凝土制成,内衬耐酸砖二层。塔可以由数个成组相结合并形成一个总体的结构。
高塔分单塔和双塔两种。单塔高为35~50米,填充高为25~40米。为了降低构筑物的高度,发展了双塔装置,也就是把单塔沿高度分成两个较低的塔,并把它们串联起来,炉气顺次通过两个塔,第一个塔为强酸塔,第二个塔为弱酸塔。在第二个塔的顶部喷淋清水,从下部流出的稀酸用泵送到第一个塔的上部喷淋。
强酸塔每天需要进行一次掏洗塔和补装石灰石。为了不中断制酸车间的工作,一般设置两个强酸塔轮换使用。弱酸塔约每周掏洗和补装石灰石一次。
双塔装置较单塔装置具有较高的生产能力,每米2塔的截面积每天产酸液150~300米3,一般在200米3左右。而单塔装置则为100~150米3/米2·日。
(2)塔的直径
塔的直径按下式决定:

式中 Q——日产酸液量,米3/日;
K——每米2塔截面积的生产能力,米3/米2·日。
(3)塔的填充高度
塔的填充高度和排出废气中SO2浓度的关系的经验式为:

式中 x——排出气体中SO2的浓度,%;
a——进塔气体中SO2的浓度,%;
H——石灰石柱的高度,米;
h——半吸收高度,米。
半吸收高度系指进入塔内SO2总量的一半被吸收的高度。半吸收高度和喷淋水的温度的关系如下:

表6-2-69 按塔的高度,炉气中SO2含量的改变情况

(4)压力降
根据工厂实测资料,当空塔中炉气速度为0.3米/秒时,每米填充高度的阻力约在3毫米水柱左右。
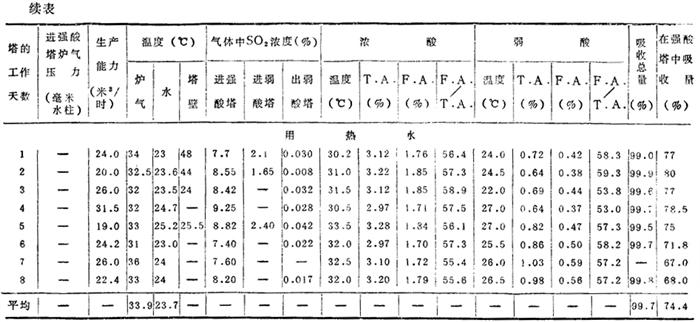
(5)双塔装置的工作特性(表6-2-72)
表6-2-70 按塔的高度酸液成分改变情况(炉气中SO2含量为10%)

表6-2-71 当改变入塔水温时原酸成分的改变

表6-2-72 双塔装置的工作特性

(6)工艺计算示例
计算依据:

塔的直径:
日产酸量:100/0.9×5=545(米3)
按每米2塔截面积产酸液量200米3/日计算,塔的直径为:

塔的填充高度:
按经验式:
上式改写为:

根据已知条件,x=0.02%;a=10%;吸收水温最高按12℃考虑,半吸收高度(h)为3.25米,代入上式:

在一个掏装塔周期中,由于石灰石被溶解而填充高度降低,为了保持预定的吸收效率,应附加20%的填充高度。
29.1×1.2=35(米)
取填充高度为36米,按双塔装置,每个塔的填充高度为18米。强酸塔设二座,以便轮换掏装清洗。
吸收过程中SO2的损失率可按下式计算:

式中 a——入塔气体中SO2浓度,10%;
x——出塔气体中SO2浓度,0.02%;
FA——原酸中游离酸浓度,2.25%;
TA——原酸中总酸浓度,3.8%。
代入上式得:

吸收过程中二氧化硫收获率为:
(100-0.188)%==99.8%
空塔速度:
塔内平均操作温度(t)30℃(303°K),塔内平均操作压力(B)为746毫米汞柱,炉气中SO2浓度(x)为10%,SO2收获率(Y)为0.998,原酸产量(Q)为22.7米3/时,总酸浓度(S)为3.8%,则在操作状态下流经吸收塔的干炉气量为:

每米3干炉气中含水蒸气:

水蒸气量:3500×0.0446=156(米3/时)
气体总量:3500+156=3656(米3/时)=1.03(米3/秒)
塔的截面积:0.785×1.872=2.74(米2)
空塔速度:1.03/2.74=0.37(米/秒),这一数值(0.37米/秒)在填料塔空塔速度的设计范围之内。关于填料塔的空塔速度见低塔部分。
原酸温度:
水温 6℃
生成真正游离酸(T.A.-2C.A.)0.7%,升温0.7×1=0.7(℃)
生成亚硫酸氢钙(2C.A.)3.1%,升温3.1×4=12.4(℃)
炉气带入热,升温 ~4(℃)
原酸温度 6+0.7+12.4+4=23.1(℃)
核算SO2的溶解度:
按公式 核算。SO2在亚硫酸氢钙溶液中的溶解度:
核算。SO2在亚硫酸氢钙溶液中的溶解度:

上述核算结果基本上满足0.7%真正游离酸的要求。
(7)淋洒器
高塔采用的淋洒器如图6-2-43,管上的喷水孔与水平成45°(可调整)夹角。它借水喷出时的反作用力而旋转,以达到均匀淋洒的目的。

图6-2-44 高塔淋洒器
1-入口横管 2-弯管 3-直管 4-玻璃球 5-喷管(4个) 6-喷头
(8)高塔装置的应用实例
国内酸法制浆厂应用高塔装置仅有两例:(1)由二座强酸塔和一座弱酸塔组成的一套典型的双塔制吸收装置,用于制备钙盐基原酸。目前三座塔均作强酸塔并联使用,其尾气在一湍流塔中用清水吸收,稀SO2水溶液泵送至强酸塔作淋洒之用。(2)由两座塔组成的单塔制装置,用于制备亚硫酸氢镁溶液。
(9)改进钙盐基原酸制备过程中的主要措施
钙盐基原酸液组成的特点是要求它含有过剩的游离酸,也就是F.A.>C.A.,游离酸在总酸中所占的比例为60%左右,因而这种酸液具有较高的SO2分压。在制备这种酸液时,为了保证良好的吸收效率和制取高游离酸含量的酸液,一般采取的措施是从提高SO2溶解的条件着手。
提高炉气中的SO2浓度:
控制沸腾焙烧炉在较低的空气过剩系数下进行燃烧,操作者常以排出的炉渣和炉灰的颜色来判断,当渣灰的颜色发红时,说明过剩空气较多,应予避免。
沸腾炉出口至风机入口是一个整体系统,大部分处于负压操作,容易漏入空气而引起炉气中SO2浓度下降,因此要使系统保持严密状态。
表6-2-73 高塔吸收装置应用实例

另外还可采用富氧空气燃烧硫铁矿的方法来提高SO2的分压。但是这种措施只能在有廉价的氧的来源时才能采用,同时要对沸腾炉的热平衡采取相应措施。
采用硫磺作为原料可以获得SO2浓度较高的炉气。
采用新的硫铁矿燃烧技术,如磁化焙烧,理论上可以获取100%SO2浓度的炉气。磁化焙烧是将硫铁矿和三氧化二铁在高温下反应生成四氧化三铁和二氧化硫,反应如下:
FeS2+16Fe2O3-→11Fe3O4+2SO2
上式生成的四氧化三铁用空气氧化成三氧化二铁,并返回参与上式反应。上述两个阶段均可在流化床反应器中完成。第二段用空气流化,而第一段则用净化后的SO2炉气进行流化。
降低吸收用水的温度:
吸收塔喷淋用水的温度一般要求在5~12℃之间。夏季如无低温地下水供应的地区,大多设置蒸汽喷射式冷冻机制取冷水。
国产Ⅲ7-DZP/85-15三效立式蒸汽喷射式冷冻机的主要性能如下:

也可以采用溴化锂吸收式冷冻机。这种冷冻机的特点是可以用低压蒸汽甚至热水作为热源。国产XS-1000溴化锂吸收式冷冻机的主要工艺特性如下:

在压力下饱和原酸:
在压力塔中用炉气饱和原酸,由于SO2分压的提高而有利于制取高游离酸含量的原酸。通常是使用耐酸压缩机把炉气压入带有惰性填料的压力塔(一般工作表压力是1公斤/厘米2)中。压力塔的计算压力(表压)为1~1.5公斤/厘米2,对日产浆250~300吨的工厂,塔径为3.0米,高12.5米。
利用液体SO2:
液体SO2是液化了的100%的亚硫酸酐。在大气压力下沸点为-10.090℃,结晶温度为-72.7℃,比导电率于0℃时为0.6×10-7欧姆-1厘米-1,即接近水的导电率。液体SO2性质见表6-2-74。
液体SO2可用槽车运入工厂。利用液体SO2来提高酸液浓度的最简便的方法是用泵(或用干的压缩空气)送入蒸煮锅中。也可以把液体SO2注入贮存有蒸煮酸或原酸的槽中,此时,应使SO2均匀地、不剧烈地进入槽中,并且很好地与酸液混合。
5.低塔
低塔吸收装置在我国被广泛地用于酸性亚硫酸氢钙和亚硫酸氢镁酸液的制备。前者用粉状石灰石悬浊液作为吸收剂,后者则用氧化镁悬浊液。
(1)塔的结构
低塔吸收装置系由多个(一般为4个,有的工厂也有用5~6个)填料塔串联。塔用钢板焊接而成,内衬耐砖。在靠近筒体的下部有木制篦子以支承上部的填料。下锥部为集液槽。每个塔均附有循环泵,泵的容量取决于所需的淋洒密度。
炉气从第一个塔进入,并顺序经过所有串联的塔而排入大气。氧化镁(或石灰石粉)悬浊液则从最后一个塔的循环泵入口加入,并顺序溢流到前一个塔,制成的原酸从第一个塔排出。
(2)塔的直径
塔的直径取决于塔的操作气速。填料塔的空塔速度,有的认为其值低者可在0.2~0.3米/秒,高者可达1~1.5米/秒。一般都控制在0.6~1.0米/秒之间,设计时可选用0.6~0.8米/秒。
在确定了空塔速度后,塔的直径可按下式计算:
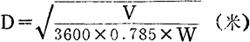
式中 V——操作状态下的处理气量,米3/时;
W——空塔速度,米/秒。
(3)塔的填充高度
可按下述顺序确定塔的填充高度。
传质面积的计算采用平均推动力方法:

式中 G——需要吸收的SO2量,公斤/时;
K——吸收速度系数,公斤/米2·时·大气压;
ΔP——平均吸收推动力,大气压。
平均吸收推动力按下式确定:
表6-2-74 液体SO2的性质



式中  ——吸收过程始末被吸收气体中SO2的分压,毫米汞柱;
——吸收过程始末被吸收气体中SO2的分压,毫米汞柱;
 ——吸收过程始末液面上SO2的平衡压力,毫米汞柱。
——吸收过程始末液面上SO2的平衡压力,毫米汞柱。
在确定传质面积后,可根据所选用的填料性质计算填料层的高度(H)。
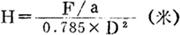
式中 F——传质面积,米2;
a——填料的比表面,米2/米3;
D——塔的内径,米。
总的填料高度H可平均分配于每台吸收塔,因此单台塔的填料高度为:
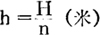
式中 n——塔的串联台数。
决定塔直径的主要因素是生产能力和压力降,而塔的效率或传质能力则取决于填料层的高度。为了使淋洒的液体在整个塔截面分布均匀,必须保证一定的填料高度,其关系以h/D表示。一般填料塔以h/D=1.5~2为下限,但避免h/D>5。
(4)填料层的阻力
经液体淋洒后的湿填料层的阻力可用下式计算:
ΔP=ΔP干(1+aL)(毫米水柱/米填料)
式中 ΔP干——干填料阻力,毫米水柱/米填料,见图5-2-45~46;
a——校正系数;
L——淋洒密度,米3/米2·小时。

图6-2-45 块状干填料阻力
1-中性长石,42.6毫米 2-焦炭,42.6毫米 3-焦炭,40.6毫米 4--焦炭,26.6毫米 5-焦炭,24.4毫米 6-卵石,42毫米

图6-2-46 环状干填料阻力
1-陶瓷环,Φ50×50毫米,管式排列 2-陶瓷环,Φ50×50毫米,交错排列 3-钢环,Φ50×50毫米,堆放 4-陶瓷环,Φ50×50毫米,堆放 5-陶瓷环,Φ35×35×4毫米,堆放 6-陶瓷环,Φ25×25×3毫米,堆放 7-陶瓷环,Φ15×15×2毫米,堆放 8-瓷环,Φ8×8×1.5毫米,堆放
(5)低塔吸收装置特性(表6-2-75)
表6-2-75 低塔吸收装置的特性


(6)填料的特性
制取钙、镁盐基的亚硫酸盐溶液时,常采用普通瓷环作为吸收塔的填料,因为瓷环易被沉淀物堵塞。但是当用这种填料塔来制备钠,铵盐基的亚硫酸盐溶液时,就可以选择高效的填料。有关填料的特性资料如下:
填料基本特性数据在缺乏资料时可按下列近似公式计算。
填料的数量:
塔径较填料直径大十倍以上,填料的高和直径相等时,单位体积内填料的数量可按下式计算:
nd3=K
式中 n——每米3填料的数量,个/米3;
d——填料的外径,米:
K——常数。对于普通瓷环:堆放时取0.77;整放时采用三角形排列取1.15,采用正方形排列取1.00。马鞍瓷环、槽鞍瓷环:堆放时取1.21。
比表面:
单位体积的填料中,填料的表面积称为比表面。
a=na0(米2/米3)
式中 a——比表面,米2/米3;
a。——一个填料的表面积,米2/个:
n——每米3体积内填料个数。
计算普通瓷环比表面的近似式:
a=2nπ(d2-δ2)(米2/米3)
堆放时的近似公式:
a=4.8/d(米2/米3)
整放时采用三角形排列的近似公式:
a=7.15/d(米2/米3)
整放时采用正方形排列的近似公式:
a=6.2/d(米2/米3)
式中 d——瓷环的外径,米;
δ——瓷环的厚度,米。
空隙率:
空隙率系指填料呈干燥状态时,塔内净空间所占的百分率。
ε=1-nv。
式中 ε——空隙率;
n——填料数量,个/米3;
v。——一个填料的材料体积,米3。
操作时由于填料壁上附有液体层,故实际空隙率要小于上述干空隙率。
干填料因子:
干填料因子a/ε3米-1是表示填料流体力学特性的数群。
有关普通瓷环的特性列于表6-2-76。
表6-2-76 普通瓷环的特性(根据公式的计算值)

(7)工艺计算示例
计算依据:
采用亚硫酸氢镁法。

炉气量:
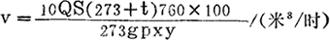
式中 Q(原酸产量)=600/24=25米3/时;
S(原酸中T.A.)=4.0%
t(炉气温度)=60℃
P(炉气压力)=760毫米汞柱(当地大气压740毫米汞柱,假设塔的阻力为270毫米水柱,约等于20毫米汞柱)
g(标准状态下,1米3SO2的重量)=2.9269公斤
x(炉气中SO2含量)=10%容积
y(SO2吸收得率)=0.995

每米3干炉气中含水蒸气:

水蒸气量:4170×0.292=1215(米3)
总气体量:
塔的直径:
选取空塔速度为0.8米/秒,塔截面积:
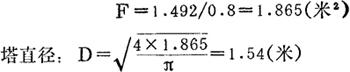
平均推动力:假定整个装置的阻力为20毫米汞柱,当地大气压为740毫米汞柱。
进塔气体中SO2分压
出塔气体中SO2分压
进塔液体的SO2平衡压力 毫米汞柱
毫米汞柱
出塔液体的SO2平衡压力 毫米汞柱(假定酸液温度为50℃,查图6-2-42)
毫米汞柱(假定酸液温度为50℃,查图6-2-42)

每小时吸收的SO2量:G=25×4.0×10=1000公斤/时
取吸收速度系数K=30公斤/米2·时·大气压。
所需传质面积F:
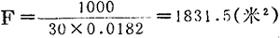
填料体积:选用Φ100×100毫米的普通瓷环,采用三角形整放,比表面积为71米2/米3。
1831.5/71=25.8(米3)
填料层高度:25.8/1.865=13.83(米)
采用四塔串联,每个塔的填料层高度:
13.83/4=3.5(米)
h/D=3.5/1.54=2.27。根据填料塔设计要求h/D不低于1.5而不高于5。
淋洒密度:一般在20~25米3/米2·时。现按25米3/米2·时计算循环泵容量:
25×1.865=42(米3/时)
(8)亚硫酸氢镁溶液制备过程中的主要工艺参数
亚硫酸氢镁溶液组成的特点是没有过剩的游离酸,因此C.A.≥F.A.,所以这种溶液界面上SO2的平衡压力很低,能够利用低浓度SO2炉气(如红液燃烧炉的炉气)来制备这种酸液。化学反应速度是制备这种酸液时的主要控制方面。用氧化镁悬浊液吸收SO2的资料列于表6-2-77。
表6-2-77 用氧化镁悬浊液吸收SO2时,主要工艺参数的影响

适当提高温度,有利于加快化学反应速度而改善吸收状况,工厂中一般控制成品酸液的温度在60℃左右。
提高酸液中C.A/F.A的比值大于1能显着改善吸收状况。但必须避免过大而引起MgSO3析出,造成堵塔。
使用具有良好活性的氧化镁(主要是在较低温度与较短时间内烧成的纯度较高的氧化镁)。
可以适当地加大淋洒密度来改善吸收状况。
6.湍流塔
湍流塔的特点是在塔内栅板上放置一定数量的轻质球,在高速气流、淋洒液和自身重力的作用下,作剧烈的旋转和翻腾,形成气、液、固三相湍流运动和搅拌作用,从而引起气液两相良好的接触。国内一些新建的亚硫酸盐法制浆厂已采用湍流塔制备亚硫酸氢镁溶液。湍流塔也可用于沸腾炉炉气的除尘和洗涤。
(1)塔的参数
湍流塔的空塔气流速度一般选用2.5~6米/秒,它与静止床层高度、淋洒液量有关。
用于炉气除尘和洗涤时,空塔速度可取2.5~3米/秒;用于吸收时可在3~5米/秒之间选择。
静止床层高度H0与塔径D的关系,当H0/D>1时,发生活塞流动和沟流现象。
静止床高度一般为湍动区高度的20~40%,如大于50%则失去湍动的特性。
填料过少,则效率下降。但填料过多,对效率影响不大,但阻力显着增加。
湍流塔对液体的淋洒密度要求不严,在较大范围内变动时均能保持良好的效率。用于炉气净化时,其淋洒密度可取35~40米3/米2·时;用于吸收时可根据相平衡选取适合的淋洒量。
搁球用的筛板可做成栅条形、多孔形或网形,其自由截面最好在45~60%。栅条间距或钻孔直径不应大于小球直径的2/3,以免被损坏的小球卡位。为了减少压力降,栅条的高度最好不大于筛条间距的1/2。拦球用筛板同搁球筛板,开孔率至少不小于搁球筛板。
当气体的空塔速度为2~5米/秒、淋洒密度大于25米3/米2·时时,静止床层高度H0与床层膨胀高度He之间的关系以下式表示:

式中 w——空塔速度,米/秒;
L——淋洒密度,米3/米2·时;
K——系数0.045~0。08,一般取0.06。
一般情况下,应使床层的膨胀高度不超过1000毫米。
筛板间距,即接触区高度HK一般选取1000~1500毫米。空塔速度高时取其上限,低时取其下限。HK大致为1.25He或2.5~5H0。
(2)小球的选取
塔径D和球径d的比值D/d最好大于10。当塔径D≥200毫米时可选用Φ38、Φ30、Φ25毫米的小球:当塔径<200毫米时,可选用Φ20、Φ15毫米的小球。
小球的比重应小于气液混合物的比重才有利于湍动,一般在0.15~0.65之间,
小球的材料取决于操作条件,要求耐磨、耐腐蚀、耐温、耐压。赛璐珞球易裂,目前都用聚乙烯或聚丙烯制小球。聚乙烯球的使用温度应在110℃以下,长期操作条件最好低于70~80℃,其寿命约6个月。国外有用不锈钢、铝或玻璃钢及其他新型材料做的薄壳球。
表6-2-78 国产塑料小球的特性

(3)小球填充数
小球填充数可按下式求取:

式中 N——球数,个;
D——塔直径,毫米;
H0——静止床层高度,毫米:
ε——静止床层平均空隙率,当D/d>12时取ε=0.4;
D/d≤12时取ε=0.45;
d——球直径,毫米。
(4)塔的段数
塔的段数取决于气-液-固三相湍动的程度、工艺上的要求和传质推动力。对有化学反应的吸收操作,还要保证有足够的反应时间。对于制备亚硫酸氢镁酸液的吸收塔,一般采用四段;对于炉气净化则用二段就够了。
(5)压力降
一般情况下,每段的压力降为40~120毫米水柱。
当未淋洒液体时,可按气-固系统流化床阻力计算方法。

式中 G——球体总重,公斤;
F——塔截面积,米2;
H0——静止床层高度,米;
γ——小球重度,公斤/米3:
γg——气体重度,公斤/米3;
ε——空隙率,%。
当淋洒密度小于20米3/米2·时,可按下式计算压力降:
ΔP=H0(2.92v1/8、d-2/3L1/3γL+γK-γg)×(1-ε)(毫米水柱)
式中 H0——静止床层高度,米;
v——液体运动粘度,米2/秒;
d——球直径,米;
L——淋洒密度,米3/米2·时;
γL——液体密度,公斤/米3;
γ——球体重度,公斤/米3;
γg——气体重度,公斤/米3;
ε——空隙率,%。
淋洒密度大于25米3/米2·时,压力降计算公式为:
ΔP=Aw0.8L0.44(毫米水柱)
式中 L——淋洒密度,米3/米2·时;
W——空塔速度,米/秒;
A——系数。
系数A与静止床层高度H0的关系如下:

(6)临界气速

图6-2-47 静止床层高度和淋洒密度与压力降的关系
静止床层高度(毫米):
1-800 2-700 3-500 4-450 5-300
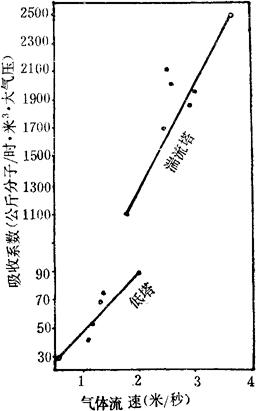
图6-2-48 湍流塔和低塔吸收系数的比较
当无淋洒液时,球体从静止状态转为运动状态所需的最低气速称为无淋洒的临界气速。
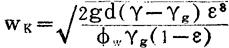
式中 wK——无淋洒时临界气速,米/秒;
d——球直径,米;
γg——气体重度,公斤/米3;
γ——球重度,公斤/米3;
ε——静止床层的空隙率;
g——重力加速度,9.81米/秒2;
ΦW——阻力系数,见表5-2-79。
表6-2-79 塑料球比重与压力降的关系
当向床层淋洒液体时,由于三相流化时运动的复杂性,尚无三相流化时临界气速的计算公式。在实际应用中可根据无淋洒时临界气速来确定操作气速:
W=AwK
式中 W——操作气速,米/秒;
wK——无淋洒时的临界气速,米/秒;
A——系数,1.5~3.0,对于淋洒量大者取小值。
表6-2-80 阻力系数ΦW

(7)湍流塔的特点
湍流塔结构简单,空塔速度可达3~5米/秒,因此设备小,投资省,占地面积小,效率高。当制备亚硫酸氢镁溶液时,湍流塔和普通低塔的比较数据列于表6-2-81。
表6-2-81 湍流塔和低塔的比较
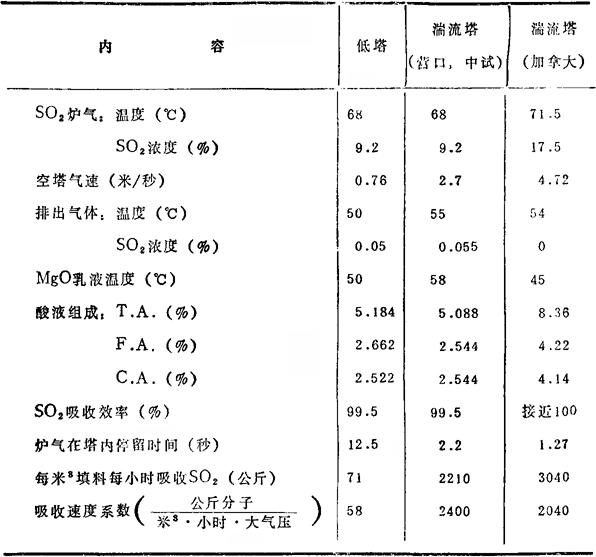
湍流塔气、液、固三相经常处于运动状态,因此不象低塔那样容易为物料堵塞,因此塔压比较稳定。
维修量小,除更换小球外,几乎没有其他故障。
用于吸收SO2以制取亚硫酸氢镁酸液的湍流塔的特性列于表6-2-82。
表6-2-82 湍流塔的运行特征


(8)工艺计算示例
计算依据见低塔部分。
炉气量5385米3/时,或1.492米3/秒,计算见低塔部分。
选取空塔速度为3.0米/秒,塔截面积:F塔=1.492/3.0=0.497(米2)
塔直径:
平均推动力ΔP为0.0182大气压,计算见低塔部分。
吸收的SO2量G=25×4.0×10=1000(公斤/时)
吸收速度系数K取120000公斤/米3·时·大气压。
填料体积
静止床层总高0.46/0.497=0.925(米),按四段设计,每段静止床高度H0=925/4==230(毫米),取H0=250毫米。
H0/D=250/790×100=31.6%。符合湍流塔设计要求H0/D在20~40%之间。
取静止床层高度为接触(湍动)区高度的20%,接触区高度(即筛板间距)为:
250/0.2=1250(毫米)
选用Φ38毫米聚乙烯空心球,每个球的重量4.5克。每段小球填充数:
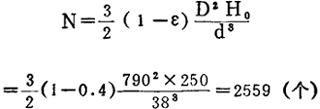
氧化镁乳液的淋洒量等于制酸量,每小时为25米3。淋洒密度为:
25/0.497=50(米3/米2·时)
由于淋洒密度大于25米3/米2·时,采用下式计算压力降:
ΔP=Aw0.28L0.44=18×30.88×500.44=153(毫米水柱)
四段总压力降为:
4×153=612(毫米水柱)
7.文氏管吸收器
(1)概述
文氏管吸收装置是由数个(一般为3~4个)文氏管吸收器串联组成。这种装置较多地用于吸收红液燃烧炉的低SO2浓度(~1%)的炉气以制备亚硫酸氢镁(或钠)溶液。由这种回收装置出来的浓度较低的酸液,在另一台文氏管或其他吸收装置中用硫铁矿(或硫黄)燃烧炉的高SO2浓度的炉气增浓。
在文氏管吸收器中,气体与液体是并流的(在数个文氏管串联的装置中,则是逆流的),气体所带的能量将液体分裂成很小的液滴,形成传质表面。
(2)影响文氏管吸收效率的参数
当文氏管吸收器用于从低SO2浓度的炉气制取亚硫酸氧镁溶液时,影响吸收效率的主要工艺参数如下:
MgSO3的影响:喷洒液中MgSO3浓度对文氏管吸收效率的影响如图6-2-49。但是提高MgSO3浓度以提高文氏管吸收效率有一定限度,因为MgSO3在酸液中的溶解度有限。

图6-2-49 喷洒液中MgSO3含量对文氏管吸收效率的影响
温度的影响:喷洒液温度对文氏管吸收效率的影响很小(图6-2-50)。在MgSO3浓度(以SO2表示)为0.5%,温度从110℉(43.4℃)提高到170℉(76.6℃)时,吸收效率下降10%。温度提高,MgSO3溶解度增加,借提高MgSO3浓度完全可以补偿温度的影响。

图6-2-50 喷洒液液温度对文氏管吸收效率的影响
浓度的影响:喷洒液浓度也是一个影响文氏管吸收效率的因素(图6-2-51)。为了能最大限度地吸收SO2,需要根据炉气中SO2浓度确定一个合适的浓度。MgSO3浓度影响文氏管吸收效率的相互关系可以下式表示:

图6-2-51 喷洒液浓度对文氏管吸收效率的影响
MgSO3浓度(以SO2表示):1-1.0% 2-0.7% 3-0.4% 4-1.0% 5-0.7% 6-0.5% 7-1.4% 8-0.7% 9-0.7%
A≈117+30M-15T-0.10t
式中 A——在文氏管中SO2吸收效率:
M——喷洒液中MgSO3浓度(以SO2表示),%;
T——喷洒液中总SO2浓度,%;
t——喷洒液的温度,℉。
(3)传质系数
文氏管的传质系数如图6-2-52。

图6-2-52 文氏管的传质系数
(4)原酸中硫酸盐含量
原酸中硫酸盐含量不仅取决于气体中氧的浓度,而且和吸收过程的作用时间有关。在用文氏管吸收器时,由于相互作用时间较短,因此可以获得硫酸盐含量低的原酸(图6-2-53)。

图6-2-53 原酸中的硫酸盐
1-4个填料塔 2-2个填料塔和2个文氏管 3-1个填料塔和3个文氏管 4-4个文氏管