硫酸盐法蒸煮液的分析计算
出处:按学科分类—工业技术 中国轻工业出版社《制浆造纸工业计算手册下册》第229页(2323字)
1.总碱量的测定计算
[说明]总碱量包括:NaOH+Na2CO3+Na2S+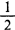 Na2SO3,以Na2O表示。总碱量的测定方法及计算公式均与烧碱法蒸煮液总碱量的测定与计算相同。
Na2SO3,以Na2O表示。总碱量的测定方法及计算公式均与烧碱法蒸煮液总碱量的测定与计算相同。
2.活性碱量的测定计算
[说明]硫酸盐法蒸煮液的活性碱量是指蒸煮液中全部NaOH和Na2S的量,以Na2O表示。活性碱量的测定方法与烧碱法蒸煮液活性碱量的测定方法相同。

式中 G1′-活性碱量(g/L)(以Na2O计)
其它同式3-1-9及式3-1-8。
3.硫化钠含量的测定计算
①碘量法
[测定方法]用移液管吸取25mL蒸煮液于100mL容量瓶中,加水稀释至刻度,摇匀。从滴定管中放出0.05M碘标准溶液25~30mL于250mL锥形瓶中,加5mL20%醋酸,并用约30mL水冲洗瓶及内壁,摇匀;然后注入10mL已稀释的蒸煮液于酸化的碘液中,摇荡瓶中液体,用0.1M硫代硫酸钠标准溶液滴定过量的碘,至淡黄色时,加淀粉指示剂,继续滴定至蓝色消失。

式中 G3-Na2S含量(g/L)(Na2S计)
M1、V1-加入碘标准溶液的摩尔浓度(mo1/L)和体积(mL)
M2、V2-滴定用硫代硫酸钠标准溶液的摩尔浓度(mol/L)及所耗体积(mL)
0.039-与1ml1mol硫代硫酸钠溶液相当的硫化钠的量(g)
②硝酸银铵法
[测定方法]用移液管吸取25mL蒸煮液于500mL锥形瓶中,由滴定管滴入标准硝酸银铵溶液。至接近终点时,剧烈摇荡使生成的硫化银凝聚成块状物,沉浮于透明的浅褐色溶液中,继续滴定,每加1滴硝酸银铵,即剧烈摇荡,直至不再有沉淀形成。记录所耗用的标准硝酸银铵溶液的量。

式中 G3′-硫化钠含量(g/L)(以Na2S计)
V-滴定时所耗用的硝酸银铵标准溶液量(mL)
0.020-1mL标准硝酸银铵溶液相当于硫化钠的量(g)
4.硫化度的测定计算
[说明]硫化度是指硫酸盐法蒸煮液中硫化钠的量占活性碱量的百分率。
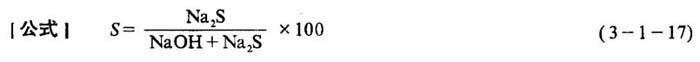



式中 S-硫化度(%)
G1′、G3-同上
0.7942、0.7748-分别为Na2S及NaOH转换成Na2O的转换系数
0.975、1.025-分别为NaOH转换为Na2S及Na2S转换成NaOH的转换系数
5.新“双指示剂”法测定各组分含量的计算
[说明]“双指示剂法”,即在蒸煮液中先后加入酚酞和甲基橙指示剂,用盐酸滴定(见烧碱法蒸煮液的测定),一次即可求出有效碱、活性碱及硫化钠含量;但由于在第一等当点酚酞变色不敏锐,终点难以控制,致使滴定波动不稳,结果误差大。新“双指示剂”法即采用百里香酚酞(pH变色范围为9.0~10.2)代替酚酞,因在第一等当点溶液的pH值为9.5,而使溶液由蓝色变无色,变色明显,易于控制终点,平行滴定波动减少。
[测定方法]吸取蒸煮液25mL置于500mL容量瓶中,加入20mL20%BaCl2使沉淀完全,再加入新煮沸冷却后不含CO2的蒸馏水,稀释至刻度,摇匀。待溶液澄清后吸取清液10mL于250mL锥形瓶中,加入20mL蒸馏水,滴入2滴百里香酚酞,溶液显蓝色,用0.1M盐酸标准溶液滴定,近终点时将溶液煮沸,继续滴定至蓝色消失,所消耗的盐酸体积为V1mL;加入2滴甲基橙,继续滴至溶液呈橙黄色,此时消耗的盐酸为V2ml。



式中 G1-NaOH含量(g/L)(以NaOH计)
G2-Na2S含量(g/L)(以Na2S计)
S-硫化度(%),计算参考式3-1-18~3-1-20
M-盐酸标准溶液的摩尔浓度,M≈0.1mol/L