分步计算法
出处:按学科分类—工业技术 中国轻工业出版社《制浆造纸工业计算手册上册》第135页(1739字)
1.中和氨用量的计算
【说明】中和氨用量需根据亚铵蒸煮液中亚硫酸铵及亚硫酸氢铵的含量来确定。按化学反应:
NH4HSO3+NH3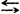 (NH4)2SO3
(NH4)2SO3
即lmol质量的NH4HSO3(99g)需要消耗1mol质量的中和氨NH3(17g),生成1mol质量的(NH4)2SO3(116g)。
如果使用固体亚硫酸铵来配制蒸煮液,根据固体亚铵的质量标准要求,亚硫酸氢铵含量应在1%以下,因此,中和氨用量可忽略不计。如果使用亚硫酸铵溶液来配制蒸煮液,溶液中主要成分是亚硫酸铵和亚硫酸氢铵,它们之间有一定的比例关系,通过测定溶液的相对密度,查阅亚硫酸铵与亚硫酸氢铵溶液的相对密度与重量百分浓度的关系表(见表1-4-1),就可以查出亚硫酸铵及亚硫酸氢铵的含量。
表1-4-1 亚硫酸铵、亚硫酸氢铵溶液相对密度与重量百分浓度的关系
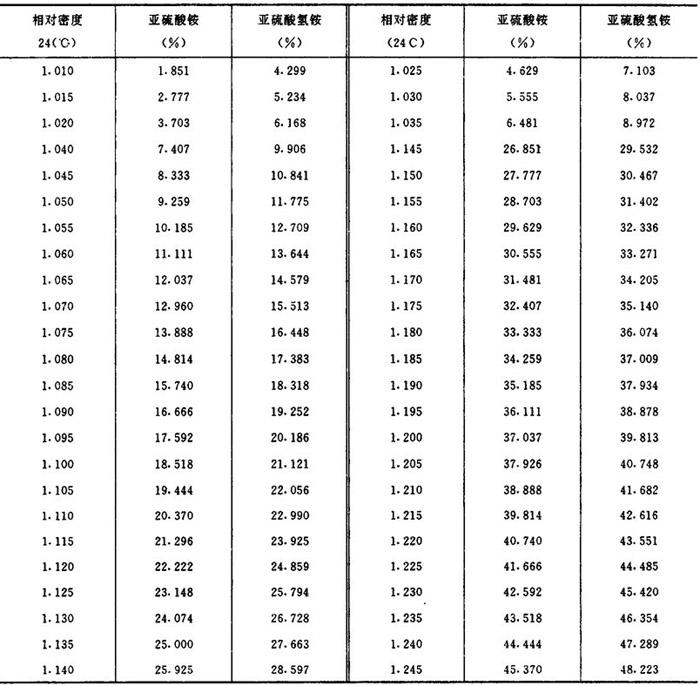
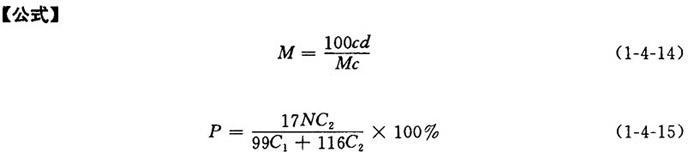
式中 M——亚硫酸铵或亚硫酸氢铵的摩尔浓度(mol/L)
c——亚硫酸铵或亚硫酸氢铵的重量百分浓度(%)
d——亚铵蒸煮液相对密度
Mc——亚硫酸铵或亚硫酸氢铵的摩尔质量
P——中和氨百分率(对绝干原料计)(%)
N——蒸煮用亚铵[(NH4)2SO3]用量(对绝干原料)(%)
C1——蒸煮液中(NH4)2SO3的含量(%)查表1-4-1
C2——蒸煮液中NH4HSO3的含量(%)查表1-4-1
17、99、116——分别为NH3、NH4HSO3以及(MH4)2SO3的摩尔质量
【例4】蒸煮用(NH4)2SO3量为13%(N),液比1:3,使用液体亚铵蒸煮液,测得相对密度为1.19,查表1-4-1知(NH4)2SO3含量为35.185%(C1),NH4HSO3含量为37.934%(C2),求中和氨的用量。
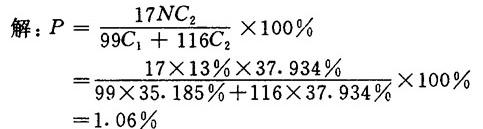
2.游离氨用量的计算
【说明】在亚硫酸铵蒸煮液中加入氨水后,先把蒸煮液中的亚硫酸氢铵中和为亚硫酸铵(这部分氨为中和氨),当继续加入氨水时为游离氨,同时形成(NH4)2SO3——NH3的缓冲体系。游离氨的加入量需根据蒸煮液中(NH4)2SO3的摩尔浓度和蒸煮液的pH值来计算。氨溶液的相对密度和浓度的关系见表1-4-2。
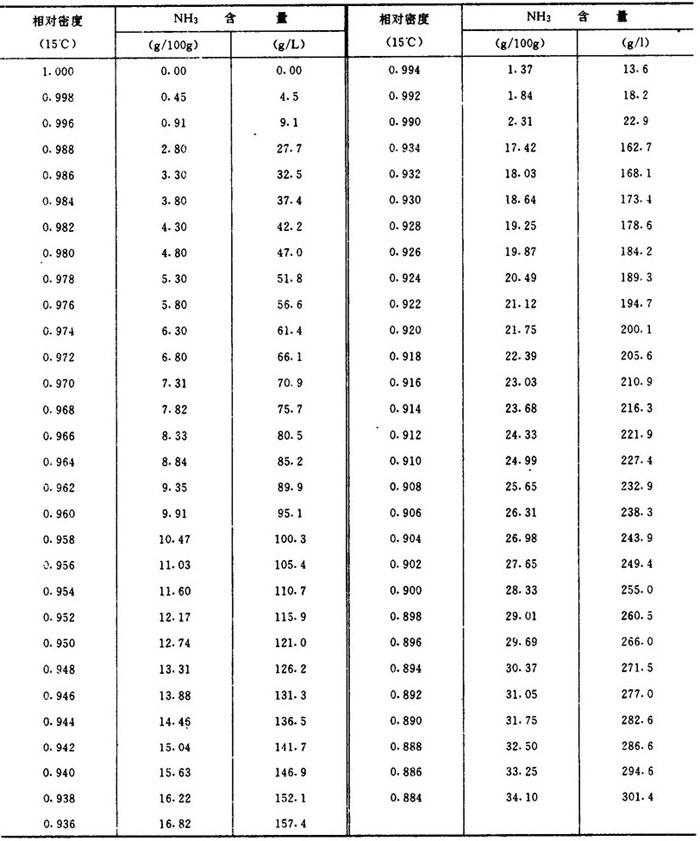
表1-4-2 氨溶液的相对密度和浓度的关系
【公式】
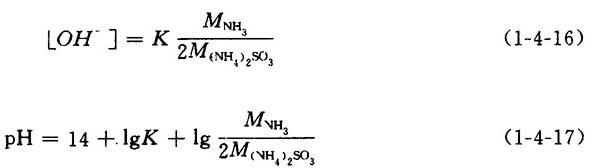
式中 M(NH1)。so3——(NH4)2SO3的摩尔浓度(mol/L)
MNH。——氨水的摩尔浓度(mol/L)
K——氨水的电离常数,K=1.8×10-5
【例5】蒸煮用(NH4)2SO3量为13%(对绝干原料),液比1:3,要求蒸煮液pH=9.0,求需要加入游离氨的量。
解:以1t绝干原料为计算基准,则蒸煮液中(NH4)2SO3浓度为:
