胶原
出处:按学科分类—工业技术 中国轻工业出版社《皮革工业手册制革分册》第32页(1945字)
(一)几种原料皮胶原的氨基酸平均组成
表1-25 几种原料皮胶原的氨基酸平均组成


(二)胶原分子结构
胶原的单体是原胶原。原胶原分子的相对分子质量为30万,呈细棒状,长30nm,直径1.5nm,它是由三条右手螺旋的α肽链拧成一股绳状右手螺旋。构成原胶原分子的多肽链有α1链和α2链。α1链又有四种形式:即α1(Ⅰ)、α1(Ⅱ)、α1(Ⅲ)、α1(Ⅳ)。这样组成原胶原分子的α肽链实际上有五种。这五种α肽链的氨基酸组成基本相似,但排列顺序不同。上述的五种α肽链组成四种不同类型的原胶原分子,见表1-26。
表1-26 不同类型的原胶原分子的α肽链组成

(三)原胶原分子的生物合成
原胶原分子的生物合成分为两个阶段;在细胞粗面内质网内生物合成前胶原分子,分泌到细胞外;在细胞外前胶原分子受内肽酶的作用切除N端区和C端区,即为原胶原分子,见图1-21和图1-22。

图1-21 原胶原分子生物合成示意图

图1-22 前胶原分子和原胶原分子结构示意图
(四)胶原纤维的形成及结构(以牛皮为例)
原胶原分子→初原纤维(Protofibril)→纤丝(Filament)或d=3.5nm
亚原纤维(Subfibril)→原纤维(Fibril)或微纤维(microfiber)→d=50~200nm
基元纤维(Primitive fiber)→纤维束(Fiber)
d=5μm d=200μm
胶原纤维形成过程见图1-23。

图1-23 胶原纤维形成过程示意图
(五)胶原的主要性质
胶原在绝干状态下是微白、硬而脆的物质,相对密度为1.4。
胶原不溶于冷水和有机溶剂。
胶原是一种两性聚电解质,牛皮胶原的等电点为7.5~7.8。在等电点时,胶原膨胀最小。胶原的酸容量为0.82~0.9mmol(一价酸或 二价酸),碱容量0.4~0.5mmol(一价碱或
二价酸),碱容量0.4~0.5mmol(一价碱或 二价碱)。
二价碱)。
胶原在酸碱溶液中发生胶解和水解。氢氧化钙的胶解能力最大。强酸的胶解能力又比强碱的大。如果强酸或强碱浓度大或处理时间过长,使胶原发生水解。制革加工过程要求胶原受到适度胶解,有利于胶原纤维结构的松散;不希望胶原过度水解,否则皮质损失过多,影响成革品质。
胶原在食盐的稀溶液中仅有微微膨胀,当食盐浓度较大时才能引起脱水作用,此时胶原的收缩温度略为提高。硫酸盐、硫代硫酸盐、碳酸盐在任何浓度下都会引起胶原脱水,但吸附性小。胶原在钙盐、镁盐、钡盐等任何浓度中都会产生剧烈膨胀,纤维束缩短,变粗,它的收缩温度也显着降低。在制革生产过程中应用中性盐的工序有浸水、脱水、浸酸等。
有些蛋白酶可以水解胶原,如胰凝乳蛋白酶、胃蛋白酶、木瓜蛋白酶、胶原酶等。胰蛋白酶仅作用变性胶原。胰蛋白酶的专一性是水解赖氨酰和精氨酰C端的肽键。它水解变性胶原的最适合条件是:pH值8.1~8.2,温度37℃。
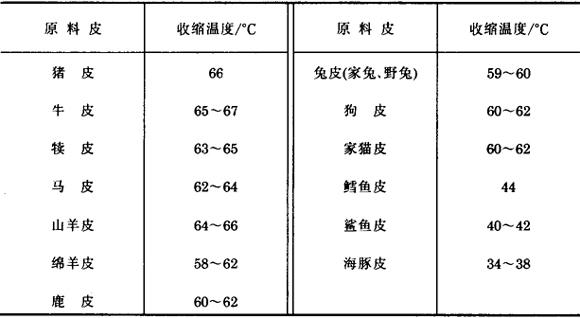
胶原纤维在水中受热到一定的温度就要自行收缩蜷曲,此时产生胶原纤维变形的水的温度,称为收缩温度,用T。表示。各种原料皮的收缩温度见表1-27。
表1-27 各种原料皮的收缩温度
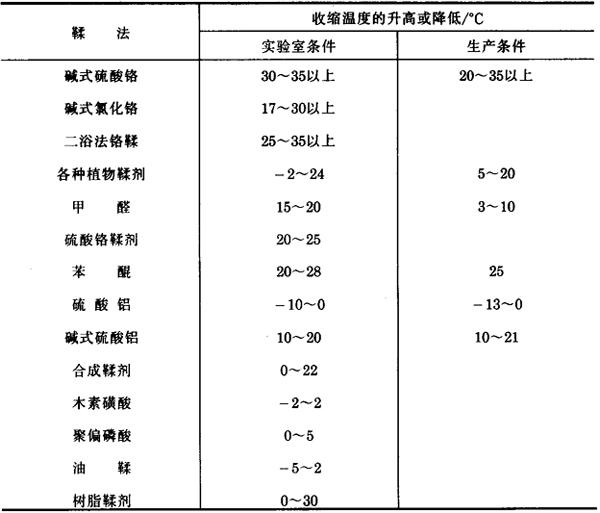
鞣制对胶原收缩温度的影响见表1-28。
表1-28 鞣制对胶原收缩温度的影响